Определение направления и средней движущей силы процесса абсорбции. Число единиц переноса (ЧЕП).
Рабочая линия , изображённая на рис.19-2, позволяет установить условия , при которых процесс абсорбции станет возможным .Рассмотрим условие равновесия газа и сорбента. Примем для этого правило фаз. В рассматриваемом случае мы имеем две фазы (газ и жидкость) и три компонента ( поглощаемый компонент, инертный газ и жидкость ) .Определяющими параметрами будут давление, температура и концентрация: S=K-f+2
Где S- число степеней свободы ,К-число компонента системы , f–число фаз системы.
В нашем случае , когда поглощается один компонент газовой смеси,S=3-2+2=3
Этими тремя степенями свободы являются состав одной из фаз , давление и температура. Содержание поглощаемого компонента в другой фазе не может быть произвольно .Оно определяется тремя выбранными параметрами .
Для идеальных растворов , в которых силы взаимодействия между молекулами компонентов системы одинаковы, условия равновесия определяются законами Генри и Рауля. Закон Генри можно сформулировать так:
х=р 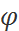 (2)
(2)
где х-количество растворённого газа , отнесённое к поглощающей жидкости, моль-доли; 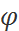 - коэффициент пропорциональности , определяемый из опыта.
- коэффициент пропорциональности , определяемый из опыта.
Уравнение 2 называется законом Генри, который может быть сформулирован так: растворимость газа прямо пропорциональна парциальному давлению газа над жидкостью .Известно также , что в газовой смеси парциальное давление компанента может быть выражено уравнением :
р=уР, (3)
где у- мольная доля рассматриваемого компанента в газовой смеси;
Р–общее давление в смеси.
Приравнивая р из уравнений 2и 3 получим,
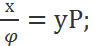 у=х/(Р
у=х/(Р 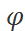 ) (4)
) (4)
Уравнение 4 является уравнением фазового равновесия.
Движущая сила процесса абсорбции может быть выражена также , как разность парциальных упругостей рассматриваемого компанента, которые пропорциональны молярной концентрации компонента. Парциальное давление поглощаемого компонента в газовой смеси обозначим через рА , равновесное парциальное давление того же компонента обозначим 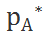 .Тогда средняя движущая сила абсорбции может быть выражена как разность (рА–
.Тогда средняя движущая сила абсорбции может быть выражена как разность (рА– 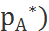 .
.

Число единиц переноса
Для газовой фазы 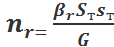
Для жидкой фазы 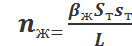
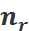 ,
, 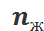 –число едниниц переноса на тарелку
–число едниниц переноса на тарелку
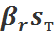 ,
, 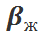 -коэффициенты массоотдачи, отнесённые к единице рабочей площади
-коэффициенты массоотдачи, отнесённые к единице рабочей площади 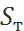
Схемы ведения процесса абсорбции(противоточная, противоточная с рециклом, каскадная). Рабочие линии процессов.
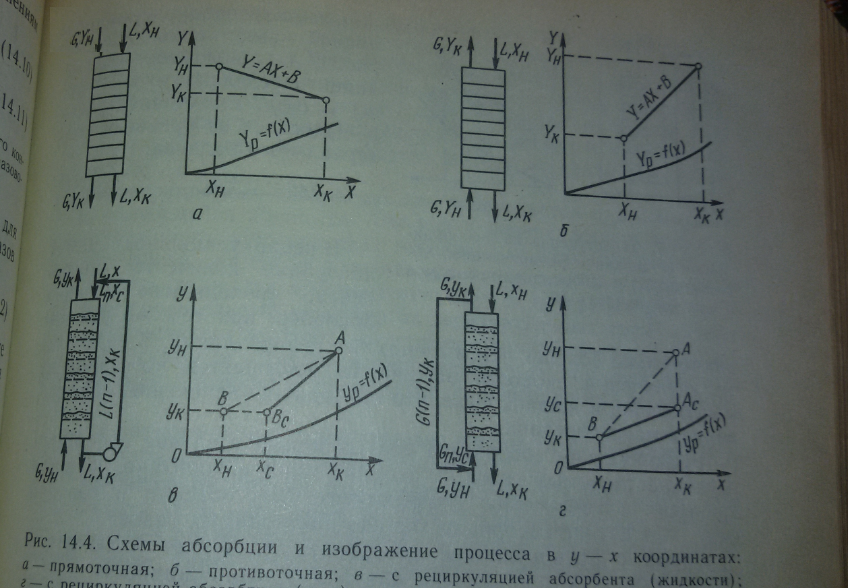
В технике используют следующие принципиальные схемы абсорбционных процессов: прямоточные, противоточные, одноступенчатые с рециркуляцией и многоступенчатые с рециркуляцией.
Прямоточная схемавзаимодействия веществ в абсорбере показана на рисунке 14.4 а. В этом случае потоки газа и абсорбента движутся в одном направлении; при этом газ с большей концентрацией абсорбтива приводится в контакт с жидкостью, имеющей меньшую концентрацию абсорбтива, а газ с меньшей концентрацией взаимодействует на выходе из абсорбтера с жидкостью, имеющей большую концентрацию абсорбтива.
Противоточная схемапоказана на рисунке 14.4, б. В противоточном абсорбере в одном конце аппарата контактируют газ и жидкость, содержащие большие концентрации абсорбтива, а в другом противоположном конце –меньшие. Э
При противоточном процессе достигается большая конечная концентрация абсорбтива в абсорбенте , чем при прямоточном. Расход абсорбента также ниже. Однако ввиду того что средняя движущая сила при противотоке ниже , то габариты противоточного абсорбера больше, чем прямоточного.
В схемах с рециркуляцией абсорбента или газовой фазыпроисходит многократный проток абсорбента или газовой фазы через абсорбер.
На рисунке 14.4, в изображена рециркуляционная схема по абсорбенту.Жидкая фаза –абсорбент многократно возвращается в абсорбер, а газовая фаза проходит через абсорбер снизу вверх .
Абсорбент подаётся в верхнюю часть абсорбера и движется противотоком к газовой фазе. В результате смешения свежего абсорбера с концентрацией хн с выходящим из абсорбера его концентрация повышается до хс .Рабочая линия на диаграмме у-х представляет собой прямую с координатами крайних точек А и Вс
Соответственно ун ,хн, ук, хс.
Дата добавления: 2018-05-02; просмотров: 1140; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
