Процесс абсорбции .Назначение, области применения и движущая сила. Уравнение материальных балансов и рабочей линии поверхности.
Процесс абсорбции
Абсорбцией называют процесс поглощения газа жидким поглотителем, в котором газ растворим в той или иной степени. Обратный процесс - выделение растворенного газа из раствора - носит название десорбции.
В абсорбционных процессах (абсорбция, десорбция) участвуют две фазы - жидкая и газовая, и происходит переход вещества из газовой фазы в жидкую (при абсорбции) или, наоборот, из жидкой фазы в газовую (при десорбции). Таким образом, абсорбционные процессы являются одним из видов процессов массопередачи.
Промышленное проведение абсорбции может сочетаться или не сочетаться с десорбцией. Если десорбцию не производят, поглотитель используется однократно. При этом в результате абсорбции получают готовый продукт, полупродукт или, если абсорбция проводится с целью санитарной очистки газов, отбросный раствор, сливаемый (после обезвреживания) в канализацию.
Сочетание абсорбции с десорбцией позволяет многократно использовать поглотитель и выделять абсорбированный компонент в чистом виде. Для этого раствор после абсорбера направляют на десорбцию, где происходит выделение компонента, а регенерированный (освобожденный от компонента) раствор вновь возвращают на абсорбцию. При такой схеме (круговой процесс) поглотитель не расходуется, если не считать некоторых его потерь, и все время циркулирует через систему абсорбер - десорбер - абсорбер.
В промышленности процессы применяются главным образом для извлечения ценных компонентов из газовых смесей или для очистки этих смесей или для очистки этих смесей от вредных примесей.
Материальный баланс и рабочая линия процесса
Примем расход фаз по высоте аппарата постоянными и выразим содержание поглощаемого газа в относительных мольных концентрациях. Обозначим: G–расход инертного газа, кмоль/сек; 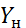 и
и 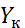 –начальная и конечная концентрации абсортива в газовой смеси, кмоль/кмоль инертного газа; L–расход абсорбента, кмоль/сек ; его концентрация;
–начальная и конечная концентрации абсортива в газовой смеси, кмоль/кмоль инертного газа; L–расход абсорбента, кмоль/сек ; его концентрация; 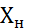 и
и  , кмоль/кмоль, абсорбента.Тогда уравнение материального баланса будет:
, кмоль/кмоль, абсорбента.Тогда уравнение материального баланса будет:
G( 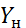 –
– 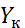 )= L(
)= L( 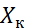 –
– 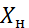 ) (1)
) (1)
Отсюда общий расход абсорбента (в кмоль/сек)
L=G 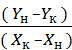
а его удельный расход( в кмоль/кмоль инертного газа)
l=  =
= 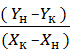
Это уравнение можно переписать так
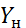 –
– 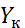 =l
=l 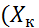 –
– 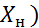
Последнее уравнение показывает, что изменение концентрации в абсорбционном аппарате происходит прямолинейно и, следовательно, в координатах Y–X рабочая линия процесса абсорбциипредставляет собой прямую с углом наклона, тангенс которого равен l=L/G.
Движущая сила
Скорость процесса абсорбции характеризуется уравнением:
M= 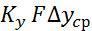 (2)
(2)
где 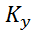 –коэффициент массопередачи;
–коэффициент массопередачи;
F–поверхность контакта фаз;
М-масса вещества, переносимого из фазы в фазу в единицу времени(нагрузку аппарата).
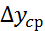 –величина средней движущей силы;
–величина средней движущей силы;
И уравнением
M= 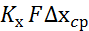 (3)
(3)
В этих уравнениях коэффициенты массопередачи определяются следующим образом:
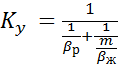 (4)
(4)
и
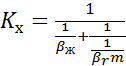 (5)
(5)
где 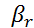 –коэффициент массоотдачи от патока газа к поверхности контакта фаз;
–коэффициент массоотдачи от патока газа к поверхности контакта фаз;
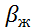 –коэффициент массоотдачи от поверхности контакта фаз к потоку жидкости;
–коэффициент массоотдачи от поверхности контакта фаз к потоку жидкости;
m–тангенс угла наклона линии равновесия;
Для хорошо растворимых газов величина m незначительна и мало также для диффузионное сопротивление в жидкой фазе.Тогда 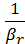 >>
>> 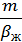 и можно принять, что
и можно принять, что 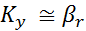 .Для плохо растворимых газов можно пренебречь диффузионным сопротивлением газовой фазе (в этом случае значения m и
.Для плохо растворимых газов можно пренебречь диффузионным сопротивлением газовой фазе (в этом случае значения m и 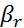 велики). Отсюда
велики). Отсюда
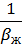 >>
>> 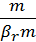 можно полагать , что
можно полагать , что 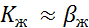 .
.
В уравнении 2 мольные концентрации газовой фазы могут быть заменены парциальным давлением газа, выраженнымв долях общего давления.Тогда
M= 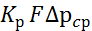 (6)
(6)
где 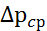 –средняя движущая сила процесса , выраженная в единицах давления;
–средняя движущая сила процесса , выраженная в единицах давления;
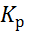 – коэффициент массопередачи, отнесённый к единице движущей силы, выражаемой через парциальные давления поглощаемого газа.
– коэффициент массопередачи, отнесённый к единице движущей силы, выражаемой через парциальные давления поглощаемого газа.
Если линия равновесия является прямой, то средняя движущая сила процесса выражается уравнением:
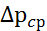 =
= 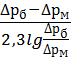 (7)
(7)
где 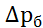 =
= 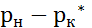 и
и 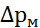 =-
=- 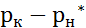 –движущая сила на концах абсорбционного аппарата;
–движущая сила на концах абсорбционного аппарата;
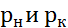 – парциальные давления газа на входе в аппарат и на выходе в него;
– парциальные давления газа на входе в аппарат и на выходе в него;
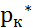 и
и 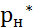 – равновесные парциальные давления газа на входе в аппарат и на выходе из него.
– равновесные парциальные давления газа на входе в аппарат и на выходе из него.
Дата добавления: 2018-05-02; просмотров: 767; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
