Круговые процессы (циклы). КПД цикла Карно
1. Циклы.Круговым процессом (циклом) называется такой процесс, при котором термодинамическая система (тело) после ряда изменений возвращается в исходное состояние. На графике цикл изображается замкнутой линией (рис.10).
После совершения цикла всякая функция состояния, например, внутренняя энергия U, принимает прежнее значение. Следовательно, ее изменение за цикл равно нулю, DU = 0.
Работа, совершаемая термодинамической системой, есть функции процесса, при переходе 1®2 газ расширяется, работа, совершаемая системой, положительна, A1®2 > 0. Графически эта работа изображается площадью фигуры под кривой перехода 1®2.
При переходе 2®1 газ сжимается под действием внешних сил. Работа отрицательна, A2®1 < 0. Графически она изображается площадью фигуры под кривой перехода 2®1.
Суммарная работа, совершаемая газом в цикле, в котором система возвращается в исходное состояние другим путем, не равна нулю. Графически она определяется площадью фигуры между кривыми перехода 1®2 и 2®1. A = A1®2 +A2®1.
Если цикл протекает по часовой стрелке, работа цикла положительна. Такой цикл называют прямым. Газ в прямом цикле преобразует часть подводимой к нему извне теплоты в механическую работу (рис.11).

Если цикл совершается против часовой стрелки, работа цикла отрицательна. Газ в обратном цикле преобразует совершаемую над ним работу внешних тел в теплоту (рис.12).
2. Цикл Карно. Прямой цикл может использоваться для превращения теплоты в работу. Он открывает путь к созданию тепловых машин.
|
|
|
Для реализации цикла нужны 3 тела: нагреватель – более нагретое тело, холодильник – менее нагретое тело, рабочее тело – в нашем случае – идеальный газ. Форма циклов может быть какой угодно, лишь бы они были замкнуты.
 В 1824 г. Сади Карно предложил цикл, составленный из двух изотерм и двух адиабат. Исследование этого цикла позволило выявить в нем замечательные свойства и использовать его позднее как метод изучения термодинамических систем.
В 1824 г. Сади Карно предложил цикл, составленный из двух изотерм и двух адиабат. Исследование этого цикла позволило выявить в нем замечательные свойства и использовать его позднее как метод изучения термодинамических систем.
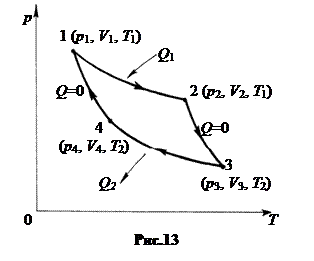
Пусть рабочим телом являются n молей идеального газа, исходное состояние 1 которого имеет параметры p1, V1, T1 (рис.13).
Теплоемкость нагревателя и холодильника полагаем настолько большой, что их температуры при теплообмене с рабочим телом не меняются. Такие тела называют еще термостатами. Температура холодильника T2 < T1. Рассмотрим процессы цикла.
а. Изотермическое расширение 1®2, T1 = const. В исходном состоянии 1 рабочее тело (идеальный газ) имеет тепловой контакт с нагревателем. Газ расширяется при T1 = const, давление падает по изотерме от p1 до p2. Подводимая к газу теплота полностью превращается в работу, так как изменение внутренней энергии DU1®2 = 0.  . (4.1)
. (4.1)
|
|
|
б. Адиабатное расширение 2®3, Q2®3 = 0. Рабочее тело теплоизолируется и расширяется от объема V2 до объема V3 так, что его температура падает от температуры нагревателя T1 до температуры холодильника T2. Работа расширения газа совершается за счет его внутренней энергии.  . (4.2)
. (4.2)
в. Изотермическое сжатие 3®4, T2 = const. Газ сжимается внешними телами при температуре холодильника T2 от объема V3 до V4. Работа сжатия выделяется в виде теплоты Q2 и через тепловой контакт отдается холодильнику. Изменение внутренней энергии DU3®4 = 0.
 . (4.3)
. (4.3)
г. Адиабатное сжатие 4®1, Q4®1 = 0. Газ теплоизолируется и адиабатно сжимается внешними телами до параметров начального состояния p1, V1, T1. Работа адиабатного сжатия на последнем этапе  . (4.4)
. (4.4)
3. Суммарная работа цикла A = A1®2 + A2®3 + A3®4 + A4®1 = A1®2 + A3®4 (4.5)
определяется лишь изотермическими процессами. В адиабатических процессах работа одинакова по величине, но противоположна по знаку. Поэтому ее сумма равна нулю.
 . (4.6)
. (4.6)
|
|
|
Итак, 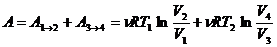 . (4.7)
. (4.7)
Так как  , то
, то  . (4.8)
. (4.8)
4. КПД цикла Карно. Полная работа цикла равна алгебраической сумме работ, совершаемых рабочим телом в изотермических процессах. При изотермическом расширении газа работа равна полученной от нагревателя теплоте Q1 = A1®2 = nRT1 ln(V2| V1).
При изотермическом сжатии часть этой теплоты в количестве Q2 = A3®4 = nRT2 ln(V3| V4) отдается холодильнику. Следовательно, при полном цикле в работу превращается не вся теплота Q1, полученная от нагревателя, а лишь часть ее Q1 - Q2.
Эффективность функционирования любой тепловой машины определяется коэффициентом полезного действия h, равным отношению работы A к количеству полученной от нагревателя теплоты Q1.  . (4.9)
. (4.9)
Коэффициент полезного действия идеального цикла Карно
 . (4.10)
. (4.10)
Это выражение можно упростить. Запишем уравнения левой и правой адиабат (по рис.13) в параметрах T и V.
Левая, T1V1g-1 = T2V4g-1, (4.11)
|
|
|
Правая, T1V2g-1 = T2V3g-1. (4.12)
Разделив 2-е уравнение на 1-е получаем:  .
.
Логарифмы в (4.10) сокращаются, и получаем:
 . (4.13)
. (4.13)
Полученная формула выражает первую теорему Карно: коэффициент полезного действия тепловой машины, работающей по идеальному циклу Карно, зависит только от температур Т1 и T2 нагревателя и холодильника, но не зависит от устройства машины и вида используемого рабочего вещества.
Из теоремы Карно следует, что без перепада температур нельзя теплоту превратить в работу.
КПД идеального цикла Карно является наибольшим из всех реальных и мыслимых процессов. Этот факт составляет содержание 2-й теоремы Карно: коэффициент полезного действия всякой тепловой машины не может превосходить коэффициента полезного действия идеальной машины, работающей по циклу Карно с теми же самыми температурами T1 и T2 нагревателя и холодильника.
5. Термодинамическая шкала температур. В 1848 г. Уильям Томсон (Кельвин) предложил построить такую температурную шкалу, которая бы не зависела от термометрических свойств реальных тел. Суть его идеи в том, что процесс измерения температуры T1 некоторого тела реализуется путем проведения цикла Карно между этим телом и некоторым другим телом, температура которого T0 принимается эталонной. Тогда, как следует из формулы (4.13), количество тепла Q1, полученного от исследуемого тела, пропорционально температуре T1.
Для построения шкалы нужно выбрать эталонную (опорную) температуру и приписать ей определенное численное значение.
В 1954 г. 10-я Генеральная конференция по мерам и весам утвердила в качестве опорной температуру тройной точки воды и приписала ей значение 273,16 К точно.
Температуры плавления льда и кипения воды при нормальном атмосферном давлении составляют 273,15 К и 373,15 К приближенно.
Понятия “шкала Кельвина” и “абсолютная термодинамическая шкала температур” в сегодняшнем понимании идентичны.
Конечно, цикл Карно позволяет построить температурную шкалу лишь в принципе. Для практических измерений температуры он не пригоден. На практике эмпирическая температура измеряется всегда с помощью каких-либо реальных термометров. Задача сводится лишь к определению поправок к показаниям таких термометров.
Лучшим приближением к термодинамической шкале являются идеальные газовые термометры, для которых поправок не требуется. Но и идеальных газов в природе нет. Поэтому для практических целей используются реальные газы, приближающиеся по своим свойствам к идеальным. Наиболее подходит для этих целей гелий.
Дата добавления: 2018-04-15; просмотров: 1093; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
