Материальное обеспечение работы
1.Исходная вода – суспензия – 3 дм3 .
2. Лабораторные цилиндры по 500 мл – 5 шт.
3. Растворы реагентов – 1% Al2(SO4)3 - 0,5 дм3
0,1% ПАА - 0,25 дм3
0,1% ППС - 0,25 дм3
0,1н HCl - 0,25 дм3
4. Дистиллированная вода - 3 дм3
5. Фотоэлектроколориметр КФК-2
6. РН-метр
7. Метилоранж
8. Пипетки на 0,5 и 2,0 см3 – 2 шт.
9. Мерный цилиндр на 200 см3 – 5 шт.
Порядок выполнения работы
1. Определить мутность пробы шахтной воды на приборе КФК-2 по методике лабораторной работы №1.
2. Определеить щелочность пробы шахтной воды по методике, изложенной в приложении 4.
3. Определить рН пробы шахтной воды по методике, изложенной в приложении 5.
4. Определить дозы коагулянта и флокулянта из табл. 16, 17 СНиП 2.04.02-84 (приложение 6).
5. Налить в 5 цилиндров по 500 см3 пробы воды.
6. В первый цилиндр ввести расчетную дозу коагулянта (1-%ный раствор сернокислого алюминия), быстро смешать 5-кратным опрокидыванием цилиндра, а затем медленно перемешивать суспензию в течение 10 – 15 мин, наблюдая за процессом хлопьеобразования и осаждения. Отметить момент начала хлопьеобразования (опалесценции, появления видимых глазом хлопьев) и конца осаждения хлопьев
7. Во второй цилиндр ввести расчетную дозу коагулянта, а через 2 мин - флокулянта ПАА (0,1%ный раствор), наблюдать за процессом.
8. В третий цилиндр ввести коагулянт с флокулянтом ППС (0,1%ный раствор), наблюдать за процессом.
|
|
|
9. В четвертый цилиндр ввести только флокулянт ПАА, в пятый – только ППС. Каждый раз наблюдать за процессом.
10. После завершения процесса осаждения хлопьев определить мутность, щелочность и рН проб отстоянной воды.
11. Результаты опытов занести в таблицу, сделать выводы об эффективности каждого режима.
Изучение эффективности режимов коагулирования.
| 1 | Показатель | Единица измерения | Обозначение | Метод определения | Значение показателя при режиме обработки | ||||||
| Коагулянт (К) | К + ПАА | К + ППС | ПАА | ППС | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | ||
| Данные исходной воды: | |||||||||||
| 1 | Мутность | мг/л | Мо | КФК-2 | |||||||
| 2 | Щелочность | мг-экв/л | Щисх | Приложение 4 | |||||||
| 3 | РН | рН-метр | |||||||||
| Дозы реагентов: | |||||||||||
| 4 | Коагулянт | мг/л | Дк | Приложение 6 | |||||||
| 5 | ПАА | мг/л | Дф | Приложение 6 | |||||||
| 6 | ППС | Дф | Приложение 6 | ||||||||
| Объем раствора реагентов для обработки: | |||||||||||
| 7 | Коагулянт | мл | Wк | Wк = Дк / 10 | |||||||
| 8 | ПАА | мл | Wф | Wф = Дф | |||||||
| 9 | ППС | мл | Wф | Wф = Дф | |||||||
| Данные воды после обработки:
| |||||||||||
| 10 | Мутность | мг/л | КФК-2 | ||||||||
| 11 | Щелочность из опыта | мг-экв/л | Приложение 4 | ||||||||
| 12 | Щелочность по расчету | мг-экв/л | Щобр | Формула 2.1 | |||||||
| 13 | РН | рН-метр | |||||||||
| Результаты наблюдений: | |||||||||||
| 14 | Опалесценция через | сек | |||||||||
| 15 | Появление хлопьев через | сек | |||||||||
| 14 | Конец осаждения хлопьев через | сек | |||||||||
Лабораторная работа № 4
ОПРЕДЕЛЕНИЕ ОПТИМАЛЬНОЙ ДОЗЫ КОАГУЛЯНТА ДЛЯ ОБЪЕМНОЙ КОАГУЛЯЦИИ ВЗВЕШЕННЫХ ПРИМЕСЕЙ ШАХТНЫХ ВОД
Цель работы - овладеть стандартной методикой определения оптимальных доз коагулянтов при очистке шахтных вод от взвешенных веществ отстаиванием.
Теоретические основы работы
Сокращение времени отстаивания и достижение эффективной степени очистки воды достигается путем применения реагентов – коагулянтов и флокулянтов
|
|
|
Коагуляция- это процесс укрупнения дисперсных частиц в результате их взаимодействия и объединения в агрегаты. В процессах очистки вод коагуляция происходит под влиянием добавляемых к ним специальных веществ – коагулянтов. Коагулянты в воде образуют хлопья гидратов оксидов металлов, которые имеют слабый положительный заряд. В то же время тонкодисперсные взвешенные частицы, находящиеся в воде, имеют слабый отрицательный заряд. В момент образования хлопьев захватываются взвешенные в воде частицы и частично бактерии. Хлопья вместе с захваченными взвесями быстро оседают под действием силы тяжести, вода осветляется. Процесс гидролиза коагулянтов и образования хлопьев происходит по следующим стадиям:

 Me3+ + HOH Me(OH)2+ + H+
Me3+ + HOH Me(OH)2+ + H+

 Me(OH)2+ + HOH Me(OH)2+ + H+
Me(OH)2+ + HOH Me(OH)2+ + H+


 Me(OH)2+ + HOH Me(OH)3 + H+
Me(OH)2+ + HOH Me(OH)3 + H+
 |

 Me3+ + 3HOH Me(OH)3 + 3H+
Me3+ + 3HOH Me(OH)3 + 3H+
В качестве коагулянтов обычно используют соли алюминия, железа или их смеси. Выбор коагулянта зависит от его состава, физико-химических свойств и стоимости.
Из солей алюминия в качестве коагулянтов используют сульфат алюминия Al2 (SO4)3 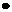 18H2O; алюминат натрия NaAlO2; оксихлорид алюминия Al2(OH)3Cl; квасцы алюмокалиевые KAl(SO4)2
18H2O; алюминат натрия NaAlO2; оксихлорид алюминия Al2(OH)3Cl; квасцы алюмокалиевые KAl(SO4)2 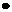 12H2O. Из этих соединений наиболее распространен сульфат алюминия, который эффективен в интервале значений рН 5-7,5. Он хорошо растворим в воде, имеет относительно низкую стоимость.
12H2O. Из этих соединений наиболее распространен сульфат алюминия, который эффективен в интервале значений рН 5-7,5. Он хорошо растворим в воде, имеет относительно низкую стоимость.
|
|
|
Из солей железа в качестве коагулянтов используют сульфаты железа: Fe(SO4)3 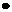 2H2O , Fe2(SO4)3
2H2O , Fe2(SO4)3 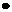 3H2O , FeSO4
3H2O , FeSO4  7H2O, а также хлорное железо FeCl3 . Наибольший эффект осветления имеет место при использовании солей трехвалентного железа. Образование хлопьев протекает по реакциям:
7H2O, а также хлорное железо FeCl3 . Наибольший эффект осветления имеет место при использовании солей трехвалентного железа. Образование хлопьев протекает по реакциям:
 FeCl3 + 3H2O Fe(OH)3 + 3HCl
FeCl3 + 3H2O Fe(OH)3 + 3HCl
 Fe2(SO4)3 + 6H2O 2Fe(OH)3 + 3H2SO4
Fe2(SO4)3 + 6H2O 2Fe(OH)3 + 3H2SO4
Оптимальная доза коагулянта зависит от его вида, содержания взвешенных и коллоидных примесей в воде, их дисперсности, температуры и рН воды. Определяется путем пробного коагулирования проб испытуемой воды.
Дата добавления: 2018-04-05; просмотров: 203; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
