Билет №12. Общая характеристика солей алюминия, их растворимость, гидролиз. Галогениды, строение их молекул и свойства. Комплексные соединения. Квасцы
Соли алюминиярастворимы в воде, за исключением AlPO4. В растворах соли алюминия гидролизуются. Вследствие гидролиза сульфид, карбонат, цианид и некоторые другие соли алюминия из водных растворов получить не удаётся: 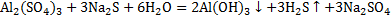 .
.
Галогениды AlX3 (где X – F, Cl, Br, I) – бинарные соединения алюминия с фтором. AlF3 резко отличается от остальных галогенидов (AlCl3, AlBr3, AlI3). В отличии от остальных галогенидов AlF3 хорошо растворяется в воде (но гидролиз неполный и обратимый) и является весьма нереакционноспособным веществом. В парообразном состоянии AlCl3, AlBr3, AlI3 состоят из димерных молекул Al2X6:
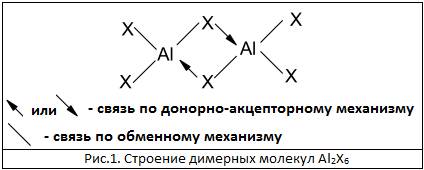
Свойства AlX3:
1. 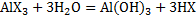
2. 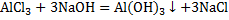
2. 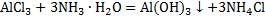
Алюминий является лучшим комплексообразователем среди s- и p-металлов (с алюминием может сравниться только диагональный аналог – бериллий). В своих координационных соединениях Al3+ стремится к октаэдрической и тетраэдрической координации. Для алюминия известны аква-, гидроксо-, фторо-, а также цианидные и роданидные комплексы.
Квасцы Me2SO4 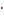 Al2(SO4)3
Al2(SO4)3 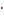 24H2O – двойные соли, образуемые сульфатом алюминия Al2(SO4)3 и сульфатом металла в степени окисления +1 (например, K2SO4
24H2O – двойные соли, образуемые сульфатом алюминия Al2(SO4)3 и сульфатом металла в степени окисления +1 (например, K2SO4 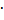 Al2(SO4)3
Al2(SO4)3  24H2O – алюмокалиевые квасцы).
24H2O – алюмокалиевые квасцы).
Дата добавления: 2018-04-04; просмотров: 423; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
