Билет №10. Оксид бора, борные кислоты, галогениды, способы получения, строение молекул и свойства. Нитрид бора – строение молекулы и свойства. Боразон
Оксид бора B2O3 – бинарное соединение бора с кислородом. Существуют 2 аллотропные модификации оксида бора: кристаллический бор и аморфный бор. Оксид бора обладает кислотными свойствами.
Кристаллический B2O3 пассивен.
Свойства аморфного B2O3:
1.  .
.
2. 

3. 
Получение B2O3:
1. 
Борные кислотыили оксобораты водорода:
· H3BO3 – ортоборная или борная кислота
· HBO2 – метаборная кислота
· H2B4O7 – тетраборная кислота со следующим строением:

Свойства борных кислот:
1. 
2. 
3. 
4. 
Галогениды бора BX3(где Х – F, Cl, Br, I) –бинарные соединения бора с галогенами. Существуют следующие галогениды бора:
· BF3 – газ
· BCl3 – жидкость
· BBr3 – жидкость
· BI3 – твёрдое вещество
Все галогениды бора обладают кислотными свойствами.
Свойства галогенидов бора:
1. Гидролиз BCl3, BBr3, BI3: 
Гидролиз BF3: 
Вследствие этого BCl3 и BBr3 во влажном воздухе дымят, а BI3 с водой протекает со взрывом.
2. 
Нитрид бора BN – бинарное соединение бора с азотом. Существует 2 аллотропные модификации нитрида бора:
· α-модификация – белый графит (графитоподобная модификация с гексагональной атомно-слоистной структурой)
· β-модификация – боразон (алмазоподобная модификация)
Свойства BN:
1.  -
-  -
- 
2. 
3. 
Билет №11. Алюминий – получение, свойства, применение. Алюмотермия. Оксид, гидроксид – получение и свойства. Алюминаты. Алюмосиликаты.
Алюминий – второй типический элемент IIIA группы ПСМ с электронной формулой []3s23p1. Алюминий является типичным амфотерным элементом. Он имеет степень окисления +3 и координационное число 4 и 6, является сильным восстановителем, обладает высокой электрической проводимостью и теплопроводностью, на воздухе покрывается оксидной плёнкой.
Получение алюминия:
1. В промышленности электролизом раствора Al2O3 в расплавленном криолите Na3[AlF6]:

Свойства алюминия:
1. 
2. 
3.  (где X – Cl, Br)
(где X – Cl, Br)

4. 
5. 
6. Взаимодействие с водой, если с поверхности алюминия удалена оксидная плёнка (например,
амальгированием ртутью):
 .
.
7.  .
.
8. Восстановление многих металлов из оксидов (этот процесс называется алюмотермией):

Применение алюминия:
1. Для перевозки концентрированной азотной кислоты (т.к. при взаимодействии азотной кислоты с алюминием толщина оксидной плёнки на поверхности алюминия увеличивается).
Оксид алюминия Al2O3 – бинарное соединение алюминия с кислородом, обладающее амфотерными свойствами.
Получение Al2O3:
1. 
2. 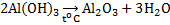
Свойства Al2O3:
1. 
2. 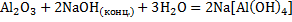

Гидроксид алюминия алюминия Al(OH)3 –соединение, обладающее амфотерными свойствами.
Свойства Al(OH)3:
1. Осушение приводит к образованию активной формы Al2O3 – алюмогеля (это пористое вещество,
отличающееся от обычного порошка Al2O3): 
1. 
2. 

Получение Al(OH)3:
1.  .
.
Алюминаты— соли, образующиеся при действии щёлочи на свежеосаждённый гидроксид алюминия либо растворением металлического алюминия в щелочах (реакции выше). Пример алюмината: Na[Al(OH)4].
Алюмосиликаты — группа природных и синтетических силикатов, комплексные анионы которых содержат кремний и алюминий. Наибольший интерес представляют цеолиты – кристаллические вещества, состоящие преимущественно из алюмосиликатов. Цеолиты бывают природные и синтетические. При обычных условиях поры цеолитов заполнены водой. При нагревании воды выделяется в виде пара и цеолит “кипит”. После удаления воды полости цеолита могут быть заполнены другими веществами, критический размер которых меньше диаметра входного окна d0. Таким образом, цеолиты используются в качестве молекулярных сит, с помощью которых можно разделять вещества. Например, схема разделения смеси н-гексана и бензола на цеолите CaA:

Как видно из рисунка, диаметр молекул н-гексана меньше диаметра окна (4,9Å<5Å), поэтому они легко проникают в полости цеолита. Диаметр молекул бензола больше диаметра окна (6Å>5Å), поэтому они проходят через слой гранул цеолита, не задерживаясь.
Дата добавления: 2018-04-04; просмотров: 1192; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
