Ферменты и коферменты дыхательной цепи
НАД –зависимые дегидрогеназы.
В качестве кофермента содержат НАД и НАДФ. Пиридиновое кольцо никотинамида способно присоединять электроны и протоны водорода.
НАД-зависимая дегидрогеназа расположена на матриксной поверхности внутренней мембраны митохондрий отдает пару электронов водорода на ФМН-зависимую дегидрогеназу. При этом из матрикса пара протонов переходит также на ФМН и в результате образуется ФМН Н2. В это время пара протонов, принадлежащих НАД выталкивается в межмембранное пространство.
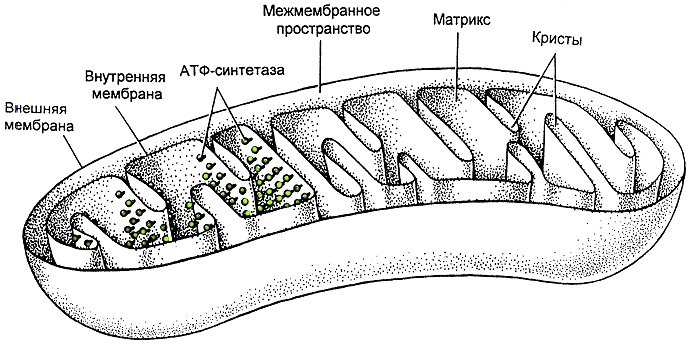
Строение митохондрий
Субстратами НАД-зависимых дегидрогеназ являются спирты, альдегиды, амины, дикарбоновые и кетокислоты. Все НАД-зависимые дегидрогеназы являются анаэробными дегидрогеназами, то есть посылают атомы водорода на ближайший в окислительной цепи другой фермент.
Примером НАД-зависимой дегидрогеназы является алкогольдегидрогеназа из печени животных. Фермент состоит из двух субъединиц, каждая из которых несет молекулу НАД+ и атом Zn. Он катализирует реакцию окисления спирта в альдегид.

ФАД-зависимые дегидрогеназы.
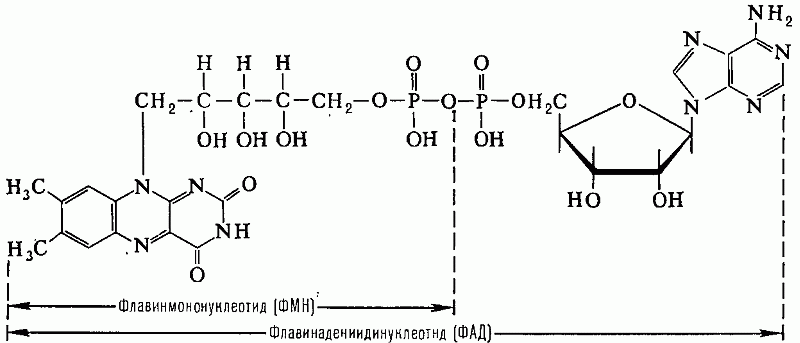
Флавиновые дегидрогеназы содержат в качестве простетических групп ФАД или ФМН. Рабочей частью ФАД и ФМН является витамин В2, к которому присоединяются от окисляемого субстрата два протона Н+ и два электрона.
Большинство ФАД-зависимых дегидрогеназ – растворимые белки, локализованные в матриксе митохондрий. Они являются акцепторами протонов Н+ и электронов от субстратов: ацил-КоА, глицерол-3-фосфат и др.
Исключение составляет сукцинат-фумарат дегидрогеназа, находящаяся во внутренней мембране митохондрий - это II комплекс в ЦПЭ. Она является акцептором протонов Н+ и электронов от субстрата – янтарная кислота (сукцинат).
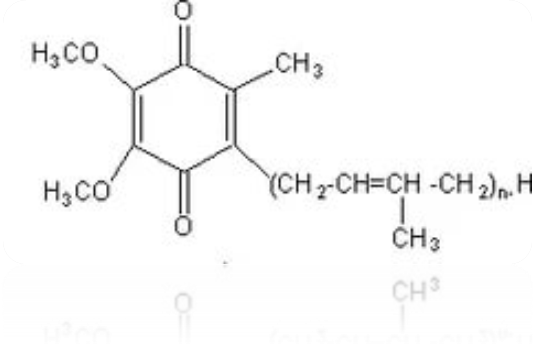
3. Убихинон (коэнзимQ10). Убихинон –это жирорастворимый хинон с длинной изопреноидной боковой цепью. Он найден практический во всех клетках. Количество изопреноидных единиц отображается в названии. В большинстве животных клеток и клеток млекопитающих присутствует убихнон с количеством изопреноидных единиц -10: Ко Q10.
 ВорганизмечеловекакоэнзимQ10синтезируетсяизмевалоновойкислотыипродуктовобменатирозинаифенилаланина. Кофермент Q принимает участие в реакциях окислительного фосфорилирования, является компонентом цепи переноса электронов в митохондриях. Ингибиторы работы убихинона останавливают реакции окислительного фосфорилирования.
ВорганизмечеловекакоэнзимQ10синтезируетсяизмевалоновойкислотыипродуктовобменатирозинаифенилаланина. Кофермент Q принимает участие в реакциях окислительного фосфорилирования, является компонентом цепи переноса электронов в митохондриях. Ингибиторы работы убихинона останавливают реакции окислительного фосфорилирования.
АнтиоксидантнаяактивностькоэнзимаQ10болеечемв2разапревышаеттаковуюстандартногокомплексавитаминов-антиоксидантов.
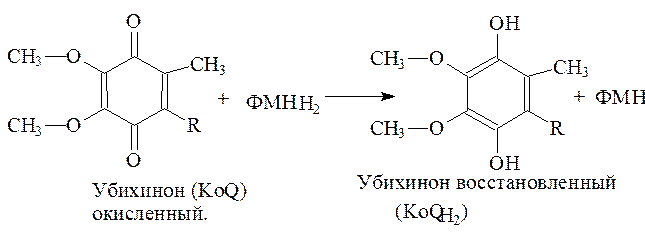
4. Цитохромы-это гемопротеины, белки, содержащие в качестве прочно связанной простетической группы гем с Fe+3, окрашенные вкрасный или коричневый цветЦитохромы — это гемопротеины, характерной особенностью которых является перенос электронов, сопряженный с обратным изменением степени окисления простетической группы. Это изменение окислительно-восстановительного состояния включает обратимое равновесие между Fe2+ и Fe3+ состояниями гема:
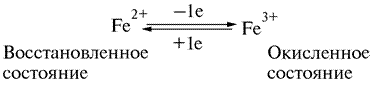
Цитохромы относятся к одноэлектронным окислительно-восстановительным соединениям. Οʜᴎ не могут принимать или отдавать водород, в связи с этим их называют переносчиками электронов. Цитохромы присутствуют во многих тканях животного, растительного и бактериального происхождения. Цитохромы подразделяются на цитохромы a, b, c и d в соответствии с положением их спектральных полос поглощения в восстановленном состоянии.

Структура гема цитохрома
5. Цитохромоксидаза(a и a3)содержат кроме гема катион меди Сu+2. Цитохромоксидаза,цитохром, а, a3, фермент класса оксидоредуктаз, конечный компонент цепи дыхательных ферментов, переносящий электроны от цитохрома с на молекулярный кислород. Цитохромоксидаза открыта в 1926 году немецким учёным О. Варбургом (т. н. «дыхательный фермент Варбурга»). В растительных и животных клетках локализована во внутренней мембранемитохондрий. По химической природе цитохромоксидаза — сложный белок, в состав молекулы которого входят два гема, два атома меди, а также 20—30% липидного компонента. Оба гема представлены гемом а, но только часть гема а окисляется кислородом и обозначается a3. Связь меди с белком осуществляется через S-содержащий лиганд. При отделении меди Цитохромоксидаза теряет активность. Молекулярная масса цитохромоксидаза (по разным данным) от 50 000 до 240 000 Да. Ингибиторами цитохромоксидазы являются цианид, азид, CO, гидроксиламин
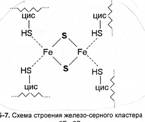 6. Железосерные белки – Fe-S-белки, это окислительно-восстановительные системы, переносящие электроны. Железосерные белки (FeS-белки) содержат атомы железа связанные, с одной стороны, с серой аминокислоты цистеина, а с другой – с неорганической сульфидной серой.Железосерные белки имеют небольшую молекулярную массу около 10 кДа. Дыхательные цепи содержат большое число FeS-центров. Эти белки участвуют в переносе протонов и электронов и, как предполагают, на нескольких стадиях. Однако до сих пор не ясен механизм, по которому железосерные белки претерпевают обратимое окисление-восстановление. Наиболее известный белок из этого семейства, называется ферредоксином.
6. Железосерные белки – Fe-S-белки, это окислительно-восстановительные системы, переносящие электроны. Железосерные белки (FeS-белки) содержат атомы железа связанные, с одной стороны, с серой аминокислоты цистеина, а с другой – с неорганической сульфидной серой.Железосерные белки имеют небольшую молекулярную массу около 10 кДа. Дыхательные цепи содержат большое число FeS-центров. Эти белки участвуют в переносе протонов и электронов и, как предполагают, на нескольких стадиях. Однако до сих пор не ясен механизм, по которому железосерные белки претерпевают обратимое окисление-восстановление. Наиболее известный белок из этого семейства, называется ферредоксином.
Железосерные белки-это окислительно-восстановительные системы, переносящие электроны. Они содержат атомы железа, связанные, с одной стороны, с серой аминокислоты цистеина, а с другой-с неорганической сульфидной серой. Последняя очень легко отщепляется в виде сероводорода при подкислении. Остатки цистеина входят в состав полипептидных цепей Fe-S-центры можно рассматривать как простетические группы полипептида. Участвующие в дыхательной
Дата добавления: 2018-02-28; просмотров: 5165; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
