Организация дыхательной цепи
Окисление субстратов в процессе дыхания можно представить как перенос электронов и протонов (т. е. атомов водорода) от органических веществ на кислород. В этом процессе участвует ряд промежуточных переносчиков, образующих дыхательную цепь.
Дыхательная цепь (электронотранспортная цепь, цепь переноса электронов) - система трансмембранных белков и переносчиков электронов, которые передают электроны от субстратов на кислород. В клетках эукариот дыхательная цепь расположена во внутренней мембране митохондрий в виде 4 ферментных и АТФ-азного комплексов в соответствии с возрастанием окислительно-восстановительного потенциала.
1комплекс -В переносе электронов в толще мембраны митохондрий главную роль выполняет дыхательная цепь. Первый комплекс транспортной цепи принимает на себя молекулы НАД*Н+ (у животных) или НАДФ*Н+ (у растений) с последующим отщеплением четырех протонов водорода. I комплекс также называется НАДН – дегидрогеназой (по названию центрального фермента). В состав дегидрогеназного комплекса входят железосерные белки 3 видов, а также флавинмононуклеотиды (ФМН).Пиридинзависимые дегидрогеназы осуществляют перенос электронов и протонов (водорода) от субстрата. НАДН2, образовавшийся в цикле Кребса, в результате гликолиза и других окислительно-восстановительных процессов, окисляется дегидрогеназой (комплекс I), которая отбирает у него два электрона и протона и переносит их на растворимый в липидах убихинон (во внутреннюю мембрану митохондрий). Во время этого процесса комплекс I перекачивает протоны из матрикса в межмембранное пространство митохондрий.
|
|
|
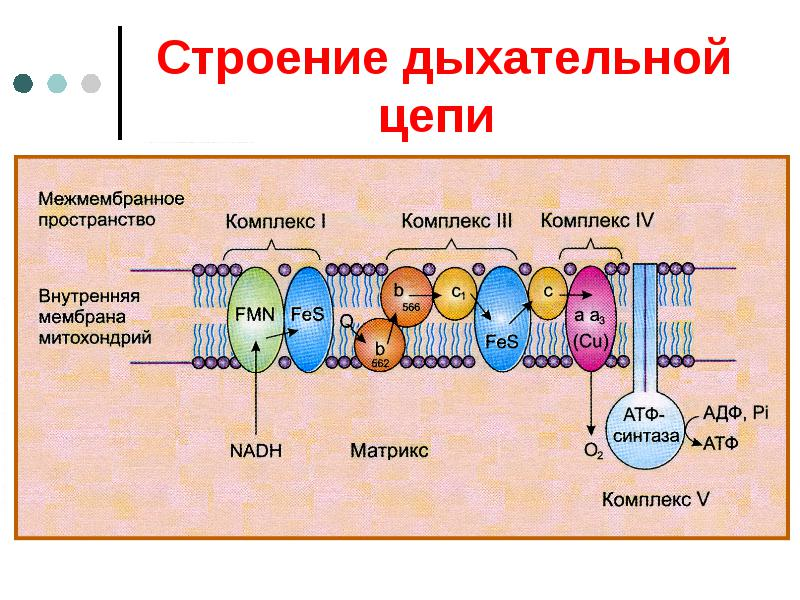
2 комплекс - Флавинзазисимые дегидрогеназы в качестве кофермента содержат ФАД+ или ФМН. К флавинзависимым дегидрогеназам относится сукцинатдегидрогеназа.ФАДН2 окисляется сукцинатдегидрогеназой (комплекс II). При этом процессе протоны не перекачиваются через мембрану, но убихинон получает дополнительные электроны и протоны.
3 комплекс. Восстановленный убихинон (гидрохинон) отдаёт электроны на цитохромный комплекс (комплекс III), а он в свою очередь переносит электроны на два водорастворимых цитохрома с, расположенных на внутренней мембране митохондрии. При этом процессе также переносятся протоны убихинона, которые перекачиваются комплексом.
4 комплекс.Конечным акцептором электронов в дыхательной цепи является кислород. Передачу электронов на кислород осуществляет цитохромоксидаза (комплекс). При этом комплексом IV перекачиваются протоны в межмембранное пространство. Цитохромоксидаза отдаёт электроны на кислород и активирует его. В заключение активированный кислород с двумя протонами образует воду.В итоге при переносе электронов и протонов в дыхательной цепи или цепи переноса электронов образуется протонный потенциал на внутренней мембране митохондрий.В рассмотренной дыхательной цепи конечным акцептором электронов и протонов является кислород. У некоторых микроорганизмов конечным акцептором протонов и электронов выступает нитрат, который восстанавливается до азота или даже до аммиака.
|
|
|
5 комплекс.Синтез АТФ. Общепризнанной теорией синтеза АТФ в ЭТЦ является теория хемиоосмотического сопряжения, выдвинутая П. Митчелом. Сущность ее следующая: процесс окислительного фосфорилирования осуществляется пятым комплексом дыхательной цепи митохондрий — протонной АТФ-синтазой. В процессе транспорта электронов по дыхательной цепи образуется градиент ионов водорода по разные стороны внутренней мембраны митохондрий. Возникший градиент концентрации заставляет протоны проходить через АТФ-синтазу на ту сторону мембраны, где концентрация протонов ниже. На АТФ-синтазе удерживаются АДФ и Фн. Проход протонов через АТФ-синтазу приводит к её конформационным изменениям и соответственно взаимодействию АДФ и Фн. Реакция синтеза такова:
|
|
|
АДФ + Фн → АТФ + H2O
Это наиболее распространенный способ окисления субстрата в клетках, осуществляемый путем дегидрирования. Эффективность этого способа характеризуется высоким коэффициентом полезного действия. Примерно 40% энергии, заключенной в химической связи окисляемых веществ, концентрируется в макроэргических связях АТФ, а остальная энергия рассеивается в виде тепла.
Мембрана, на которой создается электрохимический трансмембранный градиент протонов называется энергизированной. Энергизированная мембрана стремится разрядиться за счет перекачки протонов из межмембранного пространства обратно в матрикс. Этот процесс осуществляется с помощью протонзависимой АТФ-азы.

Синтез АТФ, сопряженный с электронотранспортной цепью
Н+-АТФаза встроена во внутреннюю мембрану митохондрий. Она похожа на гриб и состоит из двух белковых факторов F0 и F1 . Фактор F0 пронизывает всю толщу внутренней мембраны митохондрий. Шаровидная часть, выступающая вматрикс митохондрий, - это фактор F1. Строение, свойства и функции этих белковых факторов совершенно разные.Фактор F0 состоит из трех гидрофобных полипептидных цепей разной структуры. Этот фактор выполняет функцию протонпроводящего канала, по которому протоны водорода попадают к фактору F1.Фактор F1 является водорастворимой частью Н+-АТФазы и представляет собой белковый комплекс, состоящий из девяти субъединиц пяти разных типов. Одна эпимолекула фактора F1 содержит 3 α, 3β и по одной субъединице γ, δ, ε (α, β,γ,δ). Фактор F1 осуществляет синтез АТФ из АДФ и фосфорной кислоты. Центры связывания АДФ и АТФ находятся в субъединицах α и β каждаяиз которых может удерживать по одной молекуле АДФ или АТФ. Согласно данным рентгеноструктурного анализа центры связывания АДФ и АТФ находятся на стыке субъединиц α и β. Субъединица β выполняет каталитическую функцию в синтезе АТФ
|
|
|

Строение протонзависимой АТФазы
Существует несколько концепций, объясняющих механизм образования АТФ при посредстве Н+-АТФазы. Все концепции рассматривают протоны водорода, поступающие по протонпроводящему каналу к фактору F1, в качестве активаторов различных процессов, приводящих к образованию АТФ из АДФ и фосфорной кислоты.Как только атомы водорода или электроны достигают определенного компонента цепи дыхания, из матрикса в межмембранное пространство выбрасывается 2 протона водорода, и на внутренней мембране митохондрий возникает ΔμН+; протоны проходят через протонпроводящий канал и достигают фактора F1 H+-АТФазы, которая катализирует синтез АТФ. Если в цепь дыхания атомы водорода поставляет НАД, то возникают 3 точки сопряжения работы цепи дыхания с синтезом АТФ, т.е. происходит синтез 3 молекул АТФ. Если в цепь дыхания атомы водорода поставляет ФАД, то синтезируются 2 молекулы АТФ.В мышечной клетке существует митохондриальный ретикулум, при помощи которого митохондрии связаны в единую цепь или представляют собой одну гигантскую разветвленную митохондрию.
По ее энергизированной мембране ΔμН+ может передаваться на большие расстояния, обеспечивая в нужном месте синтез необходимого количества АТФ для совершения мышечной работы.
И так, весь комплекс протекающих в митохондриях процессов можно изобразить следующей схемой:

Синтез АТФ из АДФ и фосфорной кислоты за счет энергии, выделяющейся при тканевом дыхании, называется окислительным фосфорилированием.
Процессы окисления и фосфорилирования взаимосвязаны. Их соотношение определяется коэффициентом фосфорилирования Р/О – количество фосфорилированного АДФ в молях на ½ моль кислорода.
Коэффициентом окислительного фосфорилированияназывают отношение количества фосфорной кислоты (Р), использованной на фосфорилирование АДФ, к атому кислорода (О), поглощённого в процессе дыхания.
При окисление молекулы НАДН2 электроны по дыхательной цепи проходят 3 пункта сопряжения, что обеспечивает синтез 3 АТФ при затрате 3 Н3РО4и 3 АДФ на 1 атом кислорода. Соответственно для НАДН2Р/О=3.
При окисление молекулы ФАДН2, электроны по дыхательной цепи проходят только 2 пункта сопряжения, что обеспечивает синтез 2 АТФ при затрате 2 Н3РО4и 2 АДФ на 1 атом кислорода. Соответственно для ФАДН2Р/О=2.
Эти величины Р/О отражают теоретический максимум синтеза АТФ, фактически эта величина меньше из-за затрат на транспорт.
Зависимость интенсивности дыхания митохондрий от концентрации АДФ называют дыхательным контролем. В сутки человек потребляет в среднем 27 моль кислорода. Около 25 моль используется в дыхательной цепи. При среднем значении Р/О=2,5 ежесуточно образуется 125 моль АТФ или 62 кг. В норме субстраты тканевого дыхания и О2находятся в достаточном количестве и не лимитируют окислительное фосфорилирование. Активность окислительного фосфорилирования ограничивает только концентрация АДФ, которая обратно пропорциональна концентрации АТФ.При нагрузке концентрация АТФ снижается, а АДФ увеличивается, что ускоряет дыхание и фосфорилирование. В состоянии покоя количество АТФ увеличивается, а АДФ снижается, что тормозитдыхание и фосфорилирование.
В результате дыхательного контроля скорость синтеза АТФ соответствует потребностям клетки в энергии. Общее содержание АТФ в организме 30—50 г, но каждая молекула АТФ в клетке «живёт» меньше минуты. В сутки у человека синтезируется 40—60 кг АТФ и столько же распадается.
На синтез молекул АТФ расходуется примерно 40-45% всей энергии электронов, переносимых по ЦПЭ, приблизительно 25% тратится на работу по переносу веществ через мембрану. Остальная часть энергии рассеивается в виде теплоты и используется теплокровными животными на поддержание температуры тела.
Повреждение внутренней мембраны митохондрий или увеличение ее проницаемости под действием разобщителей вызывает исчезновение электрохимического потенциала, разобщение процессов окисления и фосфорилирования, и прекращение синтеза АТФ.
Разобщением дыхания и фосфорилированияназывают явление исчезновения на мембране электрохимического потенциала под действием разобщителей и прекращение синтеза АТФ.
Разобщителямиявляются вещества, которые могут переносить протоны (протонофоры) или другие ионы (ионофоры) через мембрану минуя каналы АТФ-синтетазы. В результате разобщения количество АТФ снижается, АДФ увеличивается, возрастает скорость потребления О2, окисления НАДН2, ФАДН2, а образовавшаяся свободная энергия выделяется в виде теплоты.Как правило, разобщители — липофильные вещества, легко проходящие через мембраны. Например, вещество 2,4-динитрофенол (переносит Н+), лекарство - дикумарол, метаболит - билирубин, гормон щитовидной железы - тироксин, антибиотики - валиномицин и грамицидин.
Разобщение окислительного фосфорилирования может быть биологически полезным. Оно позволяет генерировать тепло для поддержания температуры тела у новорождённых, у зимнеспящих животных и у всех млекопитающих в процессе адаптации к холоду. У новорождённых, а также зимнеспящих животных существует особая ткань, специализирующаяся на теплопродукции посредством разобщения дыхания и фосфорилирования - бурый жир. Бурый жир содержит много митохондрий. В мембране митохондрий имеется большой избыток дыхательных ферментов по сравнению с АТФ-синтазой. Около 10% всех белков приходится на так называемый разобщающий белок (РБ-1) - термогенин. Бурый жир имеется у новорождённых, но его практически нет у взрослого человека.
Дата добавления: 2018-02-28; просмотров: 7298; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
