Влияние катализаторов на скорость реакции
Катализ: ускорение реакции за счет введения дополнительного вещества – катализатора (Kt), состояние и масса которого в конце реакции остаются неизменными.
k= koe-Ea/RT c катализатором k растет т.к. Еа снижается. Kt входит в состав нового активированного комплекса, отвечающего меньшей Еа,к после распада которого регенерируются в неизменном виде: А+ В + Kt →[ А…В…Kt]→АВ + Kt
 Энергетическая диаграмма некаталитической (1) и каталитической (2) реакции
Энергетическая диаграмма некаталитической (1) и каталитической (2) реакции
Вывод: Катализатор снижает Еа реакции, что приводит к увеличению доли активных молекул и возрастанию скорости реакции.
Гомогенный катализ: Kt и все реагенты-в одном фазовом состоянии (жидком или газообразном).
Ферментативный катализ -природные реакции, катализируемые ферментами - биологическими катализаторами (превращение крахмала в глюкозу, гидролиз эфиров, расщепление белков, брожение, дегидратация СО2 из крови и др.) В организме человека более 30 тысяч (!) ферментов.
Гетерогенный катализ: Kt и реагенты в разных фазах (твердая газообразная; твердая-жидкая) и реакция идет на поверхности Kt. Гетерогенные катализаторы: металлы, оксиды и соли металлов. Каталитические гетерогенные реакции включают стадии:
подвод реагента,
адсорбцию на Kt,
образование активированного комплекса,
образование продукта и его десорбцию.
Стадии гетерогенного катализа:
А + В +Кt→(А –В –Кt)адс →(А…В …Кt) →(АВ)адс + Кt →АВ + Кt
|
|
|
Пример : CO + ½ O2 → СО2 (Pt –Кt)
идет через: образование активированного комплекса
(СО…О…Pt) → (СО2)адс + Pt → СО2 + Pt Еа ↓ и υ↑
Kt отличаются:
■ активностью Реакция идет только на активных центрах, обеспечивающих оптимальные условия реакции)
■ избирательностью(влияние Kt на скорость определенной реакции):
■ универсальностью(влияние Kt -металлов Pt – группы на скорость очень многих реакций)
Вещества, увеличивающие активность Кt – промоторы. Вещества, снижающие активность Кt – каталитические яды (мышьяк, ртуть, свинец для Pt).
В обратимых каталитических реакциях Кt в равной степени ускоряют и прямую и обратную реакцию, сокращая время достижения равновесия.
Автокатализ – kt - один из продуктов реакции
Для автокаталитических реакций: А→В (В –Kt) Кинетическое уравнение  Пример: FeO + H2 = Fe + H2O Fe - kt
Пример: FeO + H2 = Fe + H2O Fe - kt
Особенности кинетики гетерогенных и обратимых реакций
Гетерогенные реакции идут на поверхности раздела фаз, которая и служит реакционным пространством (поверхностью). Поэтому первой особенностью кинетики этих реакций является влияние площади реакционной поверхности на скорость реакции.С учетом площади поверхности равной S общая скорость гетерогенной реакции первого порядка описывается уравнением:
|
|
|

|
где с – концентрация реагента (газообразного или жидкого).
Единица измерения скорости гетерогенной реакции в этом случае – [моль×с-1], константы скорости реакции– [м×с-1].
Твердое вещество в кинетическое уравнение не входит .
Например, кинетика гетерогенной реакции СаО(к) + СО2 = СаСО3(к)
описывается уравнением: 
| Удельную скорость реакции, отнесенную к единице площади реакционной поверхности, (для реакции первого порядка описывается уравнением: Единица измерения удельной скорости реакции [моль×с-1×м-2]. Скорость гетерогенной химической реакциизависит от скорости подвода реагента и отвода продукта с поверхности раздела фаз (зона химической реакции), что является второй особенностью этих реакций. Скорость обратимых гетерогенных и гоиогенных реакций зависит т скоростей прямой и обратной реакции: А + В = Д + К
Вывод: общая скорость необратимой гетерогенной химической реакции зависит, и удельная скорость реакции не зависит от площади реакционной поверхности. На скорость гетерогенной химической реакции влияют процессы массопереноса. Скорость обратимой реакции определяется разностью скоростей прямой и обратных реакций.
| |||||||
|
 Мы поможем в написании ваших работ! | |||||||

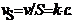 )
) = kпр СА С В – kобр СD СK
= kпр СА С В – kобр СD СK
 или kпр САС В = kобрСDСK или СDСK/ САС В =Kc =kпр/kобр
или kпр САС В = kобрСDСK или СDСK/ САС В =Kc =kпр/kобр