Уравнения, связывающие концентрацию исходных веществ и время
Консультация по теме «Химическая кинетика»
ХИМИЧЕСКАЯ КИНЕТИКА изучает скорость, механизм протекания процесса и факторы, влияющие на скорость.
Скорость реакции - количество вещества, образующееся в единице реакционного объёма (для гомогенной реакции) или на единице поверхности раздела фаз (для гетерогенной реакции) в единицу времени
Гомогенная реакция протекает в гомогенной системе, гетерогенная – на границе раздела фаз.

 моль/(л.с)
моль/(л.с)  моль/ (м2с)
моль/ (м2с)  , моль/л
, моль/л
V– объём реакционной зоны; S-поверхность раздела фаз;
τ-время; ni– количество i – го вещества.
Средняя скорость  (в определенный промежуток времен ) Мгновенная скорость
(в определенный промежуток времен ) Мгновенная скорость  ( в конкретный момент времени).
( в конкретный момент времени).
 для исходных веществ - отрицательно, для продуктов – положительно.
для исходных веществ - отрицательно, для продуктов – положительно.
Кинетические кривые – кривые, отражающая изменение концентрации какого-либо вещества от времени в ходе реакции
А → В С = f (τ)

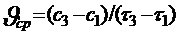
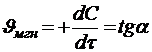
Задача 1.
За 1 с в единице реакционного пространства образуется по трем реакциям 66 г СО2, 68 г Н2S и 51 г NН3. Скорость образования какого из веществ больше?
Решение. Количество вещества (ν) в молях каждого из продуктов реакции
 |
 где R – реакционное пространство, Dν – изменение количества вещества за время Dτ;
где R – реакционное пространство, Dν – изменение количества вещества за время Dτ;
Скорость образования NН3 больше, чем скорости образования Н2S и СО2.
Простые (элементарные) реакции протекают в одну стадию.
Сложные – суммарный результат протекания нескольких простых реакций.
Простые классифицируют по молекулярности. Молекулярность - число молекул, участвующих в элементарном химическом акте:
целое (+) число: 1,2, реже 3
1 – мономолекулярные:I2 ® 2I
2 – бимолекулярные: H2 + I2 ® 2HI
3 – тримолекулярные: 2NO + Cl2 ® 2NOCl
Запись простой реакции отражает механизм ее протекания, сложной– не отражает механизма протекания процесса: 2N2O5 ® O2 + 2N2 O4
Стадияи:
1 N2O5 ® O2 + N2O3 быстро
2 N2O3 ® NO + NO2 медленно
3 2NO2 ® 2N2O4 быстро
медленная стадия (2) – лимитирующая стадия, определяет скорость

Cкорость реакции зависит от:
1) природы реагирующих веществ,
2) концентрации или давления реагирующих веществ,
3) температуры
4) катализатора
Влияние концентрации на скорость реакции
Условия протекания реакции A+B→ K +L:
1 - одновременное нахождение А и В в определённой точке реакционного пространства;
2 - удачное их столкновение.
Вероятность (ω) нахождения молекулы для каждого из веществ прямо пропорциональна его концентрации: ωA = α×CаA, ωB = β×C вB.
Вероятность одновременного нахождения обеих молекул в одной точке пространства, т.е. их столкновения: ω = ωA × ωB = α×Cа A × β×Cв B.
γ – доля удачных столкновений 

Уравнение, связывающее скорость реакции с концентрацией исходных веществ - кинетическое.
Основное кинетическое уравнение 
k - константа скорости:
а) не зависит от концентрации
б) зависит от температуры, природы реагирующих веществ, катализатора, площади поверхности раздела фаз.
k – удельная скорость:  , если СА = СВ = 1моль/л
, если СА = СВ = 1моль/л
а, в – частные порядки реакции по веществам А и В (определяются экспериментально) n = (а + в) – общий порядок реакции
В простых реакциях: n = 1, 2 редко 3 и общий порядок равен молекулярости. H2 + I2 ® 2HI – простая (элементарная) реакция
а(Н2) =1, в(I2) =1 ,т.е. порядки реакции по веществам равны стехиометрическим коэффициентам n = 1+1 =2 Þ
 закон действующих масс для химической кинетики.
закон действующих масс для химической кинетики.
В сложных реакциях: n = 0, целочисленные, дробные, (-),(+) (определяются экспериментально)
Уравнения, связывающие концентрацию исходных веществ и время
(Т = const)
Реакции 1-ого порядка А ® В CH3OCH3® CH4 + H2 + CO
Кинетическое уравнение реакции первого порядка: 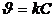 .
.
 , lnC – lnC0 = -kt Þ lnC = lnC0 - kt
, lnC – lnC0 = -kt Þ lnC = lnC0 - kt
С0 – исходная концентрация, С - концентрация в момент времени t



 [ k] =[с-1] Для реакций 1-ого порядка зависимость lgC от t линейная:
[ k] =[с-1] Для реакций 1-ого порядка зависимость lgC от t линейная:
 lgC
lgC
lgCo
t, с
период полупревращения τ1/2:время, за которое прореагировала половина исходного количества вещества
C = 0,5C0 Þ 
 -не зависит от Со для n=1
-не зависит от Со для n=1
Реакции 2-ого порядка A + B → продукты или 2А ® продукты
 если C0A = C0B
если C0A = C0B 


 [л×моль-1×с-1]
[л×моль-1×с-1]
 Для реакции 2-ого порядка зависимость 1/С от t линейная
Для реакции 2-ого порядка зависимость 1/С от t линейная 
C
a tga = k
1/C0
t
Период полупревращения для реакций 2-ого порядка C = ½ C0 
 t ½ - обратно пропорционально начальной С0
t ½ - обратно пропорционально начальной С0
Реакции 0-го – порядка:С = С0 - kt; t1/2 = С0 /2k, [k]= [моль л-1 с-1]
Реакции 3-его порядка:  ;
;  [k]= [моль-2 л2 с-1]
[k]= [моль-2 л2 с-1]
Задача 2.
В реакции второго порядка А + В ® D за 1 час концентрации веществ А и В уменьшились по сравнению с начальной с0 А = с0 В = 0,2 моль/л на 30 %. Определите константу скорости и скорость реакции в начальный момент времени и через час после начала реакции.
Решение. Концентрации веществ А и В за 1 час уменьшились на 0,3×с0 = 0,06моль/л. Отсюда, через час концентрации составят сА = сВ = 0,2 – 0,06 = 0,14(моль/л).
 Для реакции II-го порядка
Для реакции II-го порядка

Отсюда
Задача 3.
Во сколько раз изменится скорость реакции 2СО(г) + О2(г) ® 2СО2(г)
при увеличении давления в системе в 10 раз? Температура системы поддерживается постоянной.
Решение. Предположим, что рассматриваемая реакция является элементарной, т. е. для нее справедлив закон действующих масс: υ = k×с2(СО)×с(О2).
 |
Rонцентрация и парциальное давление связаны прямо пропорциональной зависимостью рi = сi×RT, получим, что υ= k×р2(СО)×р(О2).
После увеличения давления в системе в 10 раз парциальное давление каждого из реагентов реагентов возрастет тоже в 10 раз,
Отсюда υ¢/υ = 1000. Следовательно, скорость реакции увеличится в 1000 раз.
Дата добавления: 2018-02-15; просмотров: 1280; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
