Эпидемиология печеночной недостаточности
Согласно данным из клиник США, обострение хронической печеночной недостаточности регистрируется с частотой 1 случай на 11 тыс. жителей в год [2]. Собственно острая печеночная недостаточность, развивающаяся внезапно без предшествующего хронического заболевания печени, встречается в 10-15 раз реже [1].
Распространенность печеночной энцефалопатии у пациентов с циррозом печени составляет 10-14% в целом при данной патологии, 16-21% у пациентов с декомпенсированным циррозом и 10-50% у пациентов с трансъюгулярным внутрипеченочным портосистемным шунтированием (TIPS) [3].
Асцит встречается более чем у 50% больных с 10-летней историей заболевания печени. В течение первого года от момента появления асцита выживает от 45 до 82% больных, в течение 5 лет – менее 50%. Резистентный асцит встречается в 10% случаев у больных ЦП, выживаемость таких пациентов в течение 1 года не превышает 50%. Спонтанный бактериальный перитонит – самое характерное инфекционное осложнение цирроза печени: по данным литературы, его выявляют у 7–31% больных с асцитом [4].
Гепаторенальный синдром развивается примерно у 15% пациентов в течение 6 мес от момента первой госпитализации по поводу асцита, у 40% – в течение 5 лет [4].
Кровотечение из варикозно расширенных вен (ВРВ) пищевода и желудка у пациентов с циррозом печени формируются у 30% в течение 5 лет, при алкогольном циррозе – в 50% случаев за 2 года. Риск развития повторного кровотечения очень высок и зависит от тяжести цирроза: в первый год рецидив кровотечения наблюдается у 28% пациентов с классом А (по Child-Pugh), у 48% - с классом B, у 68% - с классом C [39].
|
|
|
Гипонатриемия разведения встречается в среднем у трети (30–35%) госпитальных пациентов с ЦП и асцитом [39].
Кодирование по МКБ 10
K70 - Алкогольная болезнь печени
K71 - Токсическое поражение печени
K72 - Печеночная недостаточность, не классифицированная в других рубриках
K73 - Хронический гепатит, не классифицированный в других рубриках
K74 - Фиброз и цирроз печени
K75 - Другие воспалительные болезни печени
K76 - Другие болезни печени
K77 - Поражения печени при болезнях, классифицированных в других рубриках
Классификация
Классификация осложнений, возникающих в послеоперационном периоде у пациентов с сопутствующими заболеваниями печени:
ü печеночная энцефалопатия
ü асцит и спонтанный бактериальный перитонит
ü гепатоторенальный синдром
ü кровотечение из варикозно расширенных вен пищевода
ü дилюционная гипонатриемия
ü печеночная коагулопатия.
Классификация асцита Международного общества по изучению асцита (International Ascetic Club) [4]:
ü 1-я степень – жидкость в брюшной полости определяется только при ультразвуковом исследовании,
|
|
|
ü 2-я степень – проявляется симметричным увеличением живота,
ü 3-я степень – представляет собой напряженный асцит,
ü резистентным асцит называется в том случае, если правильное назначение мочегонных препаратов не приводит к его уменьшению.
Классификация печеночной энцефалопатии [3] :
ü печеночная энцефалопатия в результате острой печеночной недостаточности,
ü портосистемное шунтирование в отсутствие цирроза печени,
ü печеночная энцефалопатия при хронических заболеваниях печени (цирроз печени).
Диагностика
Пациенты с заболеваниями печени предъявляют жалобы на слабость, быструю утомляемость, похудание, зуд кожных покровов при наличии желтухи. Истощение связано с анорексией, неправильным режимом питания и нарушением синтеза белка в тканях.
Анестезиологу следует обратить внимание на желтуху, изменение цвета биологических жидкостей и стула, телеангиоэктазии на коже, злоупотребление алкоголем, наркотиками, фармакологическими препаратами, гепатит, предшествующие гемотрансфузии и анестезии в анамнезе, изменения вкуса и обоняния и т.д.
Рекомендация 1.
Для верификации алкогольной болезни печени и алкогольной зависимости рекомендуется использовать тест AUDIT (тест расстройств от употребления алкоголя) (уровень убедительности рекомендаций I, уровень достоверности доказательств – С) [45].
|
|
|
Комментарии. Тест включает 10 вопросов, которые исследуют потребление (1-3), зависимость (4-6) и проблемы, связанные с алкоголем (7-10) (табл. 1). В анкете AUDIT необходимо суммировать баллы по каждому из 10 вопросов. Об алкогольной зависимости можно говорить, если сумма балов ≥ 8 балов для мужчин в возрасте до 60 лет или ≥ 4 балов для женщин, подростков и мужчин в возрасте старше 60.
Таблица 1.
АУДИТ (AUDIT –Alcohol Use Disorders Identification Test)
| 1. Как часто Вы употребляете напитки, содержащие алкоголь? | ||||||||||||||||
| (0) Никогда | (1) 1 раз в месяц или реже | (2) 2-4 раза в месяц | (3) 2-3 раза в неделю | (4) 4 или более раз в неделю | ||||||||||||
| 2. Сколько стандартных порций алкогольного напитка Вы выпиваете в тот день, когда употребляете алкоголь? | ||||||||||||||||
| (0) 1 или 2 | (1) 3 или 4 | (2) 5 или 6 | (3) От 7 до 9 | (4) 10 или более | ||||||||||||
| 3. Как часто Вы выпиваете 6 или более стандартных порций? | ||||||||||||||||
| (0) Никогда | (1) реже, чем 1 раз в месяц | (2) 1 раз в месяц | (3) 1 раз в неделю | (4) Каждый день или почти каждый день | ||||||||||||
| 4. Как часто за последний год Вы замечали, что, начав пить алкогольные напитки, не можете остановиться?
| ||||||||||||||||
| (0) Никогда | (1) реже, чем 1 раз в месяц | (2) 1 раз в месяц | (3) 1 раз в неделю | (4) Каждый день или почти каждый день | ||||||||||||
| 5. Как часто за последний год из-за чрезмерного употребления алкоголя Вы не смогли сделать то, что делаете обычно? | ||||||||||||||||
| (0) Никогда | (1) реже, чем 1 раз в месяц | (2) 1 раз в месяц | (3) 1 раз в неделю | (4) Каждый день или почти каждый день | ||||||||||||
| 6. Как часто за последний год Вам необходимо было опохмелиться утром, чтобы прийти в себя после того, как Вы много выпили накануне? | ||||||||||||||||
| (0) Никогда | (1) реже, чем 1 раз в месяц | (2) 1 раз в месяц | (3) 1 раз в неделю | (4) Каждый день или почти каждый день | ||||||||||||
| 7. Как часто за последний год Вы испытывали чувство вины или угрызения совести после выпивки? | ||||||||||||||||
| (0) Никогда | (1) реже, чем 1 раз в месяц | (2) 1 раз в месяц | (3) 1 раз в неделю | (4) Каждый день или почти каждый день | ||||||||||||
| 8. Как часто за последний год Вы не могли вспомнить, что было накануне вечером, потому что вы были пьяны? | ||||||||||||||||
| (0) Никогда | (1) реже, чем 1 раз в месяц | (2) 1 раз в месяц | (3) 1 раз в неделю | (4) Каждый день или почти каждый день | ||||||||||||
| 9. Получали ли Вы или кто-то другой травму по причине чрезмерного употребления вами алкогольных напитков? | ||||||||||||||||
| (0) Нет | (2) Да, но не в прошлом году | (4) Да, в прошлом году | ||||||||||||||
| 10. Кто-нибудь из родственников, друг, врач или другой медицинский работник выражали озабоченность по поводу употребления Вами алкоголя или предлагали Вам уменьшить количество употребляемого алкоголя? | ||||||||||||||||
| (0) Нет | (2) Да, но не в прошлом году | (4) Да, в прошлом году | ||||||||||||||
Примечание: Стандартная порция соответствует 10 мл этилового спирта.
При осмотре пациентов с заболеваниями печени на коже верхней части грудной клетки в зоне декольте, на лице, предплечьях и тыльной стороне кистей часто обнаруживаются сосудистые звёздочки (телеангиэктазии, сосудистые паучки, звёздчатые ангиомы). На внутренней поверхности ладоней в области тенара и гипотенара у больных с печеночно-клеточной недостаточностью определяется так называемая пальмарная эритема — интенсивное ярко-красное окрашивание кожных покровов. Островки эритемы могут появляться на подушечках и у основания пальцев. При поднятии рук кверху или надавливании на тенар (гипотенар) эритема бледнеет, но потом её цвет быстро восстанавливается.
При осмотре передней брюшной стенки больных с заболеваниями печени, сопровождающимися развитием внутри- или внепечёночной портальной гипертензией, можно видеть расширенные, извитые коллатеральные вены. При внутрипечёночной портальной гипертензии некоторое количество крови может оттекать из левой ветви воротной вены через околопупочные вены в нижнюю полую вену, что приводит к появлению расходящихся от пупка коллатералей, получивших название «голова Медузы». При внепечёночной портальной гипертензии расширенные вены появляются на боковой стенке живота.
Осмотр больных с холестатическими поражениями печени позволяет выявить потерю эластичности кожи, ее сухость и во многих случаях:
ü следы расчесов на коже рук, ног, живота и грудной клетки;
ü гиперпигментацию кожных покровов;
ü появление ксантом и ксантелазм.
Желтуха главным образом обусловлена неспособностью гепатоцитов метаболизировать билирубин, поэтому она позволяет до некоторой степени оценивать выраженность печеночно-клеточной недостаточности. При острой недостаточности, например, обусловленной вирусным гепатитом, желтуха отражает степень повреждения гепатоцитов. При циррозе эта связь не столь очевидна и желтуха может быть незначительной или отсутствовать вообще. Причиной этого при циррозе является достижение равновесия процессов некроза и регенерации в печени. Появление желтухи свидетельствует об активном печеночно-клеточном заболевании и плохом прогнозе.
Наличие синяков и пурпуры в сочетании с анамнестическими указаниями на кровоточивость дёсен и слизистых у больных с заболеваниями печени являются важным свидетельством развития печеночной коагулопатии.
К диагностическим критериям резистентного асцита [4] относят:
1) длительность лечения: интенсивная терапия мочегонными препаратами (максимальные дозы: антагонисты альдостерона 400 мг/сут, фуросемид 160 мг/сут) в течение 1 нед при соблюдении диеты с содержанием соли до 5,2 г/сут;
2) отсутствие ответа на лечение: снижение массы тела менее 0,8 кг каждые 4 дня;
3) ранний рецидив асцита: возврат асцита 2–3-й степени в течение 4 нед от начала лечения;
4) осложнения, связанные с приемом диуретических препаратов:
портосистемная энцефалопатия, развившаяся в отсутствие других провоцирующих факторов;
почечная недостаточность – повышение концентрации сывороточного креатинина более чем на 100% до уровня >177 мкмоль/л у пациентов, отвечающих на лечение;
гипонатриемия – понижение содержания сывороточного Na более, чем на 10 ммоль/л до уровня менее 125 ммоль/л;
гипокалиемия – снижение уровня сывороточного К менее 3,5 ммоль/л;
гиперкалиемия – повышение уровня сывороточного К более 5,5 ммоль/л.
Клиническая картина асцита может развиваться постепенно в течение нескольких месяцев или появиться внезапно. Чаще всего увеличение в размерах живота служит первым симптомом, который заставляет пациента с асцитом обратиться к врачу. Иногда появляется одышка, что связано с подъемом диафрагмы при выраженном скоплении жидкости в брюшной полости. При объективном осмотре можно обнаружить симптомы, характерные для заболеваний печени, – «печеночные знаки», желтуху, энцефалопатию, гинекомастию, венозные коллатерали на передней брюшной стенке. При перкуссии над местом скопления в брюшной полости свободной жидкости (более 1,5 л) вместо тимпанита определяется тупой звук. При напряженном асците пальпация внутренних органов затруднена, при этом печень и селезенка могут баллотировать.
Клиническая картина СПБ включает разлитую боль в животе различной интенсивности, без четкой локализации; лихорадку и нарастание печеночной энцефалопатии без видимых провоцирующих факторов. У 8–10% пациентов определяется положительный симптом раздражения брюшины. Ригидность брюшных мышц редко встречается при напряженном асците. Лихорадка при СБП отмечается у 50% больных и может быть связана с септическим шоком (сепсисом), нередко температура тела повышается только до субфебрильных цифр. У 10–15% пациентов возникают рвота, диарея, признаки пареза кишечника. У ряда больных заболевание манифестирует признаками септического шока с выраженной гипотензией, тахикардией, олигурией. Вместе с тем у 10–33% больных начальная симптоматика отсутствует, и заболевание выявляют случайно при исследовании асцитической жидкости. Это может быть связано с тем, что обычно у таких больных преобладает клиника печеночной энцефалопатии, что затрудняет анамнестический поиск.
Диагностические критерии гепаторенального синдрома (Рекомендации EASL) [4].
1. Цирроз печени с асцитом.
2. Уровень сывороточного креатинина более 133 мкмоль/л (1,5 мг/дл).
3. Отсутствие нормализации содержания сывороточного креатинина (до <133 мкмоль/л) спустя 2 дня, как минимум, после отмены диуретиков и инфузии альбумина в дозе 1 г/кг, максимально 100 г/сут.
4. Отсутствие шока.
5. Отсутствие текущего или недавнего использования нефротоксических лекарств.
6. Отсутствие паренхиматозных заболеваний почек, проявляющихся протеинурией более 500 мг/сут, микрогематурией до 50 эритроцитов в поле зрения и/или изменением почек по данным УЗИ
Специфических клинических симптомов ГРС нет. Клинические признаки определяются сочетанием острой почечной недостаточности с прогрессирующей печеночной недостаточностью и портальной гипертензией. Характерны жажда, апатия, слабость. У больных увеличивается в объеме живот, снижается артериальное давление, возможно нарастание желтухи. К типичным почечным признакам относятся олигурия, снижение фильтрационной функции почек с умеренным повышением уровня сывороточного креатинина и азота мочевины крови. При этом концентрационная способность почек достаточно сохранна. Протеинурия, изменения в мочевом осадке минимальны и обнаруживаются редко. В терминальной стадии может присоединиться гиперкалиемия, гипохлоремия.
Рекомендация 2.
У пациентов с заболеваниями печени необходим ежедневный скрининг на наличие печеночной энцефалопатии на основе критериев West-Haven (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [3].
Комментарии. Диагностические критерии печеночной энцефалопатии (критерии West-Haven), основанные на физикальном обследовании представлены в таблице 2.
Таблица 2.
Диагностика печеночной энцефалопатии (критерии West-Haven) (рекомендации Европейской ассоциации по исследованию печени, 2014) [3]
| Стадия | Состояние сознания | Интеллектуальный статус, поведение | Неврологический статус |
| Минимальная | Не изменено | Не изменен | Изменения психометрических тестов |
| Стадия I (легкая) | Сонливость, нарушение ритма сна | Снижение внимания, концентрации, забывчивость | Мелкоразмашистый тремор, изменение почерка |
| Стадия II (средняя) | Летаргия или апатия | Дезориентация, неадекватное поведение | Астериксис, атаксия |
| Стадия III (тяжелая) | Сомноленция, дезориентация | Дезориентация, агрессия, глубокая амнезия | Астериксис, повышение рефлексов, спастичность |
| Стадия IV (кома) | Отсутствие сознания и реакции на боль | Отсутствуют | Арефлексия, потеря тонуса |
Рекомендация 3.
Все пациентам с циррозом показана запись ЭКГ для выявления увеличенного интервала QT и других электрофизиологических отклонений. Пациентам с одышкой в покое, а также с низкой толерантностью к физической нагрузке показано выполнение эхокардиографии. Соответственно, в периоперационном периоде препараты, удлиняющие интервал QT (макролиды, амиодарон), должны использоваться с осторожностью (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [41, 42].
Рекомендация 4.
Диагностический парацентез должен быть выполнен всем больным с впервые выявленным асцитом 2 или 3 степени, а также у всех госпитализированных пациентов с утяжелением асцита или любым осложнением цирроза печени (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [4].
Рекомендация 5.
Подсчет числа нейтрофилов и посев культуры асцитической жидкости должны быть выполнены для исключения бактериального перитонита. Для СБП характерно количество нейтрофилов в асцитической жидкости более 250 мм–3 (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [4].
Комментарии. Пациенту с впервые выявленным асцитом при обращении к врачу обязательно проводится исследование АЖ – абдоминальный парацентез. Цель исследования – выявление причины возникновения асцита, поэтому АЖ направляют на биохимический и цитологический анализ. Больным с напряженным асцитом для облегчения их состояния и уменьшения одышки выполняется лечебный объемный парацентез.
Со степенью портальной гипертензии тесно коррелирует СААГ, который рассчитывается по формуле: СААГ = альбумин сыворотки – альбумин АЖ. Значения СААГ 11 г/л и более в 80% случаев свидетельствуют в пользу портальной гипертензии как причины развития асцита.

Культуры АЖ зачастую негативны, положительный ответ не является необходимым для постановки диагноза СБП, посевы важны для управления антибактериальной терапией.
Рекомендация 6.
Гепаторенальный синдром диагностируется при повышении креатинина в сыворотке крови >133 мкмоль/л и при исключении других известных причин почечной недостаточности. Необходим мониторинг уровня сывороточного креатинина для раннего выявления ГРС. Причины почечной недостаточности при циррозе, которые должны быть исключены перед постановкой диагноза ГРС: гиповолемия, шок, паренхиматозные заболевания почек и применение нефротоксичных препаратов (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [4].
Рекомендация 7.
У всех пациентов с заболеваниями печени должен быть оценен риск хирургического вмешательства с помощью систем оценки Child-Turcotte, Child-Turcotte-Pugh, модель конечной стадии заболевания печени MELD (Model of end-stage liver disease) [46], CLIF-C OF, CLIF-C ACLF, CLIF-C AD (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [47, 48].
Комментарии.
Классификация Child - Turcotte . Классификация была первоначально предназначена для оценки шансов на выживаемость после хирургического портосистемного шунтирования, но за последующие годы она также оказалась полезной для пациентов с циррозом печени, и до недавнего времени использовалась для отбора пациентов для трансплантации печени [49]. Оценка по шкале Child - Turcotte основана на трех клинических и двух лабораторных переменных – асцит, неврологические нарушения (энцефалопатия), питание, концентрация сывороточного билирубина, концентрация сывороточного альбумина. По совокупности исследуемых показателей выделяют 3 группы прогноза: А (наилучший), В (средний) и С (худший) (таблица 3).
Таблица 3.
Классификация Child - Turcotte
| Параметры | Группы | ||
| А | В | С | |
| Билирубин, мкмоль/л (мг/дл) | < 34 ( <2,0) | 34-51 (2,0-3,0) | > 51 ( >3,0) |
| Альбумин, г/л | >35 | 30-35 | <30 |
| Асцит | отсутствует | компенсированный медикаментозно | не поддающийся лекарственной терапии |
| Неврологические нарушения | отсутствуют | слабовыраженные | выраженные |
| Питание | хорошее | пониженное | кахексия |
| Операционно-анестезиологический риск | низкий (5%) | умеренный (10%) | высокий (50%) |
Классификация Child - Turcotte – Pugh . Модифицированный вариант к лассификации Child - Turcotte [49] . В зависимости от наличия/отсутствия и уровня каждого из пяти факторов (билирубин, альбумин, протромбиновое время, асцит и стадия энцефалопатии) пациенту начисляется от 1 до 3 баллов (таблица 4). У пациентов с количеством баллов 5-6 по Child - Turcotte - Pugh - достаточно компенсированный цирроз печени и адекватные синтетические функции и, следовательно, они не имеют практически никаких ограничений для проведения операции.
Для пациентов с количеством баллов 7-9 по шкале Child - Turcotte - Pugh риск периоперационных осложнений и летальности выше, любой крупной операции на печени (например, резекции печени) следует избегать. Пациентам с количеством баллов 10-15 с циррозом печени противопоказана любая обширная операция (на любом органе) и они должны быть рассмотрены в качестве кандидатов на трансплантацию печени.
Таблица 4 .
Система оценки Child - Turcotte - Pugh
| Переменные | Баллы | ||
| 1 | 2 | 3 | |
| Стадия энцефалопатии | нет | 1 и 2 | 3 и 4 |
| Асцит | нет | легкий | выраженный |
| Билирубин, мкмоль/л (мг/дл) | < 34 (< 2,0) | 34-51 (2,0-3,0) | > 51 ( >3,0) |
| Альбумин, г/л | >35 | 28- 35 | < 28 |
| Увеличение протром-бинового времени (сек) или МНО | 1-4 ( <1,3) | 4-6 (1,3-1,5) | >6 (>1,5) |
Обе представленные выше классификации взаимосвязаны (таблица 5).
Таблица 5 .
Соотношение классификаций Child - Turcotte и Child - Turcotte - Pugh ' s .
| Общая сумма баллов по Child - Turcotte - Pugh | Класс тяжести цирроза печени по Child - Turcotte | Летальность % |
| 5-6 | А | 5 |
| 7-9 | В | 10 |
| 10-15 | С | 50 |
Модель конечной стадии заболевания печени - MELD (Model of end- stage liver disease). Шкала MELD была разработана как система из клинических и лабораторных показателей [46]. Первоначально она предназначалась для прогнозирования выживаемости после наложения трансъюгулярного внутрипеченочного портосистемного шунта ( TIPS) и прогнозирования возможности кровотечения из варикозно расширенных вен. MELD -оценка также позволяет прогнозировать краткосрочную выживаемость у больных с циррозом печени. Сейчас она используется для отбора больных для трансплантации печени. Показатель MELD рассчитывается с помощью математической формулы, которая включает три переменных пациента - концентрацию креатинина сыворотки крови, сывороточного билирубина и МНО. MELD-оценка очень хорошо коррелирует с прогнозом.
MELD = (9,6 × ln[креатинин, мг/дл]) + (3,8 × ln[билирубин, мг/дл] + (11,2 × ln[МНО]) + 6,4
Примечания. В оригинальной формуле используются единицы измерения, принятые в США. Концентрации билирубина и креатинина менее 1,0 мг/дл округляются до 1,0 мг/дл. Максимально разрешенное содержание креатинина - 4,0 мг/дл. MELD оценивается в диапазоне от 6 до 40 баллов. Если пациенту было проведено за последнюю неделю два и более диализа, то уровень креатинина для расчета автоматически принимается за 4 мг/дл.
Для расчета MELD может быть использован онлайн-калькулятор: http://www.mdcalc.com/meld-score-model-for-end-stage-liver-disease-12-and-older/ Клиническое значение шкалы MELD представлено в табл. 6.
Таблица 6.
Расчет летальности от печеночно-клеточной недостаточности
в течение трех месяцев по MELD
| Индекс MELD | Летальность % | ||
| 40 и более | 71,3 | ||
| 30-39 | 52,6 | ||
| 20-29 | 19,6 | ||
| 10-19 | 6 | ||
| < 9 | 1,9 | ||
| Индекс MELD | Период, мес. | Выживаемость, % | |
| 10 баллов | 3 | 74 | |
| 6 | 66 | ||
| 12 | 59 | ||
| 20 баллов | 3 | 52 | |
| 6 | 40 | ||
| 12 | 30 | ||
| 30 баллов | 3 | 11 | |
| 6 | 5 | ||
| 12 | 2 | ||
Шкалы системы CLIF-SOFA [47, 48]. В качестве модели для диагностики ОХПечН была выбрана шкала последовательной оценки органной недостаточности ( Sequential Organ Failure Assessment , SOFA ), т. к. она широко применяется у пациентов, которым требуется интенсивная терапия. Поскольку компоненты шкалы SOFA (печень, почки, головной мозг, дыхание, кровообращение, свертывание) не включают специфические признаки цирроза, ее несколько модифицировали, специализировав для пациентов с поражением печени. Новая шкала получила название CLIF-SOFA. Позже на ее основе была разработана упрощенная шкала CLIF-C OF с такими же критериями органной недостаточности и прогнозом (таблица 7).
Таблица 7.
Шкала CLIF- C OF для диагностики ОХПечН
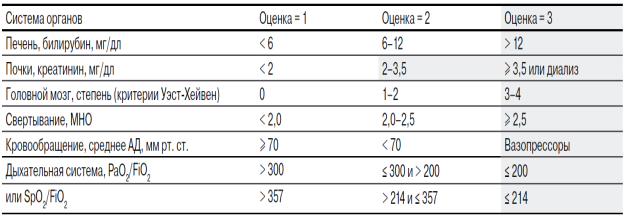
В дальнейшем появились еще две прогностических шкалы: одна для пациентов с ОХПечН (оценка CLIF-C ACLF), другая - для пациентов с острой декомпенсацией цирроза без ОХПечН (оценка CLIF-C AD), которые улучшили точность прогноза с помощью оценок CLIF-C OF и CLIF-SOFA, а также MELD, MELD-натрий и Чайлда-Пью [48]. Шкала CLIF-C ACLF учитывает показатели CLIF-C OF, возраст и число лейкоцитов. Шкала CLIF-C AD - возраст, число лейкоцитов, сывороточный уровень натрия, сывороточный уровень креатинина и МНО. Переменные всех этих шкал объединяют, получая оценочную систему с диапазоном значений от 0 до 100 баллов. Расчет по шкалам системы CLIF можно вести используя онлайн- калькулятор Е uropean foundation for the study of chronic liver failure ( http :// www . efclif . com / scientific - activity / score - calculators / clif - c - aclf ).
Эти три шкалы могут быть собраны в алгоритм, который удобно использовать для определения прогноза у госпитализируемых пациентов с циррозом [48]. Шкала CLIF-C OF применяется у лиц, срочно госпитализированных с осложнениями цирроза - энцефалопатией, кровотечением, инфекцией, асцитом. Если, судя по оценке, у пациента имеет место ОХПечН, то его прогноз можно предположить по оценке CLIF-C ACLF, которую определяют ежедневно. Эту же шкалу можно использовать для проверки эффективности лечения в течение 3–7 дней. С другой стороны, если у пациента нет ОХПечН, применяют шкалу CLIF-C AD. У пациентов с CLIF-C AD > 60 баллов высок риск развития ОХПечН под действием различных инициирующих факторов.
Валидация шкал CLIF-С OF , CLIF - C ACLF и CLIF - C ADпоказала их более высокую точность в прогнозировании смертности у пациентов с ОХПечН по сравнению со шкалами MELD , MELD -натрий и Чайлд-Пью [50].
Противопоказания к плановой хирургии у пациентов с заболеваниями печени [51]:
1. Острый вирусный гепатит.
2. Острый алкогольный гепатит.
3. Острая печеночная недостаточность.
4. Острая почечная недостаточность.
5. Тяжелая коагулопатия.
6. Гипоксимия.
7. Кардиомиопатия.
Показания к трансплантации печени [51].
Критерии King’ s College
1. ОПчН вследствие передозировки парацетамола
· pH артериальной крови < 7,3 после восполнения ОЦК и позднее первых суток после приема парацетамола
• Лактат > 3 ммоль/л или 3 следующих критерия:
o тяжесть энцефалопатии выше III степени
o креатинин сыворотки > 300 мкмоль/л
o МНО > 6,5
2. ОПчН непарацетамоловой этиологии
• МНО > 6,5 или 3 из 5 следующих критериев:
o гепатит неясной или лекарственной этиологии
o возраст < 10 или > 40 лет
o промежуток времени от появления желтухи до манифестации энцефалопатии > 7 дней
o билирубин > 300 мкмоль/л
o МНО > 3,5
Критерии Клиши (больниц Beaujon и Paul Brousse)
• Спутанность сознания или кома (печеночная энцефалопатия 3-й или 4-й стадии)
• Уровень фактора V < 20 % нормы у больных моложе 30 лет или
• Уровень фактора V < 30 % нормы у больных старше 30 лет
Лечение
Рекомендация 8.
При выборе анестезиологического пособия необходимо учитывать сниженный клиренс ряда препаратов у пациентов с сопутствующими заболеваниями печени (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [52-67].
Комментарии.
Ингаляционные анестетики. Влияние ингаляционных анестетиков на печеночный кровоток носит комплексный характер и зависит не только от свойств препаратов, но и от тяжести заболевания печени, возраста, характера оперативного вмешательства. Тем не менее, применение севофлюрана, изофлюрана и десфлюрана возможно у пациентов с хроническими заболеваниями печени, от применения галотана и энфлюрана следует в этом случае отказаться. Вопрос о безопасности применения ксенона у больных с патологией печени пока требует дальнейших клинических исследований.
Регионарная анестезия. Как спинальная, так и эпидуральная анестезия могут безопасно использоваться у пациентов с заболеваниями печени, при этом, воздействие на функцию печени менее выражено, чем при общей анестезии.
Наркотические анальгетики.У больных с заболеванием печени метаболизм морфина может значительно замедляться, что увеличивает риск развития неблагоприятных эффектов препарата – избыточной седации и депрессии дыхания [52]. Хотя внепеченочные пути выведения морфина могут быть эффективными у больных с печеночной недостаточностью, интервалы его введения должны быть увеличены в 1,5-2 раза, а в случае приема внутрь доза должна быть уменьшена в связи с повышенной биодоступностью. Подобные рекомендации распространяются и на промедол, период полувыведения которого также увеличивается в 2 раза.
Фентанил имеет высокий объем распределения из-за его хорошей растворимости в липидах, поэтому фармакокинетика препарата мало изменяется у пациентов с циррозом печени, но при тяжелых заболеваниях печени его доза должна быть снижена [53]. Связано это с тем, что фентанил практически полностью метаболизируется печенью, поэтому, как при методике повторяющихся болюсов, так и при длительной инфузии возможна кумуляция его эффекта [52]. Фармакокинетика суфентанила аналогична таковой для фентанила, при этом она практически не нарушена при однократной инъекции препарата. В отличие от фентанила и суфентанила, период полувыведения альфентанила практически вдвое выше у больных с печеночной недостаточностью, что может значительно увеличить время его действия [54]. Ремифентанил – препарат, быстро подвергающийся гидролизу ферментами крови, поэтому его фармакодинамика не меняется у пациентов с печеночной дисфункцией, независимо от дозы, методики и продолжительности введения. Все это делает его препаратом выбора у пациентов с тяжелой печеночной недостаточностью [55, 56].
Седативные препараты/гипнотики.Метаболизм тиопентала характеризуется низким отношением печеночной экстракции (т.е. клиренс зависит от емкости ферментных систем печени), что потенциально может приводить к пролонгации его действия, однако практически период его полувыведения у больных циррозом печени меняется незначительно, что связано с большим объемом распределения [57, 58]. У других внутривенных анестетиков, включая кетамин и пропофол, отношение печеночной экстракции высокое (то есть клиренс зависит в большей степени от уровня печеночного кровотока), что также потенциально может снизить их клиренс при патологии печени [59]. Фармакокинетика пропофола также изменяется незначительно у больных циррозом печени, как при болюсном введении, так и при длительной инфузии, однако клинически время восстановления после анестезии может быть увеличено [60].
Сниженный клиренс мидазолама при заболеваниях печени приводит к увеличению периода его полувыведения. В связи с уменьшением связывания с белками и увеличением свободной фракции препарата, у пациентов с тяжелыми заболеваниями печени следует ожидать более длительную продолжительность действия и усиление седативного эффекта, особенно после повторных доз или длительной инфузии. Аналогичные изменения наблюдаются при применении всех бензодиазепинов [61].
Дексомедетомидин, как препарат практически полностью метаболизирующийся в печени, при применении у больных с тяжелой ее патологией может иметь более длительный период полувыведения [62]. В этом случае необходимо с осторожностью подходить к выбору дозировки, чтобы избежать избыточной седации.
Несмотря на значительные изменения в метаболизме препаратов при печеночной недостаточности, наличие такой патологии, как цирроз печени, мало влияет на эффект большинства внутривенных анестетиков и гипнотиков. Тем не менее, в условиях печеночной недостаточности следует с осторожностью применять повторные дозы и длительную инфузию бензодиазепинов ввиду риска усиления седативного эффекта и увеличения его длительности. Пропофол, вероятно, является препаратом выбора у пациентов с печеночной дисфункцией, а для поддержания печеночного кровотока необходим адекватный контроль системного артериального давления.
Миорелаксанты.Векуроний – стероидный миорелаксант, который элиминируется в печени, в связи с чем его клиренс у больных с печеночной недостаточностью может быть снижен, а длительность действия увеличена. Хронический алкоголизм и индукция печеночных ферментов не влияют на фармакодинамику препарата [24].
Рокурониум, также стероидный миорелаксант со сходным метаболизмом; при однократном его введении у больных печеночной недостаточностью длительность клинического эффекта не увеличивается. Однако увеличение начальной дозы или повторные введения могут пролонгировать его эффект [63].
Более безопасно могут применяться миорелаксанты с орган-независимымми путями элиминации – атракуриум (неспецифический гидролиз) и цисатракуриум (хофмановская элиминация). Период полувыведения и длительность действия данных препаратов не меняется при наличии патологии печени [64]. Тем не менее, в процессе их метаболизма образуется побочный продукт – лауданозин, который элиминируется печенью. У больных с печеночной недостаточностью он может кумулировать, что несет в себе потенциальный нейротоксический эффект, который, однако, не был подтвержден клинически [65].
Мивакуриум должен с осторожностью применяться у больных с печеночной недостаточностью ввиду увеличения длительности его действия из-за снижения холинэстеразо-зависимого клиренса его активных изомеров. Доза препарата должна подбираться с осторожностью [66].
Снижение активности холинэстеразы также влияет и на фармакодинамику сукцинилхолина, что выражается в удлинении его клинического эффекта [67].
Печеночная недостаточность снижает элиминацию векурониума, рокурониума и мивакуриума, что увеличивает длительность их действия, особенно после повторных введений или длительной инфузии. Применение суггамадекса для реверсии нейромышечного блока, вызванного рокурониумом, является эффективным у больных с заболеваниями печени, но без исходного изменения печеночных тестов. Вопрос о применении суггамадекса при значительной печеночной недостаточности остается открытым. Эффект атракуриума и цисатракуриума не зависит от функции печени, поэтому они могут быть препаратами выбора у данной категории пациентов.
Стабильная центральная гемодинамика и адекватная оксигенация более важны во время оперативного вмешательства и анестезиологического пособия, чем возможные гепатотоксические эффекты анестетиков и адъювантов.
Рекомендация 9.
Для лечения ПЭ рекомендуется использовать препараты, уменьшающие образование аммиака в кишечнике (лактулоза 30,0-120,0 г/сутки); антибиотики (рифаксимин 1200 мг/сутки или ципрофлоксицин 500 мг/сутки) в течение 5-7 дней, препараты, усиливающие обезвреживание аммиака в печени (L-орнитин-L-аспартат(Гепа-мерц) при отсутствии почечной дисфункции) (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [3].
Комментарии. L-орнитин-L-аспартат выпускается как в виде раствора для внутривенной инфузии, так и в форме гранул для перорального приема. Стандартная схема применения предусматривает внутривенное капельное введение по 20–30 г препарата в течение 7–14 дней с последующим переходом на пероральный прием 9–18 г/сут. Для достижения более быстрого и стойкого результата возможно сочетание внутривенного и перорального способов применения. Комбинированная терапия гепа-мерцем и лактулозой способствует элиминации аммиака как из кишечника, так и из крови, что обусловливает суммацию лечебных эффектов.
Рекомендация 10.
Необходимо соблюдать меры по контролю и предотвращению отека головного мозга при ОПечН(уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [3].
Комментарии. К мерам по контролю и предотвращению отека головного мозга относится:
- коррекция метаболических нарушений;
- контроль уровня электролитов ( Na, K, CI), лактата, аммиака;
- избегать гиперинфузии и гипергидратации, контроль водного баланса, стремление к нормоволемии;
- интубация трахеи и ИВЛ показаны у пациентов с гипоксемией, а также при прогрессировании энцефалопатии (III/IV степень) с целью контроля СО2 и защиты дыхательных путей;
- контроль внутричерепного давления (перед установкой датчика ВЧД – коррекция коагулопатии), его коррекция, в случае необходимости, маннитолом;
- контроль уровня глюкозы;
- гемодинамический мониторинг, избегать колебаний артериального давления;
- поднять головной конец кровати на 15–30 ° ;
- использование седации, чтобы избежать неадекватных реакций пациента;
- экстренный гемодиализ для коррекции уровня аммиака, натрия.
Рекомендация 11.
Лечебная тактика у пациентов сосредним или умеренным асцитом - ограничение приема натрия (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [4], назначение диуретиков (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [4].
Рекомендация 12.
Лечебная тактика у пациентов с большим или напряженным асцитом - ограничение приема натрия (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [4], назначение диуретиков (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [4], проведение лапароцентеза с последующим применением коллоидных растворов, альбумина - при удалении больших объемов АЖ (8 г альбумина на каждый удаленный литр) (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [4].
Рекомендация 13.
Показания к отмене диуретиков (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [4]:
- сывороточный натрий < 120 ммоль/л;
- прогрессирующая почечная недостаточность;
- углубление ПЭ.
Рекомендация 14.
Показание к отмене фуросемида - сывороточный калий < 3 ммоль/л; показание к отмене верошпирона - сывороточный калий > 6 ммоль/л. (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [4].
Рекомендация 15.
Способы лечения цирроза печени с рефрактерным асцитом (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [4]:
• повторный большой парацентез - наиболее распространенная терапия;
• портосистемное шунтирование (TIPS) - установка внутрипеченочного стента между печеночной и воротной веной.
Комментарии. Основной недостаток повторных парацентезов - ранний рецидив асцита (пациенты нуждаются в парацентезе каждые 2-4 нед).
TIPS эффективно в лечении рефрактерных асцитов, но связано с высоким риском развития печеночной энцефалопатии. TIPS должно рассматриваться у пациентов, требующих очень частого парацентеза, или в тех случаях, когда парацентез неэффективен (например, из-за наличия ограниченного асцита). Разрешение асцита после TIPS происходит медленно и у большинства пациентов требуется продолжение приема диуретиков и ограничения соли.
TIPS не может быть рекомендовано у больных с тяжелой печеночной недостаточностью (сывороточный билирубин >5 мг/дл, МНО >2 или баллы по MELD >11, печеночная энцефалопатия 2 степени или хроническая печеночная энцефалопатия), сопутствующей активной инфекцией, прогрессирующей почечной недостаточностью или тяжелой легочно-сердечной недостаточностью.
Рекомендация 16.
Нестероидные противовоспалительные препараты (НПВП) противопоказаны пациентам с асцитом из-за высокого риска развития дальнейшей задержки натрия, гипонатриемии и почечной недостаточности (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [4].
Рекомендация 17.
Препараты, снижающие АД или почечный кровоток, такие как ингибиторы АПФ, антагонисты ангиотензина II, или блокаторы α1-адренергических рецепторов не должны использоваться у пациентов с асцитом в связи с повышенным риском почечной недостаточности (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [4].Рекомендация 18.
У пациентов с асцитом без почечной недостаточности использование рентгеновского контраста следует применять с осторожностью и использовать общие меры профилактики почечного повреждения (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [4].Рекомендация 19.
Эмпирическое назначение антибиотиков должно быть начато сразу после диагностики СБП. Антибиотиками первой линии являются цефалоспорины третьего поколения. Альтернативные варианты включают амоксициллин/клавулановая кислота и хинолоны, такие как ципрофлоксацин или офлоксацин. Антибиотикотерапия продолжается до разрешения СБП, которое подтверждается снижением количества нейтрофилов в асцитической жидкости <250 мм–3 и ее стерильностью (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [4].
Рекомендация 20.
Терлипрессин (1 мг/4-6 ч внутривенно струйно) в сочетании с альбумином следует считать первой линией терапевтического воздействия для пациентов с ГРС (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [4].
Комментарии. Целью терапии является улучшение функции почек в достаточной степени для снижения креатинина сыворотки крови менее 133 мкмоль/л (1,5 мг/дл). Если креатинин сыворотки не уменьшается как минимум на 25% после 3 дней терапии, дозу терлипрессина необходимо поэтапно увеличивать до максимума 2 мг/4 ч. У пациентов с частичным ответом (креатинин сыворотки не уменьшается <133 мкмоль/л) или у пациентов без снижения сывороточного креатинина лечение должно быть прекращено в течение 14 дней.
Альтернативная терлипрессину терапия включает норэпинефрин или октреотид в сочетании с альбумином, но имеющаяся информация весьма ограничена в отношении использования этих препаратов у пациентов с ГРС 1 типа.
Рекомендация 21.
При подозрении на кровотечение из ВРВ должны быть назначены вазоактивные препараты как можно раньше, препаратом выбора является терлипрессин (уровень убедительности рекомендаций I, уровень достоверности доказательств – А) [68].
Комментарии. К вазоактивным препаратам, рекомендуемым для лечения кровотечения из ВРВ относятся соматостатин и терлипрессин.
Соматостатин вызывает селективную вазоконстрикцию внутренних органов, обусловленную подавлением активности эндогенных вазодилятаторов (в частности, глюкагона) и секреции соляной кислоты. Портальное давление снижается на 20-25%. Препарат вводится первоначально болюсно в дозе 50-100 мкг, затем переходят на длительную внутривенную инфузию в дозе 25-50 мкг/час в течение 5-7 дней.
Терлипрессин уменьшает артериальный приток в портальную систему, снижая портальное давление на 30-40%. По данным проведенных исследований, из всех вазоактивных препаратов, терлипрессин является препаратом выбора для лечения острого кровотечения, из ВРВ [68], его назначение приводит к снижению на 34 % риска смертельного исхода.
Рекомендация 22.
Тяжелая дилюционная гипонатриемия требует коррекции – внутривенного введения раствора натрия хлорида или проведения экстренного диализа (уровень убедительности рекомендаций I, уровень достоверности доказательств – В) [40, 41].
Комментарии. Первый шаг в лечении дилюционной гипонатриемии – ограничение ведения жидкости и отмена диуретических препаратов. Ограничение объема жидкости до 1 л в день предотвращает дальнейшее падение уровня натрия, но не приводит к его повышению. В дополнение к ограничению потребляемой жидкости больные должны соблюдать бессолевую диету. В этих условиях назначение гипертонических солевых растворов нецелесообразно из-за их низкой эффективности, дополнительного увеличения объема внеклеточной жидкости и возможного усугубления отеков и асцита.
Доза изотонического раствора натрия хлорида рассчитывается следующим образом: необходимое количество Na, ммоль = (искомый уровень Na – реальный уровень Na) × масса тела, кг × 0,6, где 0,6 – коэффициент. Так как в 1 л 0,9% раствора NaCl содержится 154 ммоль Na, пациенту в сочетании с коллоидами (альбумином) необходимо ввести количество раствора 0,9% NaCl = необходимое количество Na/154 ммоль Na.
Дата добавления: 2021-06-02; просмотров: 61; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
