Расчет материального баланса процесса сорбционного концентрирования урана из продуктивных растворов
Теоретическая часть. Современным вариантом получения ХКПУ является сорбционный метод с использованием органических ионообменных материалов.
Уран в сернокислых растворах после подземного выщелачивания может находиться в виде катиона уранила, недиссоциированной молекулы уранилсульфата и в виде сульфатных комплексных анионов, соотношение между которыми зависит от концентрации сульфат-ионов и иона уранила в соответствии с реакциями:
UO22+ + SO42- ↔ UO2SO4 , K1 = 50
UO2 2+ + 2SO42- ↔ [UO2(SO4)2 ] 2-, K2 = 350
UO2 2+ + 3SO42- ↔ [UO2(SO4)3 ] 4-, K2 = 2500
Можно считать, что в растворе существует подвижное равновесие:
UO22+ + SO42- ↔ UO2SO4 + SO42- ↔ [UO2(SO4)2 ] 2- + SO42- ↔ [UO2(SO4)3] 4-
Следовательно, для извлечения урана мы можем применить в качестве сорбентов катиониты, которые будут извлекать катион уранила, и аниониты, которые будут извлекать сульфатные анионные комплексы, главным образом, [UO2(SO4)3] 4-.
Однако, так как кислотность продуктивного раствора находится в пределах рН < 1, то уран почти полностью присутствует в виде комплексного аниона [UO2(SO4)3] 4-. В этом случае сорбция урана на анионите идет следующим образом:
4(R4N)Cl + [UO2(SO4)3] 4- = (R4N)4[UO2(SO4)3] + 4Cl-
Наиболее вероятный механизм «сорбции» урана можно представить следующим образом: вначале происходит переход смолы от хлоридной или нитратной формы в сульфатную форму, а затем к ней присоединяются молекула уранилсульфата или ионы уранила и сульфата:
|
|
|

Если сложить эти реакции, то получим:

То есть, сорбент концентрирует уран в виде трисульфатного комплекса.
Процесс сорбции заключается в следующем. Осветленные продуктивные растворы насосами подаются на сорбционное концентрирование урана в нижнюю часть напорных сорбционных колонн СНК-3М. Колонны работают в автономном режиме, движение растворов осуществляется снизу вверх противотоком по отношению к движению ионообменной смолы.
Маточники сорбции (МС) с содержанием урана до 3 мг/л выводятся из верхней части колонн СНК-3М через дренажные кассеты и направляются на контрольное сито для улавливания проскочившего через дренаж сорбента. Далее маточники сорбции собираются в пескоотстойнике выщелачивающих растворов (ВР). Уловленный сорбент через буферную колонну возвращается в процесс.
Возвратные растворы (ВР) из пескоотстойника ВР насосами подаются в технологические узлы закисления (ТУЗ), где доукрепляются поступающей со склада серной кислотой до кислотности 5-7 г/л, после чего подаются в закачные скважины.
Насыщенный сорбент выгружают из колонны и направляют на регенерацию («десорбцию»). Регенерация смолы производится путем вытеснения анионных комплексов ионами Cl− или NO3- при повышении их концентрации. В качестве вымывающих растворов используют 1М NaCl, подкисленный 0,1М НС1, или 1М NH4NO3, подкисленный 0,1М HNO3 или 0,15М H2SO4 .
|
|
|
Пример задачи. Производительность сорбционного отделения цеха по переработке продуктивных растворов составляет 3000 т/год. Произвести расчет и составить материальный баланс процесса сорбционного концентрирования урана из продуктивных растворов при следующих исходных данных:
- время работы предприятия (количество рабочих дней в году) – 365 дней;
- коэффициент использования рабочего времени – 0,93;
- количество смен в сутки – 2;
- продолжительность смены – 12 часов.
- концентрация урана в ПР, поступающем на сорбцию 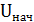 = 0,16 кг/м3;
= 0,16 кг/м3;
- остаточная концентрация урана в возвратном растворе  = 0,003 кг/м3.
= 0,003 кг/м3.
- остаточная емкость смолы 1 кг/м3;
- степень извлечения урана в анионит 98,5%;
- плотность ПР 1,01 кг/м3.
Процесс сорбционного концентрирования осуществляется в сорбционно-напорных колоннах (СНК-3М), работающих в режиме противотока сорбент-раствор. В качестве ионобменной смолы используется Ambersep 920UCl- (SO4)2-. Рабочая емкость смолы 0,55 кг/кг.
Решение:
1. Определяем часовую производительность цеха по урану:
|
|
|
а) Часовая продолжительность работы предприятия
365 × 0,93 × 2 × 12 = 8147 ч/год.
б) Тогда часовая производительность по урану
Qчас = 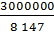 = 369 (кг/ч).
= 369 (кг/ч).
2. Определяем часовой объем раствора м3/ч
Vчас= 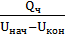 , (5.1)
, (5.1)
где Vчас – часовой объем раствора (м3/ч);
Qчас – часовая производительность по урану (кг/ч);
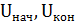 – начальная и конечная концентрация урана в продуктивном и возвратном растворах (кг/м3);
– начальная и конечная концентрация урана в продуктивном и возвратном растворах (кг/м3);
Qчас = 369 кг/ч; 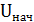 = 0,16 кг/м3;
= 0,16 кг/м3;  = 0,003 кг/м3.
= 0,003 кг/м3.
Vчас= 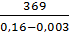 = 2350(м3/час).
= 2350(м3/час).
Расход продуктивного раствора – 2350 м3/час или 20586000 м3/год, следовательно, производительность по урану – 369 кг/час или 3232440 кг/год.
Определим суточное количество исходного раствора ПР, плотность которого 1,01 г/м3:
Vсут = 2350· 24 = 56400 (м3/сут),
mсут= 56400· 1,01 = 56964 (кг/сут).
Количество урана в продуктивном растворе
56400·0,16 = 9024 (кг).
Так как извлечение урана в анионит 98,5 %, то количество извлекаемого урана составит
9024· 0,985 = 8888,64 (кг).
Поскольку рабочая емкость смолы Ambersep 920UCl- (SO4)2- – 0,55 кг/кг, то смолы для сорбции потребуется:
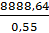 = 16161,16 (кг).
= 16161,16 (кг).
В растворе после сорбции остается урана
9024 – 8888,64 = 135,36 (кг).
Количество анионита с сорбированным ураном составит:
|
|
|
16161,16 + 8888,64 = 25049,8 (кг).
Количество маточников сорбции
56964 – 8888,64 = 48075,36 (кг).
На основе проведенных расчетов составляем материальный баланс процесса сорбции – таблица.
Таблица – Материальный баланс процесса сорбционного извлечения урана из продуктивного раствора
| Приход | Расход | ||||
| Наименование | количество, кг/сут | Наимено-вание
| количество, кг/сут | ||
| всего | в т.ч. урана | всего | в т.ч. урана | ||
| 1. Продуктивный раствор | 56964 | 9024 | 1. Насыщен-ный анионит Ambersep 920U Cl-(SO4)2- | 25049,8 | 8888,64 |
| 2.Сильно-основной анионит Ambersep 920UCl- (SO4)2- | 16161,16 | 2. Маточник сорбции | 48075,36 | 135,36 | |
| Итого | 73125,16 | 9024 | Итого | 73125,16 | 9024 |
Таким образом, суточное количество сорбируемого урана составляет 9024 кг, а в год – 3293760 кг.
Практическое занятие №4.
Дата добавления: 2021-04-05; просмотров: 711; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
