Содержание контрольной работы
Контрольная работа содержит задачи по темам, отражающим содержание разделов: флотационные реагенты [1, 3]; технология флотационного процесса [1, 2, 3, 4]; практика флотации [1, 3];
В контрольной работе выполняется расчёт по исходным данным, согласно варианту. Вопросы, рассматриваемые в контрольной работе, изучаются студентами самостоятельно. На установочной лекции выдается задание. Изучение вопросов и выполнение работы производится в течение семестра, в котором изучается эта дисциплина и сдается перед сессией преподавателю с регистрацией в деканате заочного отделения, в соответствии с принципами заочного обучения.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Введение
Флотация – способ разделения минералов, при которых одни минералы – гидрофобные закрепляются на межфазовой поверхности, а другие – гидрофильные такой способностью не обладают. Во флотации межфазовой границей, к которой прикрепляются минералы, обычно являются: вода-воздух, масло-вода, вода-газ. Природную гидрофобность или гидрофильность можно усилить или ослабить с помощью реагентов.
Универсальность метода заключается в том, что при помощи реагентов можно менять состояние поверхности частиц, т. е. усиливать или уменьшать гидрофильность или гидрофобность поверхности, гидрофобизировать гидрофильную поверхность или гидрофилизировать гидрофобную.
Флотационному методу обогащения подвергаются частицы, как правило, имеющие размеры менее 0,5 мм, т. е. шламы.
|
|
|
Существует большое разнообразие флотационных процессов: пенная флотация, плёночная, масляная флотация, масляная грануляция и др. Пленочной флотацией называется процесс, при котором гидрофобные частицы, попадая на поверхность движущегося потока воды, остаются на ней, образуя пленку, а гидрофильные частицы тонут. Пленочная флотация используется в процессе флотогравитации при доводке гравитационных концентратов. Масляной флотацией называется процесс, при котором гидрофобные частицы прилипают к каплям масла в пульпе и всплывают наверх, а гидрофильные частицы остаются взвешенными в пульпе. Разделение минеральных частиц может осуществляться также при помощи гидрофобной твердой поверхности (флотация твердой стенкой) или твердой поверхности, покрытой слоем гидрофобной вязкой жидкости (обогащение на жировой поверхности). К таким поверхностям, помещенным в пульпу, избирательно прилипают гидрофобные частицы. Флотация на жировой поверхности используется при обогащении алмазов. В промышленности широко применяется пенная флотация. Известны разновидности пенной флотации: флотация кипячением, химическая флотация (например, если порода содержит кальцит, то добавляя серную кислоту можно флотировать гидрофобные частицы на образующихся пузырьках углекислого газа), вакуумная флотация, флотация под давлением, электрофлотация (получение пузырьков электролизом воды) и другие виды. Традиционно на преобладающем большинстве обогатительных фабрик применяется пенная флотация минералов на пузырьках воздуха.Пенной флотацией называется процесс, при котором гидрофобные частицы прилипают к вводимым в пульпу пузырькам воздуха или газа и поднимаются с ними вверх, образуя пену. Гидрофильные частицы остаются в пульпе во взвешенном состоянии. [1; 2 стр.5-13; 5 стр. 8-17, 27-33, 46-48; 6 стр.7-10].
|
|
|
Вопросы для самопроверки
1. В чем заключается процесс флотации?
2. Чем отличаются гидрофобные минералы от гидрофильных?
3. Какие классы крупности частиц руды подвергаются обогащению флотационными методами?
4. Расскажите, какие вы знаете типы флотационных процессов?
5. Что представляет собой пенная флотация минералов на пузырьках воздуха?
6. В чем заключается актуальность применения флотационных методов обогащения, например, для полиметаллических, тонковкрапленных руд, угольных шламов и т. д.?
Теоретические основы флотационного процесса
|
|
|
Существовало много различных гипотез элементарного акта флотации. Первая заключалась в том, что кислород воздуха обладает избирательной адсорбцией при закреплении сульфидов на пузырьках воздуха. Это явление объясняли сродством кислорода воздуха с серой. Оказалось это не так, т. к. сульфиды прикрепляются так же и к пузырькам инертного газа. Второй гипотезой было, то, что частицы и пузырек закрепляются при флотации за счет электростатических сил. Считалось, что гидрофобные частицы и пузырёк воздуха имеют разные заряды поверхности и прикрепляются друг к другу под действием кулоновских сил. Но когда измерили потенциал поверхности пузырька и сульфидных минералов, выяснили, что в основном заряд поверхности имеет отрицательный знак, как у пузырька, так и у гидрофобных частиц, поэтому кулоновские силы скорее мешают прикрепляться частицам к поверхности пузырька, чем помогают. Третья гипотеза – гипотеза смачивания. Оказалось, что причина прикрепления гидрофобной частицы и пузырька за
| θ |
| жидкая фаза |
| твердая фаза |
| газ |
|
|
|
Линия соприкосновения трёх фаз называется периметром смачивания. Смачиваемость характеризуется величиной краевого угла смачивания поверхности – θ. Это угол, образованный поверхностью раздела двух фаз с поверхностью третьей фазы. Краевой угол принято измерять со стороны жидкой фазы.
θ – равновесный угол смачивания на идеально гладкой поверхности. В реальной жизни его искажает явление, которое называется гистерезисом смачивания. Гистерезис смачивания – задержка восстановления равновесного значения краевого угла. Тормозящее действие гистерезиса смачивания можно сравнить с трением, также препятствующим достижению истинного равновесия. Гистерезисная сила всегда направлена в сторону противоположную направлению относительного движения. При закреплении частицы на поверхности раздела вода – воздух площадь контакта начинает увеличиваться (наступление газообразной фазы на жидкую). Сила гистерезиса будет противодействовать этому процессу. При попытке отрыва уменьшается площадь, ограниченная периметром смачивания (наступление жидкой фазы на газообразную). Сила гистерезиса будет препятствовать уменьшению площади, а, следовательно, отрыву пузырька от частицы. Здесь, гистерезис играет положительную роль, способствуя устойчивости флотационного комплекса.
Частица удерживается на пузырьке флотационной силой

которая определяется силой поверхностного натяжения жидкость-газ –  , краевым углом смачивания
, краевым углом смачивания  и периметром смачивания –
и периметром смачивания –  Чем гидрофобнее поверхность частицы, тем больше краевой угол, а значит больше флотационная сила, тем прочнее удерживается частица на поверхности раздела фаз.
Чем гидрофобнее поверхность частицы, тем больше краевой угол, а значит больше флотационная сила, тем прочнее удерживается частица на поверхности раздела фаз.
Необходимо изучить характеристику раздела фаз, участвующих в элементарном акте флотации; роль двойного электрического и гидратных слоев на границе раздела фаз в избирательном закреплении минералов к пузырьку; изменение энергии прослоя воды между пузырьком и частицей при элементарном акте флотации; явления «сухой» и «мокрой» флотации. Ознакомится с понятием «угол формы» и влиянием формы частиц на флотируемость, проанализировать уравнение Фрумкина – Кабанова, как условие флотационного равновесия. [1; 2 стр. 14-26, 29-30,37-43, 48-51; 3; 6 стр. 15-20].
Вопросы для самопроверки
1. Какие гипотезы элементарного акта флотации существовали в истории развития флотации?
2. В чем заключается гипотеза смачивания?
3. Дайте определение краевому углу смачивания.
4. Со стороны какой из фаз принято измерять краевой угол?
5. Что такое гистерезисная сила?
6. Какую роль играет гистерезис при отрыве частицы от пузырька и при закреплении ее?
7. Что представляет собой флотационная сила, и от каких физических величин она зависит?
8. В чем заключается роль двойного электрического и гидратных слоев на границе раздела фаз при закреплении минералов к пузырьку?
9. Как изменяется энергия прослоя воды между пузырьком и частицей при элементарном акте флотации.
10. Объясните понятия «сухая» и «мокрая» флотации.
11. Что такое угол формы, и какое значение имеет при флотации?
12. Напишите условие флотационного равновесия.
Флотационные реагенты
В этой главе необходимо уделить внимание следующим вопросам. Ознакомиться с назначением и классификацией флотационных реагентов. Особое внимание уделить реагентам-собирателям: изучить их классификацию, строение молекул, механизмы действия сульфгидрильных и оксигидрильных собирателей, катионных, аполярных собирателей. Ознакомится с классификацией, строением молекул и механизмами действия реагентов модификаторов поверхности: депрессоров, активаторов, регуляторов среды. Особое внимание уделить механизмам действия таких важных реагентов-депрессоров как цианиды. Ознакомиться с рядом Каковского. Изучить классификацию, строение молекул, механизмы действия реагентов пенообразователей, а, также свойства флотационных пен.
Большинство реагентов работают в ионной форме (диссоциированные на ионы). Чтобы закрепиться на поверхности минерала, они должны образовывать с ионами поверхности трудно растворимые соединения. Следовательно, для того, чтобы уменьшить расход реагентов, необходимо повысить растворимость собирателя подбором типа и расхода регулятора среды. Подбор собирателей производить, ориентируясь на произведение растворимости соединения, которое образуется при химической реакции собирателя с ионами поверхности минерала.
Из класса оксигидрильных собирателей наиболее важными являются карбоновые кислоты и их мыла (соли). Карбоновые (жирные) кислоты – слабые, следовательно, подвергаются гидролизу, в кислых и слабокислых средах. Продукты гидролиза не обладают флотационной активностью, поэтому только в щелочных пульпах можно получить высокую концентрацию анионов кислоты. В кислых пульпах основное количество этих реагентов находиться в нерастворенном виде. Собирающие способности жирных кислот зависят от строения углеводородной цепи. При небольшом количестве углерода в цепи собирающие способности реагента меньше, а при больших количествах углерода выше. Разветвление цепи приводит к уменьшению собирающей способности карбоновых кислот. Олеиновая кислота – наиболее яркий представитель жирных кислот, замерзает при +14 Со. Следовательно, при низких температурах, флотационная активность резко падает. Для повышения активности жирных кислот при низких температурах пульпы применяют, например, органические растворители (керосин, спирт), эмульгаторы (алкилсульфаты, сульфонол) или подогревают пульпу. Собиратели – жирные кислоты используют для флотации окисленных минералов, таких как барит, шеелит, церуссит, англезит и др.
Из класса собирателей очень важными являются сульфгидрильные собиратели. Наиболее яркие представители этого класса – ксантогенаты. Ксантогенаты применяются для флотации полиметаллических руд (сульфидных) руд цветных металлов. Флотируемость сульфидных металлов ксантогенатами, зависит от их растворимости. Лучше флотируются те сульфиды, с металлами которых ион ксантогената образует менее растворимую соль. Флотируемость сульфида возрастает от сфалерита до галенита далее к ковеллину (табл. 1).
Таблица 1
Увеличение флотируемости сульфидов металлов в зависимости от растворимости ксантогенатов соответствующих металлов, образующих пленку собирателя на поверхности сульфидов
| Этиловые ксантогенаты | Произведение растворимости. |
| Bi(C2H5OCS2)3 | 10-39 |
| Hg (C2H5OCS2)2 | 2,5*10-30 |
| Fe (C2H5OCS2)3 | 10-21 |
| Cu C2H5OCS2 | 3,5*1020 |
| Ag C2H5OCS2 | 4,4*10-19 |
| Pb (C2H5OCS2)2 | 1,7*10-17 |
| Zn (C2H5OCS2)2 | 4,9*10-9 |
| Fe (C2H5OCS2)2 | 8*10-8 |
По стрелке: флотируемость сульфидов металлов возрастает, т. к. растворимость ксантогенатов металлов на поверхности сульфидов падает
Собирательные свойства ксантогенатов также усиливаются при увеличении длины углеводородного радикала (табл. 2).
Чем длиннее углеводородная цепь, тем эффективнее флотация, но хуже растворимость. Из ксантогенатов наиболее часто применяют ксантогенаты калия. Они более устойчивые при хранении. На практике используются в виде 10% раствора (чем выше концентрация, тем он устойчивей). Ксантогенаты калия – соли относительно слабой кислоты и сильного основания, следовательно, они подвергаются гидролизу. Продукты гидролиза не обладают собирательными свойствами, поэтому флотацию ксантогенатами необходимо вести в щелочной среде. Ксантогенаты особенно неустойчивы в кислых средах. Скорость действия очень велика до 1 минуты, поэтому для взаимодействия ксантогената с минеральными частицами не нужны контактные чаны. Расход реагентов от 30 до 100 г/т.
Таблица 2
Влияние длины и строения углеводородной цепи на величину краевого угла при насыщенном слое ксантогената на минерале
| Ксантогенат | Радикал | Строение углеводородной цепи | θ (краевой угол) |
| без собирателя | - | - | 0 |
| метиловый | CH3 | Открытая не разветвленная | 50 |
| этиловый | C2H5 | Открытая не разветвленная | 60 |
| пропиловый | C3H7 | Открытая не разветвленная | 68 |
| бутиловый | C4H9 | Открытая не разветвленная | 74 |
| изобутиловый | C4H9 | Открытая разветвленная | 78 |
| изомиловый | C5H11 | Открытая разветвленная | 86 |
| крезиловый | CH3C6H4 | замкнутая | 72 |
| циклогексиловый | C6H11 | замкнутая | 75 |
Стрелка указывает направление повышение флотируемости минералов при применении соответствующих ксантогенатов.
Механизм действия ксантогенатов хемосорбционный. По гипотезе Шведова замещение иона сульфида 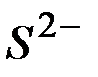 на ион ксантогената, например, на галените невозможно, т. к. произведение растворимости галенита
на ион ксантогената, например, на галените невозможно, т. к. произведение растворимости галенита

а произведение растворимости, например, этилового ксантогената свинца,

т. е. ксантогенаты свинца гораздо более растворимые соединения, и поэтому ион  не может замещаться на ион ксантогената
не может замещаться на ион ксантогената  , ввиду не протекания реакции обмена между этими соединениями. Согласно гипотезе Шведова, на поверхности сульфида, образуются сульфидоокисленные соединения, которые прочно связаны с кристаллической решёткой сульфидов. Именно кислородосодержащие анионы
, ввиду не протекания реакции обмена между этими соединениями. Согласно гипотезе Шведова, на поверхности сульфида, образуются сульфидоокисленные соединения, которые прочно связаны с кристаллической решёткой сульфидов. Именно кислородосодержащие анионы  вытесняются ксантогенатами, с образованием менее растворимых соединений. Однако чрезмерное окисление сульфидов вредно, т. к. при этом ионы ксантогената расходуются на весь окисленный слой, это приводит к большому расходу ксантогенатов.
вытесняются ксантогенатами, с образованием менее растворимых соединений. Однако чрезмерное окисление сульфидов вредно, т. к. при этом ионы ксантогената расходуются на весь окисленный слой, это приводит к большому расходу ксантогенатов.
Следовательно, небольшое окисление сульфидов необходимо для флотации ксантогенатами, чрезмерное окисление приводит к большому расходу собирателя, так как он при этом тратится на химическую реакцию с плёнкой окисленного соединения. Взаимодействие сульфгидрильных собирателей с сульфидоокисленным слоем представляет собой обменную хемосорбционную реакцию с образованием менее растворимого соединения.
Сильноокисленные минералы обрабатывают сульфидами щелочных металлов или щелочноземельных, например, сульфидом натрия или кальция, тогда часть сульфатных ионов замещается сульфидными, что приводит к меньшему расходу собирателя.
Собиратели типа ксантогенатов или олеатов на поверхности минерала распределяются неравномерно, образуя островные покрытия. Экспериментально установлено, что для флотации минералов ксантогенатами достаточно покрыть поверхность минерала на 15-20 % от условного монослоя. Превышение более, чем на 30-40% не увеличивает гидрофобность поверхности, а при больших концентрациях как ксантогенатов так и других анионных коллекторов (жирных кислот и их солей, например, олеатов), происходит обратное явление – гидрофилизация поверхности – перемасливание, что приводит к ухудшению флотации минералов.
Реагенты аэрофлоты также относятся к сульфгидрильным собирателям. Это производные дитиофосфорной кислоты. Соли дитиофосфорной кислоты – сухие аэрофлоты. Они слабее ксантогенатов, как собиратели, но устойчивы к кислой среде (не окисляются кислородом). Используются для флотации цветных металлов, особенно меди. Расход 50-150 г/т.
Катионные собиратели – органические производные аммиака (амины). Имеют свойства слабых оснований, следовательно, в кислой среде их растворимость увеличивается. Если в радикале 6-8 углеродов, то амины нерастворимы в воде и поэтому используют их соли. Катионные собиратели легко флотируют кварц, полевые, шпаты, слюды карбонаты, фосфаты, сульфиды.
Неионогенные собиратели — основные реагенты при флотации природно гидрофобных минералов (уголь, графит, сера, молибденит и др.). В качестве дополнительных собирателей их применяют при флотации самых разнообразных минералов (вводят в дополнение к ионогенным собирателям). В качестве собирателя для флотации угольных шламов лучше всего подходит керосин. Промышленные испытания показывают преимущества дробного способа подачи реагента и подачи его в виде эмульсии (табл. 3).
Таблица 3
Результаты исследования влияния подачи керосина
в эмульсионном виде на флотацию угольных шламов
| Продукты флотации | Без эмульгирования | В виде эмульсий | ||
| Выход % | Зольность % | Выход % | Зольность % | |
| 1 | 15,3 | 6,18 | 23,1 | 5,6 |
| 2 | 12 | 6,03 | 23,6 | 5,7 |
| 3 | 21,4 | 6,83 | 21,6 | 7,02 |
| 4 | 17,2 | 6,78 | 14,4 | 8,49 |
| 5 | 20,6 | 10,5 | 6,7 | 11,3 |
| 6 | 24,6 | 12,5 | 2,8 | 16,5 |
| Итого | 88,6 | 7,85 | 89,6 | 7,1 |
Из таблицы можно сделать вывод, что подача реагента в виде эмульсий существенно улучшает показатели. [1, 2 стр. 19; 57-68, 77, 115-142, 145-159; 170-173; 6].
Вопросы для самопроверки
1. Опишите механизм действия ионогенных реагентов.
2. Что представляют собой оксигидрильные собиратели? Каковы условия их работы.
3. Что представляют собой сульфгидрильные собиратели? В какой среде они активно действуют?
4. Опишите механизм действия ксантогенатов по гипотезе Шведова.
5. Что такое перемасливание? Объясните это явление.
6. Что представляют собой реагенты аэрофлоты? В какой среде они активно действуют?
7. Катионные собиратели. В какой среде они активно работают? Какие минералы можно флотировать с их применением?
8. Аполярный собиратель. В чем заключается его особенность? Опишите механизм действия. Какие минералы флотируют с его применением?
Дата добавления: 2020-12-22; просмотров: 190; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
