Пентагональная пирамида с координационным числом 6
(валентные углы L – M – L равны 720 и 900 ). Пероксокомплекс хрома (VI)
[Cr(L)O(O22-)2] L - gbhblby
Геометрия комплексов с КЧ 7 отвечает пентагональной бипирамиде (валентные углы L – M – L равны 720 , 900 и 1800 ).( sp3d3 -гибридизация): [ZrF7]3-, [UF7]2-.
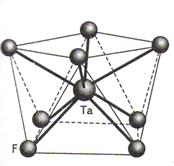
КЧ 7 может иметь и тригональная призма: [ТаF7]2-.(см.ниже).
Если координационное число принимает большее значение, например, КЧ 8 , то при условии, что ребра одинаковы, а угол между ними 900 , комплекс может иметь форму куба;
или конфигурация комплекса сильно усложняется. (см.ниже).
ПРОСТРАНСТВЕННАЯ ИНТЕРПРЕТАЦИЯ КООРДИНАЦИОННЫХ ЧИСЕЛ
Известно много методов определения пространственного строения соединений во всех агрегатных состояниях, в частности:
· Дифракционные (рентгено-, электронно-, нейтронография)
· Спектральные (спектры поглощения в разных диапазонах частот, от γ – ядерного до микроволнового; спектры оптического вращения и кругового дихроизма; магниторезонансные спектры в широком диапазоне частот)
· Магнитные
· Теоретического анализа (квантово – механические расчеты)
1. к.ч. 2
наиболее характерные для элементов подгруппы меди в степени окисления 1.
Геометрические конфигурации:
· линейная ( Валентный угол между L —ц.а.—L составляет 1800
|
|
|
· угловая
Например, [Сu(tu)2]Cl, [Ag(NH3)2]Cl, K[Au(CN)2] (tu – тиомочевина)
2. Соединения с к.ч. 3 немного.
Геометрические конфигурации:
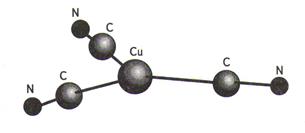
· треугольная (чаще всего)
Например, [Cu(CN)3]– ;
Nd{N[Si(CH3)3]2}3;
[(CH3)3S][HgJ3] (и катион, и анион имеют треугольную конфигурацию)
· тригональная пирамида
[AgL3]Cl; [CuL3]SO4 (L – этилентиомочевина)
3. Соединения с к.ч. 4 довольно распространенные.
Геометрические конфигурации:
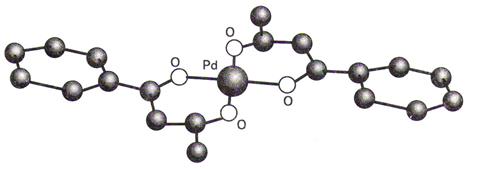
· квадрат (соединения Cu2+, Ni2+, Au3+, Pt2+, Pd2+ и др.)
Например, [AuCl3(SCl2)]; [PdCl2(py)2]; BrF4–; JCl4–;
[Pd{C6H5C(O)CHC(O)CH3}2]
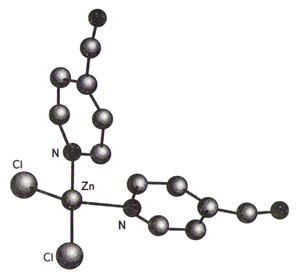
· тетраэдр
Например, Na2[Co(NCS)4];
Ni(CO)4
[ZnCl2(4-CN-py)2]
(NH4)2CuCl3 – содержат бесконечные цепочки их тетраэдров [CuCl4]
4. Раньше к.ч. 5 необычным и малораспространенным, но исследования последних десятилетий дают основания утверждать, что к.ч. 5 так же распространено как и к.ч. 4 и 6.
Геометрические конфигурации:
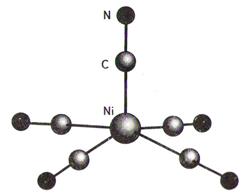
· тетрагональная пирамида
Например, [Ni(CN)5]3– в координационном соединении [Cr(en)3][Ni(CN)5]
\
[CuCl(bpy)L]∙H2O

· тригональная бипирамида
Например, [CuCl5]3– в координационном соединении [Cr(NH3)6][ CuCl5]
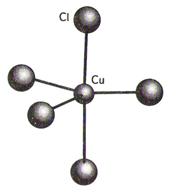
[SbLPh4], где L – ONC(CN)C(O)NH2–

5. Соединения с к.ч. 6 изучены, возможно, лучше других координационных соединений.
Их образуют большинство металлов Периодической системи, особенно кобальт(ІІІ), кобальт(ІІ), платина(ІV), иридий(ІІІ), родий(ІІІ), хром(ІІІ), ванадий(ІІІ), никель(ІІ), медь(ІІ), цинк(ІІ), кадмий(ІІ), марганец(ІІ), лантаноиды(ІІІ).
|
|
|
Геометрические конфигурации:
· Чаще всего реализуется в виде тетрагональной бипирамиды, часто очень вытянутой вдоль оси Z.
Например, [AuCl2(en)2]Cl, [Cu(SCN)2(NH3)4], [Cu(SCN)2(en)2]. [CoS2O3(NH3)5]+ (тетрагонально искривленный октаэдр)

· Если все расстояния центральный атом – донорный атом(лиганд) одинаковые, тетрагональная бипирамида «превращается» в октаэдр. Но эта правильная геометрическая фигура из-за взаимного влияния координированных групп реализуется нечасто.
Например, [Co(H2O)6]2+ и [Ni(H2O)6]2+
· Тригональная призма
Например, [Mo(S2C6H4)3]
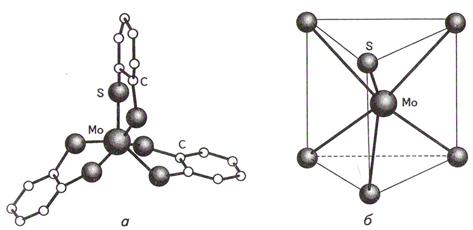
Тиолатные соединения вольфрама, молибдена, рения.
6. Соединений с к.ч. 7 меньше. Они наиболее характерны для таких металлов, как цирконий, гафний, ниобий, тантал, уран, лантаноиды.
Геометрические конфигурации:
· Тригональная призма
Например, [MoBr(t-BuNC)6]Br
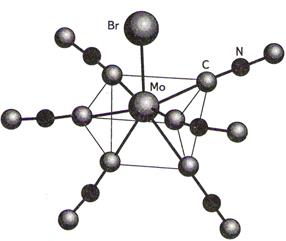
NbF72–, TaF72–, Rb2PuF7.
· Пентагональная бипирамида
Например, [ErL7](ClO4)3
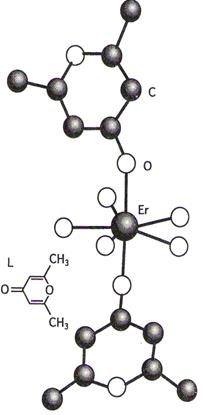
UO2(NCS)53–, UF73–, ZrF73–, K4V(CN)7∙H2O
·
·
·
·
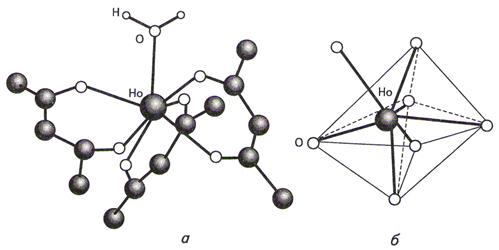
· Тетрагональная бипирамида
Например, [NbOF6]3–, [Ho(PhCOCHCOPh)3(H2O)]
7. к.ч. 8 оказывается
– в цианидах молибдена и вольфрама типа M4[E(CN)8] и M3[E(CN)8], где M – M(I),
– в некоторых комплексах лантаноидов [La(H2O)8]3+, [Ln(C2O4)4]5–,
|
|
|
– в соединениях урана (IV) [U(H2O)8]4+, K4[U(C2O4)4],
– в ацетилацетонатах циркония и гафния [E(acac)4].
Геометрические конфигурации:
· Куб {[La(bpyO2)4](ClO4)3}

·
·
· Додекаэдр Zr(C2O4)44–, [Bu4N]3[Mo(CN)8]

· Квадратная антипризма ReF82–, Zr(acac)4, Na3[TaF8]
· Гексагональная бипирамида Ba[NbO2(CH3COO)3]∙2H2O
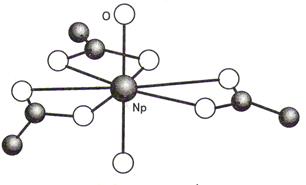
8. к.ч. 9 более характерна для лантаноидов
Например, [Nd(H2O)9](BrO3)3, [Nd(H2O)9](C2H5SO4)3, фториды циркония и гафния [EF9]5–, фториды ниобия и тантала [EF9]4–.
Геометрическая конфигурация:
· Трёхшапочная трёхгранная призма [Yb(H2O)9](CF3SO3)3.

9. Последнее время синтезировано немало координационных соединений, в которых центральный атом определяет
– к.ч. 10
Например, [Gd(NO3)3(phen)2], Li2[Sm(NO3)5∙4H2O, Cs2[Ce(ClO4)5].
– к.ч. 12
Например, Cs3[Ce(ClO4)6].
Дата добавления: 2020-11-29; просмотров: 263; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
