Почему при изменении давления смещается равновесие системы
N2 + ЗН2 = 2NH3
и не смещается равновесие системы N2 + О2 = 2NO? Напишите выражения для констант равновесия каждой из данных систем.
95. Исходные концентрации NO и Сl2, в гомогенной системе
2NO + Cl2 = 2NOCl
составляют соответственно 0,5 и 0,2  . Вычислите константу равновесия, если к моменту наступления равновесия прореагировало 20% NO.
. Вычислите константу равновесия, если к моменту наступления равновесия прореагировало 20% NO.
96. Реакция идет по уравнению N2 + O2 = 2NO. Концентрации исходных веществ до начала реакции были: [N2] = 0,049  ; [О2] = 0,01
; [О2] = 0,01  . Вычислите концентрацию этих веществ в момент, когда [NO] стала равной 0,005
. Вычислите концентрацию этих веществ в момент, когда [NO] стала равной 0,005  .
.
97. Реакция идет по уравнению N2 + 3H2 = 2NH3. Концентрации участвующих в ней веществ были: [N2] = 0,80  ; [Н2] = 1,5
; [Н2] = 1,5  ; [NH3] = 0,10
; [NH3] = 0,10  . Вычислите концентрацию водорода и аммиака, когда [N2] стала равной 0,50
. Вычислите концентрацию водорода и аммиака, когда [N2] стала равной 0,50  .
.
98. Реакция идет по уравнению Н2 + I2 = 2HI. Константа скорости этой реакции при 508°С равна 0,16. Исходные концентрации реагирующих веществ были: [Н2] = 0,04  ; [I2] = 0,05
; [I2] = 0,05  . Вычислите начальную скорость реакции и скорость ее, когда [Н2] стала равной 0,03
. Вычислите начальную скорость реакции и скорость ее, когда [Н2] стала равной 0,03  .
.
99. Вычислите, во сколько раз уменьшится скорость реакции, протекающей в газовой фазе, если понизить температуру от 120 до 80°С. Температурный коэффициент скорости реакции равен трем.
100. Как изменится скорость реакции, протекающей в газовой фазе, при повышении температуры на 60 град, если температурный коэффициент скорости данной реакции равен двум?
101. Как изменится скорость реакции, протекающей в газовой фазе, при понижении температуры на 30 град, если температурный коэффициент скорости данной реакции равен трем?
102. Напишите выражение для константы равновесия гомогенной системы 2SO2 + О2 = 2SО3. Как изменится скорость прямой реакции – образования серного ангидрида, если увеличить концентрацию SO2 в три раза?
Растворы и другие дисперсные системы.
Концентрации растворов
Пример 1. В водном растворе хлорида бария объемом 0,800 л с плотностью 1,20  содержится BaCl2 массой 192 г. Вычислите массовую долю и молярную концентрацию.
содержится BaCl2 массой 192 г. Вычислите массовую долю и молярную концентрацию.
Решение. а) Массовая доля (w), выраженная в процентах, показывает, сколько граммов растворенного вещества содержится в 100 г раствора.
 = 0,2 или 20%,
= 0,2 или 20%,
где m – масса ВаСl2;
mp – масса раствора, г (mp = V·ρ = 800·1,2 = 960 г);
V – объем раствора, мл (0,8 л = 800 мл);
ρ – плотность раствора,  .
.
б) Молярная концентрация показывает число молей растворенного вещества в 1 л раствора и выражается в  . Массу ВаСl2 в 1 л раствора находят из соотношения
. Массу ВаСl2 в 1 л раствора находят из соотношения
в 800 мл раствора содержится 192 г ВаСl2
в 1000 мл раствора содержится x г ВаСl2
 = 240 г BaCl2
= 240 г BaCl2
Молярная масса ВаСl2 равна (М(ВаСl2) = 137 + (35,5·2)) = 208  , следовательно, число молей ВаСl2, содержащихся в 1 л раствора, равно
, следовательно, число молей ВаСl2, содержащихся в 1 л раствора, равно
 = 1,15 моль.
= 1,15 моль.
Молярная концентрация
 = 1,15
= 1,15  .
.
Пример 2. Какой объем раствора (1) KOH с массовой долей ω1 = 34,9% (ρ1 = 1,34 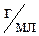 ) следует взять для приготовления раствора (2) объемом V2 = 250 мл с ω2 = 11,0% (ρ2 = 1,1
) следует взять для приготовления раствора (2) объемом V2 = 250 мл с ω2 = 11,0% (ρ2 = 1,1 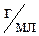 ). Чему равна молярная концентрация С2 , полученного раствора?
). Чему равна молярная концентрация С2 , полученного раствора?
Решение. К решению нужно подойти, исходя из неизменности в исходном и полученном растворах: 1) массы КОН, г; 2) количества КОН, моль. Более рационален второй подход.
Количество КОН

где m – масса КОН;
М – молярная масса КОН.
Учитывая, что m = V2·ρ2·ω2, получаем
 = 0,539 моль.
= 0,539 моль.
Молярная концентрация
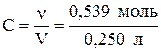 = 2,16
= 2,16 
(обратите внимание на соответствие размерностей величин).
Для исходного раствора
 ,
,
Отсюда объем исходного раствора равен
 = 64,7 мл.
= 64,7 мл.
Задания
103. Вычислите молярную концентрацию раствора хлорида натрия (ρ = 1,148  ) с массовой долей NaCl – 20%.
) с массовой долей NaCl – 20%.
104. Какой объем раствора хлороводородной кислоты (ρ = 1,100  ) с массовой долей НСl 20,01% требуется для приготовления 1 л раствора (ρ = 1,050
) с массовой долей НСl 20,01% требуется для приготовления 1 л раствора (ρ = 1,050  ) с массовой долей 10,17%?
) с массовой долей 10,17%?
105. Смешали 10 мл раствора азотной кислоты (ρ = 1,056  ) с массовой долей HNO3 10% и 100 мл раствора той же кислоты (ρ = 1,184
) с массовой долей HNO3 10% и 100 мл раствора той же кислоты (ρ = 1,184  ) с массовой долей (%) HNO3 в полученном растворе.
) с массовой долей (%) HNO3 в полученном растворе.
106-110. Водный раствор содержит массу m вещества А в объеме V. Плотность раствора ρ. Вычислите массовую долю (в %), молярную долю, молярную концентрацию, молярную концентрацию эквивалентов.
| Номер задачи | A | m, г | V, л | ρ, 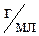
|
| 106 | H2SO4 | 784 | 1,0 | 1,44 |
| 107 | Н3РO4 | 735 | 2,5 | 1,15 |
| 108 | KOH | 718 | 2,0 | 1,27 |
| 109 | HNO3 | 1250 | 3,0 | 1,21 |
| 110 | НСl | 112 | 0,5 | 1,10 |
111-115. Какой объем раствора вещества A с массовой долей ω1, (плотность ρ1) следует взять для приготовления объема V2 раствора с массовой долей ω2 (плотность ρ2)? Чему равна молярная концентрация полученного раствора?
| Номер задачи | А | ω1 , % | ρ1, 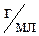
| V2, л | ω2, % | ρ2, 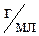
|
| 111 | HNO3 | 27,0 | 1,160 | 1,00 | 20,0 | 1,115 |
| 112 | Na2CO3 | 15,2 | 1,160 | 2,50 | 4,50 | 1,045 |
| 113 | NH3 | 26,0 | 0,904 | 2,00 | 5,25 | 0,976 |
| 114 | NaOH | 40,0 | 1,430 | 5,00 | 10,00 | 1,110 |
| 115 | H2S04 | 95,1 | 1,834 | 10,00 | 4,00 | 1,025 |
116-120. К раствору вещества А объемом Vl с молярной концентрацией c1 добавили воду объемом  . Плотность полученного раствора ρ2. Чему равны молярная концентрация полученного раствора c2 и массовая доля ω2?
. Плотность полученного раствора ρ2. Чему равны молярная концентрация полученного раствора c2 и массовая доля ω2?
| Номер задачи | А | V1, мл | c1, 
|  , мл , мл
| ρ2, 
|
| 116 | Н3Р04 | 10,0 | 2,00 | 50,0 | 1,015 |
| 117 | HCI | 25,0 | 11,00 | 100,0 | 1,035 |
| 118 | Н2S04 | 5,0 | 6,40 | 50,0 | 1,035 |
| 119 | KOH | 50,0 | 9,95 | 1000 | 1,020 |
| 120 | HCIO4 | 20,0 | 3,45 | 100,0 | 1,030 |
Электрохимические процессы
Дата добавления: 2019-11-25; просмотров: 203; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
