При их совместном присутствии
Определение содержания NaОН и Na2CO3 в их смеси проводят путем титрования раствора соляной кислотой.
При титровании наблюдаются две точки эквивалентности: первая, когда полностью нейтрализован NaОН и «наполовину» Na2CO3 и вторая, когда нейтрализуется NaНCO3. В этот момент наступает полная нейтрализация смеси NaОН и Na2CO3.
NaОН + Na2CO3 + 2HCl ® 2NaCl + NaHCO3 (фенолфталеин)
NaHCO3 + HCl ® NaCl + H2O + CO2 (метиловый оранжевый)
Реактивы
Кислота хлористоводородная, НСl 0,1н раствор;
Индикаторы: фенолфталеин, метиловый оранжевый.
Ход определения
Полученный в препараторской в мерной колбе исследуемый раствор доводят до метки дистиллированной водой и тщательно перемешивают. В коническую колбу для титрования переносят аликвотную часть раствора, добавляют 2-3 капли фенолфталеина и титруют 0,1 н раствором соляной кислоты до обесцвечивания. Записывают объем раствора соляной кислоты пошедший на титрование Vф. В ту же колбу добавляют 2-3 капли метилового оранжевого и продолжают титрование до перехода окраски от желтой до красно-оранжевой. Записывают объем раствора соляной кислоты пошедший на титрование Vмо. Повторяют опыт не менее 3 раз, определяют средние арифметические значения 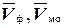 , после чего переходят к расчету.
, после чего переходят к расчету.
Расчетная часть
Содержание карбоната натрия и гидроксида натрия определяют по формулам:
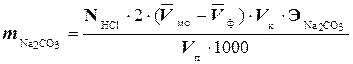
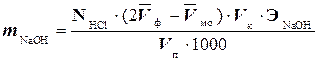
где NHCl - нормальность раствора соляной кислоты;
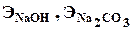 - эквивалентные массы гидроксида натрия и карбоната натрия;
- эквивалентные массы гидроксида натрия и карбоната натрия;
|
|
|
Vк и Vп - объемы соответственно мерной колбы и мерной пипетки, мл.
Лабораторная работа № 3
Перманганатометрия
Перманганатометрическое титрование или перманганатометрия, ‑ метод количественного определения веществ (восстановителей, реже ‑ окислителей и соединений, не обладающих окислительно-восстановительными свойствами) с применением титранта ‑ раствора перманганата калия КMnO4.
Основным веществом, применяемым в качестве стандартного раствора окислителя, является KMnO4. Обычно титрование стандартным раствором перманганата калия проводят в кислой среде.
Так как реакции окисления-восстановления, совершаемые в присутствии KMnO4, протекают с измеримой скоростью, то во избежании образования промежуточных форм окисления ионов марганца, титрование раствором перманганата рекомендуется проводить относительно медленно, при определенных значениях [Н+] и температуры.
Установка титра раствора перманганата калия
В коническую колбу приливают точно 20 мл щавелевой кислоты (Nщ.к. = 0,05), подкисляют 20 мл серной кислоты (1:8), нагревают до появления паров воды (60-70 оС) и титруют раствором перманганата калия до появления устойчивой бледно-розовой окраски.
|
|
|
2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 + 2MnSO4 + 8H2O + 10 CO2
Титрование проводят 3-5 раз для получения сходимых результатов.
Нормальность раствора перманганата калия рассчитывают по формуле:
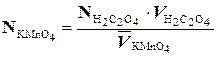 ,
,
где 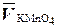 - средний объем KMnO4, пошедший на титрование, мл.
- средний объем KMnO4, пошедший на титрование, мл.
Дата добавления: 2019-09-13; просмотров: 322; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
