Экспериментальная часть. Получение азота разложением нитрита аммония
Азот в лаборатории получают при взаимодействии насыщенных растворов хлорида аммония и нитрита калия. Образующийся в результате реакции обмена нитрит аммония легко разлагается с образованием азота и воды.
Оборудование: колба Вюрца, делительная воронка, газоотводная трубка, лучина, цилиндр стеклянный, кристаллизатор, стеклянная пластина, горелка, штатив.
Техника безопасности. Соблюдать правила работы с нагревательными приборами.
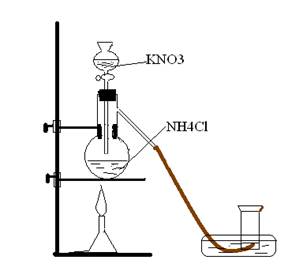
Эксперимент: В колбу Вюрца нальем раствор хлорида аммония 20 мл, а капельную воронку раствор нитрита калия. При приливании нитрита калия, через капельную лейку в колбу начинается выделение азота. Сначала реакция идет медленно, затем ускоряется. Необходимо подогреть колбу с хлоридом аммония, если реакция проходит недостаточно быстро.
KNO2 + NH4Cl = KCl + NH4NO2
NH4NO2 = N2 + 2H2O
Соберем выделяющийся азот в цилиндр. Собирать необходимо таким образом: заполненный водой цилиндр перевернуть дном вверх и поставить в кристаллизатор с водой и внести туда газоотводную трубку. Это бесцветный газ, малорастворимый в воде. Горящая лучинка в атмосфере азота гаснет. Оставим цилиндр открытым, через некоторое время опять внесем зажженную лучинку в цилиндр. Лучинка продолжает гореть. Азот улетучился из цилиндра. Азот немного легче воздуха.
А также при сбалтывании известняковой воды в цилиндре с азотом осадок не образовывается, в отличии от взбалтывания с диоксидом углерода.
|
|
|
N2+Ca(OH)2≠ осадок
Ca(OH)2 + CO2=CaCO3↓+H2O
Вывод: В результате проведенного синтеза получила азот, что подтвердила опытами [17].
Вывод
Азот очень важный и интересный элемент не только для химии, но и для человечетва в общем. В большой части азот находится в природе в свободном состоянии. Имеет 2 стабильных изотопа. Его молекула очень стойкая и мало реакционноспособная, лишь при очень высоких температурах она вступает в реакцию с различными металлами и неметаллами. Найдена некоторая схожесть атома азот с атомом карбона.
В 1964 году опубликовано первое сообщение о возможности восстановления N2 в апротонных средах (эфиры, углеводороды) в мягких условиях в присутствии комплексов переходных металлов (реакция Вольпина-Шура).
Были обнаружены реакции восстановления азота до гидразина и аммиака в водных или водно-спиртовых средах (в протонных средах). Катализаторами реакций восстановления в этих гетерогенных системах служат Mo(III) и V(II), а восстановителями - Ti(III), Cr(II) и V(II).
Изучение механизмов активации и восстановления азота в растворах комплексов переходных металлов, несомненно, очень важно для понимания механизма действия фермента нитрогеназы и создания химических моделей этого фермента. В этой связи очень интересны последние достижения в изучении структуры окислительно-восстановительных центров фермента.
|
|
|
Важнейшими соединениями азота и наиболее распространёнными являются аммиак, оксиды азота и азотная и азотистая кислоты (которые, к сожалению, не будут рассмотрены в данной работе). Азот и водород взаимодействуют, образуя соединения, отдаленно напоминающие углеводороды. Стабильность азотоводородов уменьшается с увеличением числа атомов азота в цепи в отличие от углеводородов, которые устойчивы и в длинных цепях. Наиболее важные нитриды водорода – аммиак NH3 и гидразин N2H4. В соединениях с кислородом азот проявляет все степени окисления, образуя оксиды: N2O, NO, N2O3, NO2 (N2O4), N2O5. Имеется скудная информация об образовании пероксидов азота (NO3, NO4). Сам азот и его соединения имеют очень широкое применение в промышленности и сельском хозяйстве и играют важную роль в жизни биологических организмов, как растений так и человека.
Список литературы
1. Новое в химической фиксации азота / Ред. Дж. Чатт, М.Е. Вольпин. М.: Мир, 1983.
2. Вольпин М.Е., Шур В.Б. Фиксация молекулярного азота в апротонных средах // Новое в химической фиксации азота. М.: Мир, 1983. С. 77.
|
|
|
3. Шилов А.Е. Фиксация азота в растворах в присутствии комплексов переходных металлов // Успехи химии. 1974. № 5. С. 863.
4. Шилов А.Е. Сопоставление биологической фиксации азота с химической фиксацией в модельных системах // Новое в химической фиксации азота. М.: Мир, 1983. С. 132.
5. Ричардс Р.Л. Восстановление диазотного лиганда // Там же. С. 214.
6. Temkin M. The Kinetics of Some Industrial Heterogeneous Catalytic Reactions // Adv. Catal. 1979. Vol. 28. P. 173.
7. Кучаев В.Л., Шапатина Е.Н., Аветисов А.К. О выводе кинетического уравнения синтеза аммиака вдали от равновесия // Кинетика и катализ. 1995. Т. 36, № 5. С. 726.
8. Справочник азотчика. М.: Химия, 1969.-492с.
9. Некрасов Б.В. Основы общей химии. М.: ГХИ, 1963
10. Проблемы фиксации азота. Неорганическая и физическая химия. М., 1982
11. Дж. Трефил Природа науки. 200 законов мироздания, изд. Гелиос, 2000.
12. Ахметов Н.С. Общая и неорганическая химия. М.: Высшая школа, 1981
13. Справочник по элементарной химии. Под общей редакцией А.Т. Пилипенко. Изд. 2-е перераб. и доп. К., «Наукова думка», 1977. 544 с.
14. Рэмсден Э.Н. Начала современной химии. Справ. изд. Пер. с англ./ под ред. В.И. Барановского - Л.: Химия,1989. - 784с.
15. Глинка Н.Л. Общая химия-Л.:химия,1985.-702с.
16. Терлецкий Е.Д. Азот. Популярная библиотека химических элементов. «Наука» М. 1983. с 96-112.
17. Калугин О.М., Вьюник И.М. Методичні вказівки до лабораторного практикуму курсу неорганічної хімії-Х.: ХДУ, 1997.-72 с.
Дата добавления: 2019-07-15; просмотров: 263; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
