Применения дсорбциооных процессов в медицине
Применение адсорбционных процессов в медицине
Адсорбция лежит в основе клинического анализа крови на СОЭ (скорость осаждения эритроцитов). Так, при инфекционных заболеваниях в крови происходит обменная адсорбция: вместо ионов электролитов поверхность эритроцитов занимают молекулы белков. При этом заряд эритроцитов понижается и они быстрее объединяются и оседают.
Адсорбционная терапия применяется для удаления токсинов и вредных веществ из пищеварительного тракта. Такие адсорбенты, как гидроксид алюминия, оксид магния, фосфат алюминия, входят в состав препаратов альмагель, фосфалюгель. Активированный уголь давно применяется как адсорбент газов (при метеоризме), токсинов (при пищевых токсикоинфекциях), алкалоидов и тяжелых металлов (при травлениях).
Хорошей адсорбирующей способностью обладает клетчатка. Содержание клетчатки у больных сахарным диабетом должно быть не меньше 25 г/1000 ккал: клетчатка замедляет всасывание сахаров, компенсируя повышение концентрации глюкозы в плазме после приема пищи.
На основе оксида кремния создан препарат полисорб – неселективный полифункциональный энтеросорбент. Его применяют для выведения из организма патогенных бактерий и их токсинов, пищевых аллергенов, солей тяжелых металлов, радионуклидов, этанола, а также ядов различного происхождения.
Хроматография
Хроматография – метод разделения веществ при прохождении раствора или газа через колонку с адсорбентом. Метод хроматографии широко используется для веществ, в том числе и неокрашенных. Для этого длинные тонкие капилляры с пористыми стенками или заполняют более широкие трубки зернами пористого адсорбента (оксида алюминия, оксида магния, древесного угля и др.). Это приводит к возникновению большой поверхности раздела фаз, следовательно, при медленном прохождении газа осуществляются многократно повторяющиеся процессы адсорбции и десорбции молекул компонентов газовой смеси. Это позволяет получить разные времена выходов компонентов из колонки или т.н. разные времена удерживания. Такой вид хроматографии называют газоадсорбционной хроматографией.
|
|
|
Если же крупные поры адсорбента заполнить неподвижной жидкостью, то вместо различий в адсорбируемости можно использовать различия в растворимости отдельных компонентов газовой смеси – газожидкостная хроматография.
Хроматографическое разделение смесей веществ может осуществляться разными способами:
1 способ:в колонку с адсорбентом вводят газовую смесь с постоянной концентрацией компонентов. У выхода из колонки появляются наименее адсорбирующийся или наименее растворимый компонент, затем смесь этого компонента с несколько более легко адсорбирующимся компонентом, затем смесь двух компонентов с еще более легко адсорбирующимся и т.д. вплоть до исходной газовой смеси. Такой анализ называют фронтальным. Недостатком его является то, что в чистом виде можно получить только первый компонент.
|
|
|
2 способ: через колонку с адсорбентом пропускают непрерывный поток практически неадсорбирующегося газа (газ-носитель), в который у входа в колонку вносят небольшую порцию анализируемой смеси. В этом случае у выхода из колонки в токе газа-носителя сначала появляется наименее адсорбирующийся компонент газовой смеси, затем газ-носитель, затем смесь первого компонента с более легко адсорбирующимся газом, затем газ-носитель и т.д. Таким образом, зоны выхода компонентов на хроматограмме оказываются разделенными газом-носителем. Такой анализ называется проявительнойхроматографией.
43. Специфические свойства ВМС.
Высокомолекулярные соединения обладают специфическим комплексом физико-химических и механических свойств. Важнейшие из них:
1) способность образовывать высокопрочные анизотропные волокна и пленки;
|
|
|
2)способность к большим обратимым, так называемым высокоэластическим, деформациям;
3) способность набухать перед растворением и образовывать высоковязкие растворы.
Эти свойства обусловлены высокой молекулярной массой высокомолекулярных соединений, цепным строением макромолекул, их гибкостью и наиболее полно выражены у линейных высокомолекулярных соединений. По мере перехода от линейных цепей к разветвленным, редким трехмерным сеткам и, наконец, к частым сетчатым структурам комплекс характерных свойств высокомолекулярных соединений становится все менее выраженным. Трехмерные высокомолекулярные соединения с очень большой частотой сетки нерастворимы, неплавки и неспособны к высокоэластичным деформациям.
По фазовому состоянию высокомолекулярные соединения могут быть кристаллическими или аморфными. Необходимое условие кристаллизации - регулярность достаточно длинных участков молекулярной цепи. В таких высокомолекулярных соединениях возможно образование разнообразных кристаллических форм (фибрилл, сферолитов, монокристаллов и других), тип которых во многом определяет свойства полимерного материала. Аморфные высокомолекулярные соединения помимо высокоэластического могут находиться в двух других физических состояниях: стеклообразном состоянии и вязкотекучем состоянии. Высокомолекулярные соединения, которые переходят из высокоэластичного состояния в стеклообразное при температурах ниже комнатной, относят к эластомерам, при более высокой температуре - к пластикам. Кристаллические высокомолекулярные соединения обычно являются пластиками.
|
|
|
Свойства отдельных высокомолекулярных соединений определяются химическим составом, строением, конформацией и взаимным расположением макромолекул (надмолекулярной структурой). В зависимости от этих факторов свойства высокомолекулярных соединений могут изменяться в широких пределах. Так, цис-1,4-полибутадиен, построенный из гибких углеводородных цепей, при температурах около 20°С представляет собой эластичный материал, который ниже -90°С переходит в стеклообразное состояние, тогда как полиметилметакрилат, построенный из более жестких цепей, при температурах около 20°С - твердый стеклообразный продукт, переходящий в высокоэластичное состояние лишь выше 100°С. Целлюлоза - полимер с очень жесткими цепями, соединенными межмолекулярными водородными связями, - вообще не может существовать в высокоэластичном состоянии до температуры ее разложения. Большие различия в свойствах высокомолекулярных соединений могут наблюдаться даже в том случае, когда различия в строении макромолекул на первый взгляд и невелики. Так, изотактический полипропилен - кристаллическое вещество, плавящееся около 175°С, а атактический полипропилен вообще не способен кристаллизоваться и размягчается около —40°С. В данном случае различия в микроструктуре макромолекулярной цепи определяют качественные различия и в характере надмолекулярной структуры.
Bысокомолекулярные соединения могут вступать в следующие реакции:
1) соединение макромолекул поперечными химическими связями (так называемое сшивание), происходящее, например, при вулканизации каучуков, отверждении реактопластов, дублении кож;
2) распад молекулярных цепей на более короткие фрагменты;
3) реакции макромолекул с низкомолекулярными соединениями, при которых изменяется природа боковых функциональных групп, но сохраняются длина и строение скелета основной цепи (так называемые полимераналогичные превращения), например, омыление поливинилацетата с образованием поливинилового спирта; высокомолекулярные соединения, образующиеся в результате таких реакций, называются полимераналогами;
4) внутримолекулярные реакции между функциональными группами одной макромолекулы, например внутримолекулярная циклизация.
Гетероцепные высокомолекулярные соединения в отличие от карбоцепных обычно относительно легко гидролизуются. Скорость реакций высокомолекулярных соединений, особенно сетчатых, с низкомолекулярными веществами часто лимитируется скоростью диффузии низкомолярного вещества в фазу высокомолекулярного соединения. В кинетической области (например, в разбавленном растворе) скорость взаимодействия макромолекул с низкомолекулярными веществами часто существенно зависит от природы и расположения соседних звеньев относительно реагирующего звена. Это же относится и к внутримолекулярным реакциям между функциональными группами, принадлежащими одной цепи.
Некоторые свойства высокомолекулярных соединений, например растворимость, способность к вязкому течению, стабильность, существенно зависят от небольших количеств примесей или добавок, реагирующих с макромолекулами. Так, чтобы превратить линейный полимер из расторимого в полностью нерастворимый, достаточно одной-двух поперечных связей на одну макромолекулу.
44. Понятие биогенности химических элементов.
Биогенные элементы, химические элементы, постоянно входящие в состав организмов и имеющие определённое биологическое значение.
Прежде всего это кислород (составляющий 70% массы организмов), углерод (18%), водород (10%), кальций, азот, калий, фосфор, магний, сера, хлор, натрий, железо. Эти элементы входят в состав всех живых организмов, составляют их основную массу и играют большую роль в процессах жизнедеятельности. Успехи аналитической химии и спектрального анализа расширили перечень Б. э.: находят всё новые элементы, входящие в состав организмов в малых количествах (микроэлементы), и открывают биологическую роль многих из них.
В. И. Вернадский считал, что все химические элементы, постоянно присутствующие в клетках и тканях организмов в естественных условиях, вероятно, играют определенную физиологическую роль. Многие элементы имеют большое значение только для определённых групп живых существ (например, бор необходим для растений, ванадий - для асцидий и т.п.).
Содержание тех или иных элементов в организмах зависит не только от их видовых особенностей, но и от состава среды, пищи (в частности, для растений - от концентрации и растворимости тех или иных почвенных солей), экологических особенностей организма и других факторов.
При нарушении поступления в организм того или иного Б. э. возникают заболевания - биогеохимические эндемии, например зоб у человека при недостатке иода в воде и пище или чёрная пятнистость свёклы при нехватке бора. Элементы, постоянно содержащиеся в организмах млекопитающих, по их изученности и значению можно разделить на 3 группы: элементы, входящие в состав биологически активных соединений (ферменты, гормоны, витамины, пигменты) (I - макроэлементы), они являются незаменимыми; элементы, физиологическая и биохимическая роль которых мало выяснена (II - микроэлементы) или неизвестна (III - ультрамикроэлементы).
45. Химия биогенных элементов s-блока.
S -элементы – элементы, у атомов которых электроны заселяются на s подуровни внешнего уровня.
Свойства:
· Типичные металлы
· Легко отдают электроны
· Обладают сильными восстановительными свойствами
· Высокая электро- и теплопроводность
· Химически очень активны
· Имеют малое значенте энергии инициации
· Образуют соединения с ионным типом связи
· Большинство соединений растворимы в воде, поэтому ионы этих металлов могут мигрировать из водных растворов в организмы животных, растений и человека
H2, Na, K, Mg, Ca – жизненно необходимые для растений и животных. По содержанию в организме H2, Mg, K относят к макроэлементам, остальные к микроэлементам.
46. Химия биогенных элементов d-блока.
D -элементы – элементы, у атомов которых электроны заселяются на d подуровни внешнего уровня.
Данный блок представляет собой часть периодической таблицы; в него входят элементы от 3 до 12 группы. Элементы данного блока заполняют d-оболочку d-электронами, которая у элементов начинается s2d1 (третья группа) и заканчивается s2d10 (двенадцатая группа). Однако существуют некоторые нарушения в этой последовательности, например, у хрома s1d5 (но не s2d4) вся одиннадцатая группа имеет конфигурацию s1d10 (но не s2d9). Одиннадцатая группа имеет заполненные s- и d-электроны.
D-блок-элементы также известны как переходные металлы или переходные элементы. Однако точные границы, отделяющие переходные металлы от остальных групп химических элементов, еще не проведены. Хотя некоторые авторы считают, что элементы, входящие в d-блок, являются переходными элементами, в которых d-электроны являются частично заполненными либо в нейтральных атомах или ионах, где степень окисления равна нулю.
Большинство элементов данного блока относятся к ультрамикроэлементам.
47. Химия биогенных элементов p-блока.
P -элементы – элементы, у атомов которых электроны заселяются на d подуровни внешнего уровня.
К ним относятся 30 элементов с IIА по VIIА группы периодической системы; входят во 2 и 3 малые периоды, также 4-6 большие периоды.
Свойства:
· В периоде с лева на право атомный и ионные радиусы уменьшаются, а энергия ионизации и сродство к электронам увеличивается
· В группах радиусы атомов увеличиваются, так как по мере роста числа электронных оболочек увеличивается экранирование зарядов электронов
· С увеличением порядкового номера неметаллические свойства возрастают
Большинство элементов данного блока относятся к микроэлементам.
48. Поли- и гетерофункциональность как один из характерных признаков органических соединений, участвующих в процессах жизнедеятельности и используемых в качестве лекарственных веществ. Особенности химического поведения поли- и гетерофункциональных соединений: кислотно-основные свойства (амфолиты), циклизация и хелатообразование. Взаимное влияние функциональных групп.
Полифункциональные органические соединения – соединения, в молекулах которых есть несколько одинаковых функциональных групп. Наиболее часто встречаются карбоксильная и гидроксильная группы.
Гетерофункциональные органические соединения – соединения, в молекулах которых есть несколько разных функциональных групп. Наиболее часто встречаются аминоспирты, аминокислоты, оксокислоты и аминокарбоксиллы.
Эти два типа органических соединений активноучаствуют в процессах жизнедеятельности (Например: некоторые соли щавелевой кислоты присутствуют в почках; малиновая и фумаровая кислоты участвуют в обменных процессах организма; оланин входит в состав сложных липидов) и используются в качестве лекарственных веществ (Например: бензольная кислота используется в отхаркивающих препаратах; солициловая кислота и её производные – антигрибковае и жаропонижающие препараты).
Кислотно-основные свойства: у полифункциональных соединений кислотность больше, чем у одноатомных; у гетерофункциональных кислотно-основные свойства от природы и положения в молекуле меньше или больше, чем у полифункциональных.
Циклизация - реакция внутри- или межмолекулярного образования (замыкания) цикла из ацикличных молекул либо фрагментов карбо- или гетероцикла. Циклизация с образованием гетероцикла называется также гетероциклизацией, циклизация с замыканием нового цикла на уже существующем - аннелированием.
Некоторые полифункциональные и гетерофункциональные соединения образуются путём циклизации: из гидроксикислот путём внутренней циклизации образуются амины лактаны.
Хелатообразование - химический процесс, в котром к иону или к атому металла посредством двух или более ковалентных связей присоединяются органические молекулы, охватывающие его как бы клешнями (назв. процесса произошло от лат. chele - "клешня"). Природные хелаты (напр., в почвах) устойчивы в кислых средах, но разрушаются в щелочной среде с высвобождением иона металла. Они хорошо растворимы в воде и окрашены. Их используют для определения спиртов.
49.ПОЛИФУНКЦИОНАЛЬНЫЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Общая характеристика
Полифункциональными называют соединения, в молекулах которых имеется несколько одинаковых функциональных групп.
Среди полифункциональных соединений, участвующих в процессах жизнедеятельности, наиболее широко представлены соединения с гидроксильными и карбоксильными функциональными группами. Специальный интерес представляют β-дикарбонильные соединения. Соединения с несколькими аминогруппами встречаются реже.
Многоатомные спирты и фенолы
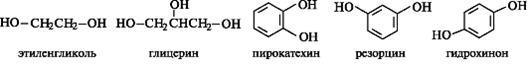
Двухатомные спирты, т. е. спирты, содержащие две гидроксильные группы, имеют общее название диолы, или гликоли;трехатомные спирты называют триолами. Представителями таких спиртов являются этиленгликоль и глицерин соответственно. Общее название многоатомных спиртов - полиолы.
В состав многих природных соединений входят в виде фрагментов двухатомные фенолы - пирокатехин, резорцин, гидрохинон.
Этиленгликоль (этандиол-1,2) - высокотоксичная жидкость (т. пл. -16 ?С, т. кип. 197 ?С), используется в технике для приготовления антифризов - жидкостей с низкой температурой замерзания.
Глицерин (пропантриол-1,2,3) - нетоксичная вязкая жидкость сладкого вкуса (т. пл. 17 ?С, т. кип. 290 ?С), входит в состав большинства липидов (см. 10.3.2). Применяется как компонент мазей для смягчения кожи.
Пирокатехин (о-дигидроксибензол), называемый также катехолом, является структурным фрагментом многих биологически активных
веществ, в частности катехоламинов (см. 9.2.1). Монометиловый эфир пирокатехина - гваякол - применяется как компонент в составе лекарственных средств при катаре верхних дыхательных путей.
Резорцин (м-дигидроксибензол) используется как антисептик и дезинфицирующее средство при кожных заболеваниях.
Гидрохинон (п-дигидроксибензол), обладающий восстановительной способностью, является структурным фрагментом ряда соединений. В организме восстановительная способность замещенного гидрохинонового фрагмента делает его участником важного процесса транспорта электронов от окисляемого субстрата к кислороду.
К спиртам высшей атомности относятся пентиты и гекситы, т. е. соответственно пяти- и шестиатомные спирты с открытой цепью. Накопление гидроксильных групп в молекуле ведет к появлению сладкого вкуса. Представители пентитов и гекситов - ксилит и сорбит (см. 11.1.5) - заменители сахара для больных диабетом.
Многоатомный циклический спирт миоинозит (см. 7.2.2) относится к витаминоподобным соединениям (витамины группы В) и является структурным компонентом сложных липидов - фосфатидилинозитов (см. 10.4.1). В растениях широко распространена фитиновая кислота, представляющая собой гексафосфат миоинозита. Кальциевая или смешанная кальций-магниевая соль фитиновой кислоты, называемая фитином, улучшает состояние нервной системы при заболеваниях, связанных с недостатком фосфора в организме.
50 Полиамины: этилендиалин.путресцин.кадоверин.
Полиамины- полимеры содержащие в повторяющемся звене макромолекулы первичные, вторичные, третичные или четвертичные аминогруппы. Термин "П." часто используют также для обозначения низкомол. и олигомерных аминов , содержащих в молекуле две или более аминогруппы, напр. полиэтиленполиамины . Известны сетчатые, разветвленные и линейные П.
П., содержащие первичные, вторичные и третичные аминогруппы,-слабые полиоснования (см. Полиэлектролиты). Способность их растворяться в воде и орг. р-рителях определяется как соотношением гидрофильной (аминогруппы) и гидрофобной (углеводородная часть) составляющих макромолекулы, так и степенью протонирования a аминогрупп. При увеличении a добавлением к-т повышается р-римость П. в воде и понижается в орг. р-рителях. П., содержащие четвертичные аммониевые группы (ионены),- сильные полиоснования и, как правило, хорошо раств. только в водных средах.
П., в макромолекулах к-рых имеются первичные и вторичные аминогруппы, образуют комплексы с ионами металлов, такими, как Cu2+ , Co2+ , Ni2+ , Fe2+ , Fe3+ . Кроме того, П. образуют устойчивые полимер-полимерные комплексы с полимерными анионами, в цепях к-рых находятся группы Ч COO-, -SO3- и -PO3-, в т. ч. с макромолекулами белков, нуклеиновых к-т, гепарина, а также с анионными ПАВ. П., в макромолекулах к-рых содержатся длинные алифатич. заместители, обладают поверхностной активностью, их наз. "полимылами".
П. способны подвергаться разнообразным полимерана-логичным превращ. благодаря тому, что для них характерны все хим. превращ. реакционноспособных низкомол. аминов . Это дает возможность, вводя в П. разл. функц. группы, напр. ОН, CONH2 , COOH, SO3H, получать полифункциональные полимеры - полиамидамины, полиамино-спирты, полиаминокислоты и др.
Нек-рые П.-физиологически активные соед.; обладают высокой токсичностью при введении в кровь, поскольку вызывают агрегацию форменных элементов крови-эритроцитов, тромбоцитов, лимфоцитов; эффективно взаимод. с клеточными мембранами, изменяя их проницаемость.
П. получают всеми известными р-циями, используемыми для синтеза полимеров: ионной и радикальной полимеризацией (ур-ния 1 и 2), поликонденсацией (3) и полимеранало-гичными превращ. (4)
Этилендиамин (1,2-диаминоэтан) H2NCH2CH2NH2 — органическое соединение класса аминов . Это широко используемый строительный блок в химическом синтезе Жидкость без цвета с запахом аммиака, испаряется при контакте с влажным воздухом. tkип 116,5 °C, tпл 8,5 °C, плотность 0,899 г/см³ (20 °C); Этилендиамин хорошо растворяется в воде (с разогреванием раствора), этаноле , хуже — в эфире , нерастворим в бензоле и других углеводородах. Является сильным основанием .
Имея в своей молекуле две аминогруппы, образует с кислотами два ряда солей. С некоторыми металлами (например, Cu, Mn, Co) образует комплексные соединения.
Динитрат этилендиамина при нагревании превращается в этилендинитрамин , являющийся взрывчатым веществом :
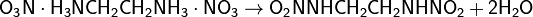
Вступает в реакции конденсации: при повышенных температурах и давлении и присутствии катализаторов превращается в пиперазин ; при конденсации с 1,2-дикетонами - 2,3-дигидропиразинами; при реакции с мочевиной - этиленмочевину (2-имидазолининон).
Путресцин вместе с кадаверином впервые были описаны в 1885 году берлинским врачом Людвигом Бригером (1849-1919) [1] в продуктах гнилостного распада белков
. Бесцветное кристаллическое вещество с чрезвычайно неприятным запахом, плохо растворимое в воде , имеет низкую темперературу плавления (tпл= 27—28 °C), является сильным основанием.
Образуется при декарбоксилировании бактериями аминокислоты орнитина . В тканях организма путресцин — исходное соединение для синтеза двух физиологически активных полиаминов — спермидина и спермина . Эти вещества наряду с путресцином, кадаверином и другими диаминами входят в состав рибосом , участвуя в поддержании их структуры
Кадавери́н (от лат. cadaver — труп), α, ε-пентаметилендиамин — химическое соединение, имеющее формулу NH2(CH2)5NH2. Бесцветная жидкость с плотностью 0,870 г/см3 и tкип 178—179 °C. Кадаверин легко растворим в воде и спирте , даёт хорошо кристаллизующиеся соли. Замерзает при +9 °C. Имеет очень сильный трупный запах — отсюда название. Содержится в продуктах гнилостного распада белков ; образуется из лизина при его ферментативном декарбоксилировании . Ранее кадаверин относили к т. н. трупным ядам (птомаинам) , однако ядовитость кадаверина относительно невелика. Обнаружен у растений
Дата добавления: 2019-02-12; просмотров: 1186; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
