Значения поправочных коэффициентов на минерализацию в зависимости от температуры
| Температура, оС | 20 | 38 | 66 | 93 | 121 |
| Коэффициент, k | 0,091 | 0,074 | 0,050 | 0,044 | 0,033 |
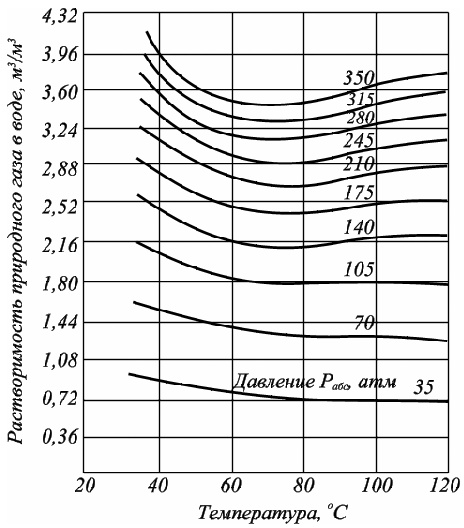
Рис. 2.8. Зависимость растворимости природного газа в пресной воде от температуры при различных давлениях
Рассмотрим пример. Определить растворимость углеводородных газов в пластовой воде при давлении 105 атм, температуре 35°С и минерализации 30000 мг/л (3 %).
Решение. Для определения растворимости углеводородных газов в пластовой воде пользуемся формулой 2.37. Находим значение коэффициента растворимости газа в пресной воде (a) используя рис. 2.8. При температуре 5оС и давлении 105 атм величина a = 2,16 м3/м3. Величина поправочного коэффициента оцениваем на основе данных таблицы 2.5, k ≈ 0,07. Растворимость углеводородного газа в пластовой воде рассчитываем по 2.37:
(a)рт = 2,16 · (1 – (0,0 7 · 3) = 2,16 · 0,79 = 1,7 (м3/м3).
Растворимость газа зависит от температуры. С увеличением температуры растворимость углеводородов в воде вначале уменьшается, а затем возрастает, пройдя через максимум (рис. 2.9). Причем температура минимальной растворимости различных газов возрастает с увеличением размера молекулы газа. Температура минимальной растворимости газов зависит от давления.
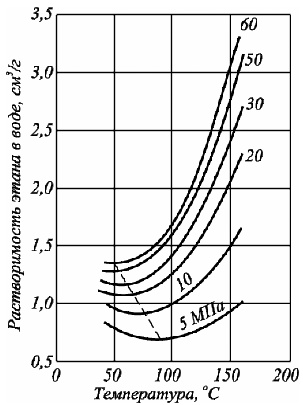
Рис. 2.9. Изменение температуры минимальной растворимости этана в зависимости от давления при 0oС
Коэффициент растворимости нефтяных газов в воде изменяется в широких пределах и достигает 4-5·10-5 м3/(м3·Па).
Количество выделившегося из нефти газа зависит не только от содержания газа в нефти, но и от способа дегазирования. Различают контактное разгазирование, когда выделившийся газ находится в контакте с нефтью, и дифференциальное разгазирование, когда выделившийся из нефти газ непрерывно отводится из системы. Строгое соблюдение условий дифференциального дегазирования в лабораторных условиях затруднено, поэтому оно заменяется на ступенчатое дегазирование, используется многократное (ступенчатое) разгазирование.
В процессе добычи нефти встречаются оба способа дегазирования. В начальные периоды снижения давления от давления насыщения, когда газ ещё неподвижен относительно нефти, происходит контактное разгазирование. В последующий период, по мере выделения газа из нефти, газ быстрее движется к забою скважины и можно говорить о дифференциальном разгазировании
Коэффициент разгазирования определяется как количество газа, выделившегося из единицы объёма нефти при снижении давления на единицу. Коэффициент разгазирования при контактном способе разгазирования будет меньше, чем при дифференциальном способе разгазирования.
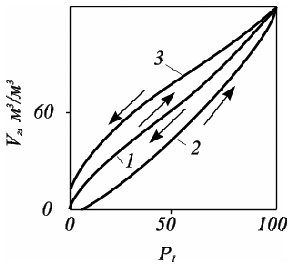
Рис. 2.10. Зависимость количества растворенного в нефти газа от давления при: 1. – контактных процессах растворения и дегазации; 2. – дифференциальном растворении; 3. – дифференциальной дегазации
При дифференциальном способе разгазирования нефти количество газа, остающегося в растворенном состоянии (условия по давлению разгазирования одинаковые) будет больше, чем при контактном способе (рис. 2.10). Это связано с преимущественным переходом в паровую фазу метана в начале процесса дегазации. С удалением метана из системы при дифференциальном способе разгазирования нефти в паровой фазе увеличивается содержание тяжелых углеводородов, что вызывает повышение растворимости их в нефти.
При движении газа по пласту наблюдается так, называемый, дроссельный эффект – уменьшение давления газового потока при его движении через сужения в каналах. При этом наблюдается изменение температуры. Интенсивность изменения температуры при изменении давления характеризуется коэффициентом Джоуля–Томсона:
DТ = a · DР, (2.38)
где DТ – изменение температуры
a – коэффициент Джоуля–Томсона (зависит от природы газа, давления, температуры);
DР – изменение давления.
Понижение температуры при движении газа в пласте даже при больших перепадах давления сравнительно невелико. В пластовых условиях, как правило, движение газа происходит в изотермических условиях. Ближе к забою, особенно в забойных штуцерах, процесс дросселирования газа может привести к значительному снижению температуры, что имеет большое значение при эксплуатации нефтяных месторождений с высоким содержанием парафина.
Упругость насыщенных газов
Упругость насыщенных газов
Упругость насыщенных паров углеводородов характеризует то давление, при котором газ начинает конденсироваться и переходить в жидкое состояние. У индивидуальных углеводородов в чистом виде упругость паров (Q) есть функция только температуры: Q =ѓ (Т). Величина упругости насыщенных паров углеводородов повышается с ростом температуры, и она тем выше, чем ниже плотность углеводорода. Аналогично с ростом молекулярной массы углеводорода, величина упругости насыщенный паров углеводородов уменьшается при равных температурах (рис. 2.11).
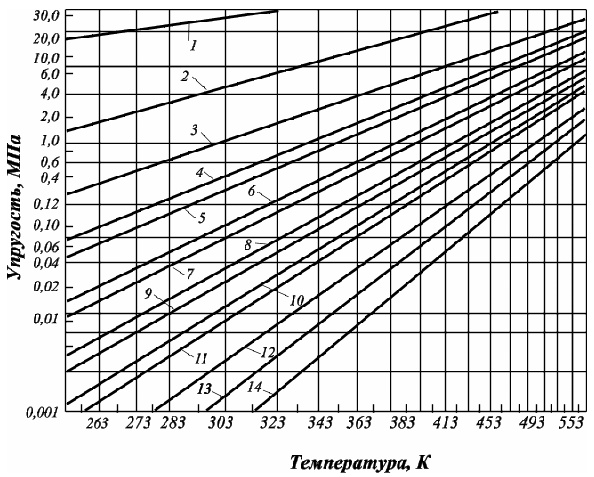
Рис. 2.11. Кривые упругости насыщенных паров чистых углеводородов:
1. – метан; 2. – этан; 3. – пропан; 4. – изобутан; 5. – бутан; 6. – изопентан; 7. – пентан; 8. – изогексан; 9. – гексан; 10. – изогептан; 11. – гептан; 12. – октан; 13. – нонан; 14. – декан
Зависимость упругости пара от температуры: Q =ѓ (Т) – нелинейная функция. Для ее линеаризации шкала упругости пара принята логарифмической, и это создает удобства для пересчета величины упругости пара при нужной температуре. Анализ зависимостей представленных на рис. 2.11 свидетельствует, что давление паров метана наибольшее. При нормальных условиях его нельзя превратить в жидкость (пунктирная линия), так как его критическая температура (Ткр.) = – 82,4о С (190,75 К).
На рис. 2.12, а изображены зависимости объёма жидкого и парообразного пропана. При сжатии от точки М до точки А имеется перегретый (ненасыщенный) пар, зависимость объёма жидкости от давления при конкретной температуре имеет гиперболическую форму.
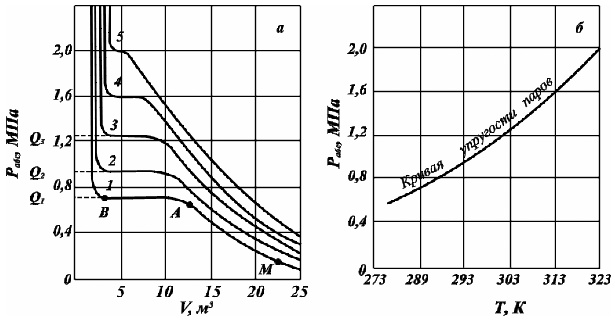
Рис. 2.10. Зависимости давления от объёма и температуры (а) и кривая упругости насыщенных паров (б) при температурах, К: 1. – 283; 2. – 293; 3. – 303; 4. – 313; 5. – 323.
В точке А пар становится насыщенным, а при дальнейшем изменении объёма (участок АВ) он постепенно переходит в жидкость при неизменном давлении. В точке В заканчивается переход пара в жидкость. При дальнейшем сжатии пара будет резко повышаться давление при почти неизменном объёме. Горизонтальный участок АВ соответствует неизменности давления в процессе конденсации паровой фазы в жидкую фазу. Величина этого давления и есть упругость насыщенного пара газового компонента при данной температуре. Чем ближе значение температуры, при которой измеряется упругость насыщенного пара газового компонента к значению критической температуре, тем короче горизонтальный участок. На основе полученных данных строят кривую упругости насыщенных паров, представляющую зависимость давления от от температуры испарения данной жидкости (рис. 2. 12, б).
У смеси углеводородов упругость паров является функцией и температуры и общего давления смеси: Q = ѓ (Т, Рсм.). Величина её зависит от упругости паров отдельных компонентов при данной температуре и от их мольных концентраций. Общее давление смеси влияет на упругость паров каждого компонента и это влияние учитывается по закону Рауля:
Р = ∑ рi и 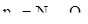 (2.39)
(2.39)
где Р – общее давление;
рi – парциальное давление i-го компонента;
Qi – упругость паров i-го компонента;
Nxi – мольная доля i-го компонента в жидкости.
Упругость паров смеси компонентов повышается с увеличением общего давления. Это влияние ничтожно при низких давлениях (≈ до 1 МПа), а при высоких давлениях упругость паров резко увеличивается.
Дата добавления: 2019-02-12; просмотров: 470; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
