Растворимость газов в нефти и воде
Растворимость газов в нефти и воде
От количества растворённого в пластовой нефти газа зависят все её важнейшие свойства: вязкость, сжимаемость, термическое расширение, плотность и другие.
Распределение компонентов нефтяного газа между жидкой и газообразной фазами определяется закономерностями процессов растворения. Способность газа, растворятся в нефти и воде, имеет большое значение на всех этапах разработки месторождений от добычи нефти до процессов подготовки и транспортировки.
Сложность состава нефти и широкий диапазон давлений и температур затрудняют применение термодинамических уравнений для оценки газонасыщенности нефти при высоких давлениях.
Процесс растворения для идеального газа при небольших давлениях и температурах описывается законом Генри:
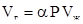 или
или 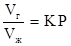 , (2.35)
, (2.35)
где Vж – объём жидкости-растворителя;
a – коэффициент растворимости газа;
Vг – объём газа, растворённого при данной температуре;
Р – давление газа над поверхностью жидкости
К – константа Генри (К = f(a)).
Коэффициент растворимости газа (a) показывает, какое количество газа (Vг) растворяется в единице объёма жидкости (Vж) при данном давлении:
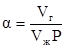 . (2.36)
. (2.36)
Коэффициент растворимости зависит от природы газа и жидкости, давления, температуры.
Природа воды и углеводородов различна. Углеводородная составляющая нефтяного газа растворяется хорошо в углеводородных системах, в нефти, а в воде хуже. Неуглеводородные компоненты нефтяного газа, такие как СО, СО2, Н2S, N2 растворяются лучше в воде. Например, пластовая вода сеноманского горизонта Западной Сибири очень газирована, она содержит приблизительно 5 м3 газа СО и СО2 на 1 т пластовой воды.
|
|
|
Растворимость углеводородов в нефти подчиняется закону Генри. С повышением давления растворимость углеводородного газа растёт.
С повышением температуры растворимость углеводородных газов в нефти ухудшается.
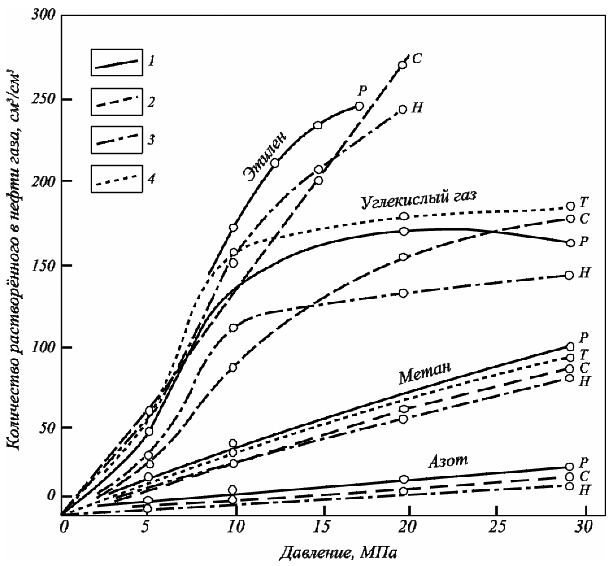
Рис. 2.5. Изотермы растворимости газов при температуре 50оС в нефтях:
1. – ромашкинская (Р); 2. – сураханская (С); 3. – небитдагская (Н);
4. – туймазинская (Т) по данным Т.П. Сафроновой и Т.П. Жузе
Разные компоненты нефтяного газа обладают различной растворимостью в нефтяных системах. С увеличением молекулярной массы газового компонента коэффициент растворимости его в углеводородных системах возрастает. На степень растворения углеводородных газов больше влияет не молекулярная масса растворителя, а его природы.
Растворимость углеводородных газов в нефти увеличивается с повышением содержания в ней парафиновых углеводородов. Работает принцип подобия: подобное растворяется в подобном. При высоком содержании ароматических углеводородов в нефти ухудшается растворимость в ней газов.
|
|
|
Растворимость углеводородов в воде не подчиняется закону Генри.
Из эксперимента известно, что при давлении 35 атм и температуре 35°С нефтяной газ растворяется в воде в количестве (Vг/Vж) = 1 м3/м3. Однако, при повышении давления в 10 раз до 350 атм растворимость газа увеличилась всего в 4 раза и составляет 4 м3/м3. Это объясняется тем, что с повышением давления растворимость газов (a) в воде увеличивается, согласно закону Генри.
Однако с увеличением давления возрастает и растворимость солей в воде, то есть увеличивается минерализация воды. При увеличении минерализации (М), растворимость газов в воде уменьшается (рис. 2.6).
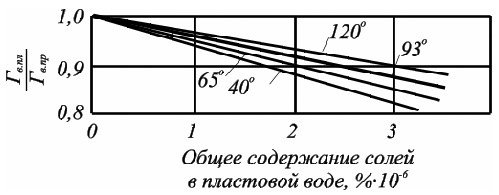
Рис. 2.6. Изменение растворимости природного газа в воде в зависимости от минерализации
Этим и объясняется отклонение зависимости растворимости углеводородов в воде от линейного вида, и при повышенных давлениях не подчинению закону Генри (рис. 2.7).
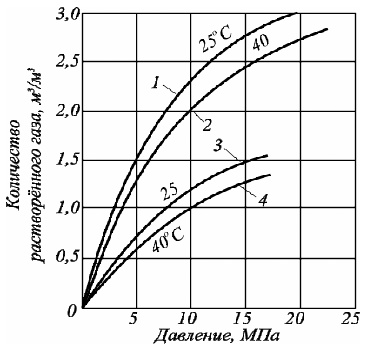
Рис. 2.7. Кривые растворимости газа в чистой и соленой воде при различных температурах и давлениях: 1,2 – дистиллированная вода; 3,4 – 2 М раствор NaCl
|
|
|
Растворимость углеводородного газа в минерализованной воде оценивается по эмпирической формуле:
aпл = aпр (1 – k М), (2.37)
где пл – растворимость нефтяного газа в пластовой воде, м3 м3;
пр – растворимость нефтяного газа в пресной воде (рис. 2.8);
k – поправочный коэффициент на минерализацию в зависимости от температуры (табл. 2.5)
М – содержание солей, %.
Таблица 2.5
Дата добавления: 2019-02-12; просмотров: 510; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
