Порядок и молекулярность для простых реакций:
1) совпадают
2) молекулярность в 2 раза больше порядка реакции
3) порядок реакции в 1,5 раза больше молекулярности
4) это зависит от условий процесса
16. Вещество, изменяющее скорость химической реакции и остающееся после этого в неизменном состоянии и количестве называется …
1) промежуточным продуктом реакции 2) восстановителем
3) катализатором 4) продуктом реакции
17. К особенностям ферментативного катализа относят:
1) высокую избирательность
2) высокую каталитическую активность
3) оптимальные значения рН и температуры
4) все предложенные варианты верны
18. Уравнение Михаэлиса-Ментена имеет вид 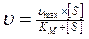 и характеризует:
и характеризует:
1) зависимость стационарной скорости ферментативной реакции от концентрации субстрата
2) соотношение между величиной константы Михаэлиса и концентрацией субстрата
3) оба утверждения верны
4) ни один из предложенных вариантов
19. Если температурный коэффициент скорости химической реакции равен 2, то при повышении температуры от 200С до 500С скорость реакции …
1) увеличивается в 8 раз 2) уменьшается в 2 раза
3) увеличивается в 6раз 4) уменьшается в 4 раза
20. Температурный коэффициент скорости химической реакции равен 2. При охлаждении системы от 100 °С до 80 °С скорость реакции…
1) не изменяется
2) увеличивается в 2 раза
Уменьшается в 4 раза
4) увеличивается в 4 раза
|
|
|
В состоянии химического равновесия скорость прямой реакции ________ скорости обратной реакции.
1) равна
2) меньше
3) не зависит от
4) больше
22. Для увеличения скорости прямой реакции 2NO(г) + О2(г)↔2NO2(г) в 1000 раз, необходимо увеличить давление в ____раз
1) 500
2) 50
3) 330
4) 10
23. Правило Вант-Гоффа выражает зависимость скорости химической реакции от…
Температуры
2) времени
3) концентрации
4) природы реагентов
Введение катализатора в систему приводит к ______ реакции.
1) изменению энтальпии
2) изменению энтропии
Уменьшению энергии активации
4) увеличению энергии активации
25. Скорость элементарной реакции  при увеличении концентрации С l2 в 3 раза увеличится в ____раз(а).
при увеличении концентрации С l2 в 3 раза увеличится в ____раз(а).
1) 3
2) 6
3) 9
4) 2
26. Если скорость реакции увеличилась в 27 раз при повышении температуры на 300С, то температурный коэффициент скорости равен…
1) 3 2) 9 3) 2,7 4) 2
27. Температурный коэффициент скорости реакции равен 3. Скорость реакции, при повышении t от 3000С до 3400С увеличивается в _____ раз
1) 9 2) 27 3)12 4) 81
28. Скорость реакции между растворами хлорида калия и нитрата серебра, концентрации которых составляют 0,2 и 0,3 моль/л соответственно, а k=1,5×10-3л/моль×с равна ____ моль×л-1×с-1:
|
|
|
1) 9×10-5 2) ) 6×10-2 3) 9×10-1 4) 9×10-3
29. Увеличение скорости реакции под действием катализатора происходит в результате…
1) увеличения концентрации реагентов
2) уменьшения концентрации продуктов
3) увеличения температуры
4) уменьшения энергии активации
30. При увеличении давления в системе в 2 раза скорость элементарной реакции 2SO2+O2↔2SO3 увеличивается в _____раз
1) 8 2) 6 3) 4 4) 2
31. При повышении давления в 2 раза скорость гомогенной элементарной химической реакции 2NO+Cl2=2NOCl увеличивается в ______ раз
1) 2 2) 4 3) 8 4) 6
13) В состоянии химического равновесия скорость прямой реакции______ скорости обратной реакции:
1) больше 2) не зависит 3) меньше 4) равна
32. Система, для которой математическое выражение закона действующих масс имеет вид k=[CO], является…
1) CaO (т ) +3 C(т ) « CaC2(т ) + CO(г )
2) Fe3O4(т) + 4 C(т) « 3 Fe(т) + 4 CO(г)
3) Fe3O4(т ) + C(т ) « 3 FeO(Т ) + CO(г )
4) CaCO3(т) + 4 C(т) « CaC(т) + 3 CO(г)
33. При повышении давления в 2 раза скорость гомогенной элементарной химической реакции  увеличивается в ___ раз(–а).
увеличивается в ___ раз(–а).
|
|
|
1) 8 2) 6 3) 4 4) 2
Дата добавления: 2019-01-14; просмотров: 356; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
