В воде объемом 200 мл растворили соль массой 40 г. Определите массовую долю соли в полученном растворе, приняв плотность воды равной 1 г/мл.
1) 1,8% 2) 2 моль/л 3) 16,7% 4) 0,48
Укажите расчетную формулу и единицы измерения моляльной концентрации
1)  ; [моль/кг]
; [моль/кг]
2)  ; [моль/г]
; [моль/г]
3)  ; [моль×г]
; [моль×г]
4) 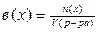 ; [моль/л]
; [моль/л]
Рассчитайте молярную концентрацию раствора, содержащего 117 г хлорида натрия
1) 2 моль/кг 2) 2,8 моль/л 3) 0,5 моль/кг 4) 2М
17. Эквивалент – это:
1) величина, соответствующая числу моль растворенного вещества
2) величина равная степени диссоциации
3) количество вещества, выпавшее в осадок
4) безразмерная величина равная основности кислоты; кислотности основания; для солей соответствует валентности металла, помноженное на количество его атомов; в окислительно-восстановительных реакций соответствует количеству электронов
18. Определите значение фактора эквивалентности для К MnO 4 в кислой среде
1) 1/2 2) 3/4 3) 1/5 4) 1,5 моль
Рассчитать молярную массу эквивалента серной кислоты
1) 46 кг/моль 2) 98 г/моль 3) 49 г/моль 4) 98 %
20. Формула для расчета молярной доли компонента в растворе имеет вид:
1) 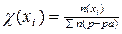 2)
2) 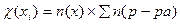
3)  4)
4) 
К метиловому спирту массой 32 г плотностью 0,8 г/мл добавили воду до объема 80 мл. Определите объемную долю спирта в растворе
1) 2% 2) 50% 3) 64 моль/л 4) 46 г/моль
|
|
|
Рассчитать молярную концентрацию эквивалента хлороводородной кислоты массой 73 г в 10 л раствора
1) 8% 2) 0,2 моль/л 3) 24 г/л 4) 0,46
При смешивании воды объемом 50 мл (плотностью 1 г/мл) и метилового спирта объемом 70 мл (плотностью 0,8 г/мл) получили раствор с плотностью 0,9 г/мл. Определите объемную долю метилового спирта в растворе
1) 47 моль/л 2) 68 моль/л 3) 59,4 % 4) 5,94 %
24. Какую массу медного купороса CuSO 4×5 H2 O и воды надо взять для приготовления раствора сульфата меди ( II) массой 40 кг с массовой долей CuSO 4 2%?
1) 1,25 кг CuSO4×5H2O и 38,75 кг H2O 2) 100 кг CuSO4×5H2O и 56 кг H2O
3) 12 кг CuSO4×5H2O и 800 г H2O 4) 60 г CuSO4×5H2O и 1 кг H2O
Определите молярную концентрацию раствора, полученного при растворении сульфата натрия массой 42,6 г в воде массой 300 г, если плотность полученного раствора равна 1,12 г/мл
1) 0,98 моль/л 2) 0,98% 3) 41М 4) 0,74
26. Фактор эквивалентности для Al2( SO4)3 равен
1) 0,6 2) 6 3) 1/6 4) 6%
Вычислите, какая масса щавелевой кислоты содержится в 200 мл раствора, если титр его равен 0,0012607 г/мл
|
|
|
1) 0,25214 г 2) 0,4 мг 3) 0,25214 г 4) 4,8 г
Определите молярную концентрацию раствора с массовой долей гидроксида натрия 0,2 и плотностью 1,22 г/мл
1) 0,164 моль/л 2) 3М 3) 8% 4) 6,1 моль/л
29. Метод определения молярной массы растворенного вещества по повышению температуры кипения его раствора называется…
1) эбуллиоскопией 2) экстракцией 3) криоскопией 4) перегонкой
Масса серной кислоты, содержащаяся в 2 л раствора с молярной концентрацией эквивалентов 0,5 моль/л, равна _______ грамма(–ам).
1) 98 2) 24,5 3) 49 4) 196
30. В 250 граммах воды растворен неэлектролит с молярной массой 340 г/моль. Раствор замерзает при – 0,28°С. Масса вещества в растворе составляет _____ грамма(–ов).
1) 45,8 2) 12,8 3) 12800 4) 163,2
31. Односторонняя диффузия молекул растворителя через полупроницаемую мембрану в коллоидный раствор называется …
1) растворением 2) осмотическим давлением 3) осмосом 4) диализом
32. После растворения вещества в растворителе при температуре 20 °С давление насыщенного пара растворителя…
|
|
|
1) Повышается
2) повышается до критического значения, затем понижается
3) понижается
4) не изменяется
33. Смешали 1,6 г метанола (СН3ОН) и 2,7 г дистиллированной воды мольная доля метанола в растворе составляет _____ %.
1) 0,25 2) 3 3) 0,75 4) 1
34. Смешали 200 г раствора глюкозы с массовой долей растворенного вещества 20% и 300 г раствора с массовой долей10 %. Массовая доля в полученном растворе равна___%.
1) 18 2) 14 3) 16 4) 15
35. Осмотическое давление раствора глюкозы с молярной концентрацией 0,1 моль/л при 25 °С равно___кПа.
1) 247,6 2) 51,6 3) 123,8 4) 61,9
36. Гипотоническим раствором по отношению к 0,1% раствору глюкозы является 0,1% раствор …
1) Сахарозы 2) глицерина 3) этанола 4) этиленгликоля
37. Масса воды, необходимая для приготовления 400 г раствора с массовой долей нитрата калия 20% _____ гр.
1) 360 2) 320 3) 80 4) 160
38. Раствор, содержащий 5г вещества (не электролита) в 100 г воды, кипит при 100,43 ° (Кэ=0,52 град кг/моль). Молярная масса вещества равна ____ г/моль.
1) 11 2) 60 3) 0,6 4) 216
|
|
|
39. В 400 г раствора гидроксида натрия с массовой долей растворенного вещества 10% содержится___моль NaOH
1) 1 2) 0,5 3) 0,1 4) 2
Молярная концентрация раствора в 500 мл которого содержится 16 г сульфата меди, равна___моль/л
1) 0,2 2) 0,1 3) 1 4)2
Для приготовления 0,5 л раствора глюкозы с молярной концентрацией 0,2 моль/л, необходимо растворить____гр. вещества
1) 90 2) 9 3) 45 4) 18
42. Растворы, обладающие одинаковым осмотическим давлением, называются…
1) гипотоническими 2) изотермическими
3) гипертоническими 4) изотоническими
Дата добавления: 2019-01-14; просмотров: 637; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
