Теплоемкость, закон Джоуля, уравнение Роберта Майера. Способы измерения теплоемкостей твердых и жидких тел.
Теплоемкость тела или системы - скалярная физическая величина, характеризующая процесс теплообмена и равная количеству тела, полученному системой при изменении его температуры на один кельвин.

ДЖОУЛЯ ЗАКОН - закон термодинамики, согласно к-рому внутренняя энергия идеального газа является ф-цией одной лишь темп-ры и не зависит от объёма. Установлен экспериментально Дж. П. Джоулем в 1845. Д. з. является следствием второго начала термодинамики. Из условия, что приращение энтропии есть полный дифференциал, следует для производной внутр. энергии U по объёму V при пост. темп-ре T:
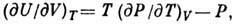
где P - давление. Для идеального газа, удовлетворяющего ур-нию Клапейрона, PV=RT, где R - газовая постоянная,  , это и есть Д. з. Степень справедливости Д. з. для газов малой плотности можно оценить по величине Джоуля-Томсона эффекта. Для идеального газа эффект отсутствует. Д. з. легко получить в кинетич. теории газов: поскольку в идеальном газе отсутствует взаимодействие между молекулами, изменение расстояний между ними (объёма) не меняет внутр. энергии. Д. H. Зубарев.
, это и есть Д. з. Степень справедливости Д. з. для газов малой плотности можно оценить по величине Джоуля-Томсона эффекта. Для идеального газа эффект отсутствует. Д. з. легко получить в кинетич. теории газов: поскольку в идеальном газе отсутствует взаимодействие между молекулами, изменение расстояний между ними (объёма) не меняет внутр. энергии. Д. H. Зубарев.
Для любого идеального газа справедливо соотношение Майера:
 ,
,
где 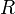 — универсальная газовая постоянная,
— универсальная газовая постоянная,  — молярная теплоёмкость при постоянном давлении,
— молярная теплоёмкость при постоянном давлении, 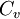 — молярная теплоёмкость при постоянном объёме.
— молярная теплоёмкость при постоянном объёме.
Уравнение Майера вытекает из первого начала термодинамики, примененного к изобарному процессу в идеальном газе:
 ,
,
в рассматриваемом случае:

 .
.
Очевидно, уравнение Майера показывает, что различие теплоёмкостей газа равно работе, совершаемой одним молем идеального газа при изменении его температуры на 1 K, и разъясняет смысл универсальной газовой постоянной 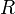 — механический эквивалент теплоты.
— механический эквивалент теплоты.
Теплоемкости жидкостей и твердых тел. Жидкости и твер дые тела в отличие от газов обладают малой сжимаемостью. Поэ тому и жидкостей и твердых тел не имеют столь замет ного различия, как у газов. Например, для железа / =1,02 .
Движение атомов в твердом теле имеет колебательный харак тер. Каждый из них имеет 3 колебательные степени свободы (любое колебание можно представить как сумму трех колебаний, происхо дящих во взаимно перпендикулярных направлениях) . По теореме Больцмана на каждую колебательную степень свободы приходится энергия . Отсюда следует, что на I атом твердого тела приходится энергия 3, а вклад колебательного движения во внутреннюю энергию I моля составляет 3RT . В соот ветствии с определением теплоемкости имеем, что теплоемкость I моля любого твердого тела Это утверждение на зывают законом Дюлонга и Пти.
Измерение теплоемкостей твердых и жидких тел обычно проводится с помощью калориметра, заполненного водой или дру гой жидкостью. Твердое тело известной массы, нагретое до из вестной температуры, быстро переносится из нагревателя в калориметр, отдавая ему некоторое количество теплоты. Измерив после опыта общую для тела и калориметра температуру, зная начальные температуры, массы всех тел и удельные теплоемкости жидкости и материала калориметра, можно вычислить неизвестную теплоемкость твердого тела но уравнению теплового баланса. Этим же методом можно изучать теплоемкость жидкости.
Из теплоемкостей газов непосредственно можно измерить лишь. Для этого некоторую массу газа при определенном по стоянном давлении пропускают через змеевик, погруженный в калориметр. Измеряя температуру газа у входа и выхода змееви ка, зная массу пропущенного газа и повышение температуры в калориметре, можно определить. Экспериментально можно определить и отношение теплоемкостей / , а затем, зная, вычислить .
Б 26
Дата добавления: 2018-11-24; просмотров: 399; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
