Стадия снижения температуры
Постепенное снижение продукции лейкоцитарных пирогенных цитокинов. Причина: уничтожение МО или неинфекционного пирогенного агента. В результате снижение активности ФЛ А2, ЦОГ, и уменьшение выработки Pg, увеличивает порог возбудимости холодовых рецепторов (снижение чувствительности). В результате установочная температурная точка центра терморегуляции снижается.
Разновидности снижения температуры на 3 стадии:
1. Литическая (постепенная)
2. Критическая (быстрая)
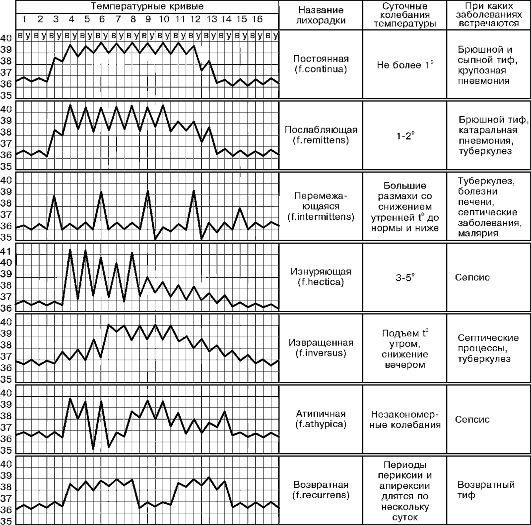
74. Этиология лихорадки. Этиологическая классификация лихорадок. Состояние обмена веществ и физиологических функций в различные стадии лихорадки. Типы температурных кривых. Принципы жаропонижающей терапии. Понятие о пиротерапии.
Этиология лихорадки (полиэтиологична) - в основе развития главная роль отводится пирогенным веществам, они же в свою очередь разделяются на первичные и вторичные (и значение, соотвественно, у них тоже разное). Первичные пирогены – главные факторы развития лихорадки, вторичные – основные звенья ее патогенеза.
Первичные – могут быть инфекционные (или экзогенные, в основном – темостабильные ЛПС мемран бактерий; к ЛПС развивается толерантность, потому что повторном попадании образуется уже меньше цитокинов, которые обладают пирогенной активностью. Экзопирогены могут быть так же представлены некоторыми нуклеиновыми кислотами, белками и полисахаридами некоторых инфекционных возбудителей) и неинфекционными (пирогены тут – продукты распада измененных тканей, как нормально, так и патологически, и лейкоцитов, фрагменты комплимента, иммунные комплексы).
Опираясь на этиологические факторы, мы можем виделить два вида лихорадки, это инфекционная – при острых, хронических заболеваниях, которые вызывают простейшие, бактерии, вирусы, грибки и т.д. и неинфекционная – при наличии очагов асептического воспаления, при наличии некротизированных тканей, внутренних кровоизлияниях, развитии злокачественых опухолей, аллергических заболеваниях, после гемотрансфузий, после операций (и т.д.)
|
|
|
В любом случае, первичные пирогены, не зависимо от природы, не могут перестроить терморегуляцию самостоятельно. Они действуют через вторичные пирогены. То есть, их образование – это основное звено патогенеза в развитии лихорадки, вне зависимости от ее причины.
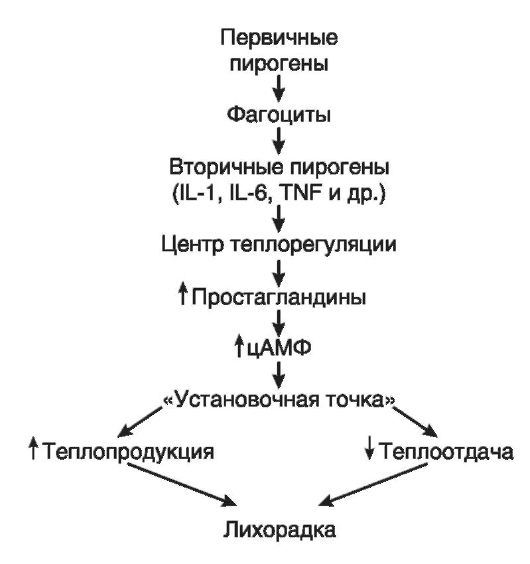 Свойства вторичных пирогенов – IL-1, IL-6, TNG альфа, пирогенным действием послабее обладают интерфероны, катионные белки и гранулоцитарномакрофагальный колониестимулирующий фактор (он же ГМ-КСФ). Где они образуются? Это и фагацитирующие клетки, и эндотелиоциты, и клетки микроглии. Интерферон и TNF альфа образуются в лимфоцитах. Их продукция начинается после их активации после контакта с первичными пирогенами, например, в процессе фагоцитоза микроорганизмов, поврежденных, погибших клеток, продуктов деградации коллагена и фибрина, иммунных комлексов.
Свойства вторичных пирогенов – IL-1, IL-6, TNG альфа, пирогенным действием послабее обладают интерфероны, катионные белки и гранулоцитарномакрофагальный колониестимулирующий фактор (он же ГМ-КСФ). Где они образуются? Это и фагацитирующие клетки, и эндотелиоциты, и клетки микроглии. Интерферон и TNF альфа образуются в лимфоцитах. Их продукция начинается после их активации после контакта с первичными пирогенами, например, в процессе фагоцитоза микроорганизмов, поврежденных, погибших клеток, продуктов деградации коллагена и фибрина, иммунных комлексов.
|
|
|
В основе развития лихорадки – воздействие вторичных пирогенов на центр теплорегуляции (находится он в преоптической зоне гипоталамуса). Образуются простагландины – вопрос, каким механизмом? Скорее всего, вторичные пирогены активируют фосфолипазу А2, которая расщепляет фосфолипиды нейрональных мембран – образуется арахидоновая кислота. Из нее под действием ЦОГ образуются PgE1 и E2,они то и повышают активность аденилатциклазы в центре терморегуляции (повышается образование цАМФ и перестраивается обмен веществ). В итоге получаем: изменение порога чувствительности нейронов как тепловых, так и холодовых к температурным влияниям, set point смещается на более высокий уровень. Данная точка локализуется в той же преоптической области и регулирует пределы колебания температуры в «ядре» тела.
Следовательно, процессы теплоотдачи в организме снижаются, а теплообразование усиливается, тепло избыточно накапливается, температура возрастает до уровня set point. Реализация установочной точки идет через симпатическую нервную систему, эндокринные железы.
|
|
|
Обмен веществ при лихорадке изменяется стремительно – происходят колебания всех видов обмена. Активация окислительных процессов – специфичное для лихорадки изменение. Основной обмен повышается на 10 % на каждое повышение на 1 градус. Потребность в кислороде начинает расти, СО2 в крови снижается.
Изменение углеводного и жирового обмена – возбуждение симпатическаой НС сопровождается усилением распада гликогена и процессов липолиза. В гепатоцитах становится меньше гликогена, следовательно, глюкоза в крови повышается (вплоть до глюкозурии). Жир мобилизируется, повышается его окисление (основной источник энергии у лихорадящих больных, в общем то), что сопрягается в незавершенность окисления ЖК и повышением образование кетоновых тел.
Так же может обнаруживаться отрицательный азотистый баланс. Усиление протеолиза и липолиза, следовательно, ведут к снижению массы тела.
 Происходит так же и изменение водно-солевого обмена. На второй стадии воды и хлорид натрия в тканях начинают задерживаться (потому что секреция альдостерона повышается). На конечной стадии выделение воды и NaCL повышено (как с мочеиспусканием, так и с потоотделением). Хроническая лихорадка же обмен ионов не нарушает. В сыворотке крови мы наблюдаем снижением свободного железа, и, вместе с тем, повышение ферритина. Длительная лихорадка ведет к гипохромной анемии, психологической депрессии и запорам. Белки острой фазы усиленно связывают бивалентные катионы в сыворотке, такие как Cu, Zn так далее. Белки печень синтезирует в повышенно количестве, соответственно.
Происходит так же и изменение водно-солевого обмена. На второй стадии воды и хлорид натрия в тканях начинают задерживаться (потому что секреция альдостерона повышается). На конечной стадии выделение воды и NaCL повышено (как с мочеиспусканием, так и с потоотделением). Хроническая лихорадка же обмен ионов не нарушает. В сыворотке крови мы наблюдаем снижением свободного железа, и, вместе с тем, повышение ферритина. Длительная лихорадка ведет к гипохромной анемии, психологической депрессии и запорам. Белки острой фазы усиленно связывают бивалентные катионы в сыворотке, такие как Cu, Zn так далее. Белки печень синтезирует в повышенно количестве, соответственно.
|
|
|
Наблюдаются сдвиги и кислотно-основного состояния: умеренная лихорадка – развивается газовый алкалоз (из-за гипокапнии), метаболический ацидоз – при лихорадке высокой степени.
Принципы жаропонижающей терапии: полезно или нет применять жаропонижающие средства – нельзя сказать однозначно. Подавление лихорадки может затруднить диагностику заболевания. Хотя положительно лихорадка влияет на течение болезни лишь непродолжительное время. П.Н.Веселкин (!!!)): однозначно вопрос о «пользе» и «вреде» лихорадки решен быть не может. Каждый случай нужно оценивать индивидуально. Показания применения: высокая, продолжительная лихорадка (до 39-40 градусов), умеренная лихорадка у больных ССС, острыми неврологическими расстройствами, наличии шока, сепсиса. Детям младше 5-ти лет и пациентам старческого возраста. Используются НПВС, глюкокортикоиды и т.д.
Пиротерапия – лечение заболеваний искусственно вызванной лихорадкой.
75. 1Лихорадка как часть ответа острой фазы (преиммунного ответа организма). 2Принципиальные отличия лихорадки от экзогенного (высокая температура +повышенная влажность) и эндогенного (цитокины) перегревания. 3Значение лихорадочной реакции в патологии. 4Механизм защитного действия лихорадки.
Лихорадка – компонент цитокин-опосредованного ТПП (преиммунного ответа). Преиммунный ответ наступает в раннюю стадию защиты организма от антигенной агрессии.
1 Ответ острой фазы (или преиммунный ответ) – управляемая цитокинами быстрая координированная перестройка обмена веществ, нейроэндокринной регуляции, функций органов и систем в ответ на любое повреждение еще до выработки специфических АТ и до окончания селекции клонов специфических лимфоцитов. Цель – повысить интенсивность использования энергии, сдержать масштабы альтерации, создать неблагоприятные условия для размножения патогенов, потенцировать действие стрессорных и иммунных элементов защиты.
Клинически: неспецифические проявления, продромальный синдром (общее недомогание). Если слишком много цитокинов – гиперэргическая реакция – шокоподобные состояния, септицемия. Синдром становления болезни, проявляющийся продромальным симптомокомплексом, трактуется как результаты активации гипоталамо-гипофизарно-надпочечниковой системы (=> стресс) и последствий системного эффекта цитокинов, выделяемых при фагоцитозе и воспалении.
Экзогенные пирогенны (экзотоксины, липополисахарид бактерий, АГ) вызывают выработку эндогенных пирогенов (ИЛ-1, ИЛ-6, ФНО) клетками АПК, эндотелием, моно- и полиморфонуклеарами. Эндогенные пирогенны «заставляют» эндотелий вырабатывать PG (медиаторы арахидонового каскада), которые смещают установочную точку температурного гомеостаза выше. PG стимулируют повышенный синтез белков острой фазы (в печени, МФ, эдотелиоцитах), обладающих следующими свойствами:
1. Антиоксидантными (церулоплазмин, С-реактивный белок, амилоид, гаптоглобин, транскоболамин)
2. Антимикробными (С-РБ, лактоферрин, факторы комплемента)
3. Регулирующими гемостаз (факторы коагуляции и антикоагулянты)
2 Лихорадка – ТПП, временное смещение установочной точки температурного гомеостаза на более высокий уровень при сохранении процессов терморегуляции, развивается путем воздействия пирогенов на гипоталамус, и эндогенные пирогены образуются в результате острофазного ответа.
Гипертермия – экстремальный тепловой стресс, способность организма к теплоотдаче становится недостаточной, происходит патологическое повышение температуры, механизмы терморегуляции нарушены.
При лихорадке, в отличие от гипертермии:
· Сохраняются механизмы терморегуляции
· Нет обезвоживания, расстройства кровообращения, гипоксии
Перегревание может развиваться параллельно с лихорадкой, наслаиваясь на нее (как при столбняке).
3 Возникновение и закрепление лихорадки в филогенезе – доказательство ее приспособительного значения. При лихорадке усиливается противоинфекционный иммунитет; ингибируется рост бактерий (опосредованно, через ограничение доступности железа и цинка); увеличивается антигипоксическая резистентность организма; ускоряется фагоцитоз и синтез Ig, ИФН, ИЛ; ускоряется окислительная нейтрализация токсинов.
Платой за это является снижение доставки железа к тканям, анемии, дистрофия скелетных мышц, риск судорог и аритмий, подсыхание слизистой рта (=> стоматиты и ангины), снижение умственной активности, очень опасна при беременности.
4 Лихорадку можно считать частью механизмов врожденного иммунитета, т.к. запуск лихорадки связан с распознаванием клетками ряда облигатных патогенных молекул и молекулярных комплексов, присутствующих у микроорганизмов (экзогенные пирогены). Эндогенные пирогены – цитокины самого организма.
Эффекторные влияния на теплопродукцию осуществляются гипоталамусом через модуляцию кожного кровотока, потоотделения, поведенческие автоматизмы (принятие позы эмбриона), управление сократительным (мышечная дрожь) и несократительным термогенезом (интенсифиация метаболизма за счет активации САС и гиперфункции щитовидной железы).
Мышечная дрожь – автономная реакция на охлаждение кожи или крови, при которой одновременно, ритмично и с большой частотой сокращаются сгибатели и разгибатели. Центр дрожи - в гипоталамусе (в его дорзомедиальной части), он повышает тонус скелетных мышц. Дрожь появляется, если тонус превышает пороговый уровень. Прекращается дрожь при температуре 39,5*С.
Метаболизм активируется под влиянием гормонов надпочечников (катехоламины стимулируют липолиз, гликогенолиз, глюконеогенез) и щитовидной железы (тироксин, трийодтиронин усиливают работу Na-K-АТФазы, способствуют митохондриальному окислению, стимулируют липолиз) и глюкагона. Самый мощный генератор метаболического тепла в организме – бурый жир, митохондрии его адипоцитов содержат белок термогенин (активатор нефосфорилирующего окисления); в клетках бурого жира много норадреналовых рецепторов и симпатических нервных окончаний.
76. Определение понятия «неоплазия». Отличительные особенности опухолевого роста (злокачественная пролиферация, клональный характер, метаплазия, инвазивность). Характеристика морфологической, физико-химической, биохимической анаплазии опухолей. Понятие о прогрессии опухолей.
Неоплазия – синоним понятий «опухолевый рост» или «новообразование». Виллис: «Неоплазия - аномальная масса ткани, рост которой избыточен и не координируется с окружающей нормальной тканью, а также продолжается в той же избыточно-автономной манере после прекращения причины, вызвавшей его». Неоплазия - избыточный, дискоординированный, персистентный, аутохтонный рост клеток, характеризующийся необратимостью, а на молекулярном уровне - расстройством функции генов, регулирующих пролиферативные процессы - протоонкогенов и опухолевых супрессоров. В основе - соматические мутации. Формируется на моноклональной основе. Необходимо накопление нескольких соматических мутаций в разных участках генома, под действием различных мутагенов и в разное время – но в пределах одного и того же клона клеток («многошаговый канцерогенез»). Этиология неоплазии всегда связана с мутагенами. Отличия неоплазии: способность клеток пролиферировать без участия ростовых факторов (автономия, аутохтонность роста), отсутствие у них способности к апоптозу. В патогенезе «опухолевая прогрессия», то есть такая эволюционная дивергенция опухолевого клона, которая увеличивает его разнообразие, выживаемость, резистентность по отношению к действующим в организме факторам отбора. В итоге - быстрое нарастание численности клона и его расселение, включая метастазирование. Принципиально важно, что опухоли, которые в клинике считаются доброкачественными, тоже являются неопластическими, а не гиперпластическими процессами. Злокачественная пролиферация – это рост нормальных клеток, поставленных в условия непрерывного деления.
В патогенезе центральную роль играет аномальная экспрессия онкогенов и синтез кодируемых ими онкобелков, действие которых делает клетки автономными в росте и атипическими по своим метаболическим, генетическим и культуральным свойствам. Обязательно происходит потеря или выключение опухолевых супрессоров - антионкогенов, - что сообщает клеткам потенциальное бессмертие и делает их более мутабельными. Неопластические клоны обычно не способны делиться быстрее, чем нормальные малодифференцированные клетки. Но, т.к. они неспособны к апоптозу и не нуждаются в управляющем сигнале для деления – то без лечения и при неэффективной иммунной защите вытесняют нормальные клоны. Многие признаки морфологического, иммунологического и биохимического атипизма при неоплазии напоминают черты малодифференцированных зародышевых клеток. Наблюдается анаплазия (катаплазия) - утрата признаков дифференцировки или рост без признаков дифференцировки, воспроизводящий, в силу использования эмбриональных росторегулирующих программ, отдельные свойства незрелых клеткам. Иммунологический атипизм – в экспрессии АГ, несвойственных нормальным клеткам, снижении количества АГ ГКГС I класса и появлении активирующих NK-клетки MIC-молекул на поверхности. Биохимический атипизм – в отсутствии эффекта Пастера, преобладании анаэробного гликолиза над аэробными процессами, тенденции к гипогликемии. На тканевом уровне атипизм выражается в снижении адгезивных способностей клеток, нарушении их прикрепления к элементам межклеточного вещества, например, вследствие необратимого фосфорилирования цитоскелетных белков. Неопластические эпителиальные клетки не образуют базальных мембран и не прикрепляются к ним, утрачивая кроющую функцию. Отсоединение от тканевого матрикса не вызывает. Неоплазмы выделяют цитокины, обусловливающие их аномальную васкуляризацию, но при злокачественном характере они лишены иннервации и имеют запустевшие лимфатические сосуды. Атипизм в культуральных свойствах: in vitro ослабление адгезивности и отсутствие контактного торможения роста, клетки не распластываются на твёрдом субстрате и могут размножаться, будучи взвешенными в полужидкой среде, не требуют факторов роста, потенциально бессмертны в культуре. Нарушение нормального клеточного цикла деления и превышение темпов размножения над темпами гибели клеток лежит в основе развития злокачественных опухолей. Разные стадии клеточного цикла контролируются различными стартующими генами, последовательность включения которых обеспечивается их взаимодействием между собой. Контрольные точки в процессе митотического цикла – пункты, где клетка проверяет целостность генома и отсутствие мутаций, в этих точках цикл может быть прерван и переключен на апоптоз. Описан ферментативный механизм (работа фосфорилируемых циклин-зависимых киназ) продолжения клеточного деления при нормальном состоянии генома. Циклины – белки, переключающие фазы митоза, они периодически деградируют в ходе клеточного цикла. Протонкогены и антионкогены регулируют эти процессы, а при неоплазии мутации нарушают их взаимодействие.
Метаплазия – аномалия дифференцировки клеток органа (ткани): камбиальные клетки дифференцируются в нехарактерные для данного органа зрелые. Метаплазия обратима, клетки не проявляют нарушения нормальных межклеточных взаимоотношений (нет признаков тканевого атипизма). Одна дифференцированная ткань превращается в другую под влиянием изменившихся условий, например, в ходе воспаления. Метапластические клетки чувствительны к регуляторным сигналам, возникают из камбиальных элементов, а не путём изменения фенотипа зрелых клеток. Метаплазия только в пределах тканей одного вида (эпителий -> эпителий). Обычно нет прямой связи между мета- и неоплазией, но в метапластических участках могут появляться признаки дисплазии – аномалии как дифференцировки, так и созревания – тогда риск возникновения онкологии повышен. Метаплазия возможна на фоне неоплазии – превращение части клеток опухолей (тоти-, плюрипотентных) в зрелые клетки разной тканевой принадлежности.
Злокачественные опухоли растут инвазивно (то есть, с прорастанием и замещением окружающих тканей, по путям наименьшего механического сопротивления) и метастазируют (т.е. дают аутотрансплантаты на удалении от места первичной локализации).
Классификация опухолей: из прогаметных тотипотентных клеток, из эмбриональных полипотентных (стволовых) клеток (из элементов органных зачатков - эмбриомы или бластомы), из дифференцированных клеток, утративших часть или все признаки дифференцировки и подвергшихся анаплазии.
77. Функциональные, метаболические и антигенные свойства малигнизированных клеток. Нарушение обмена веществ в организме с опухолевым ростом. Механизмы инфильтративного роста опухолей. Виды и механизмы метастазирования. Исходы метастазов.
Опухоль, новообразование (лат. tumor, греч. neoplasma) - патологическая неконтролируемая организмом пролиферация клеток с относительной автономией обмена веществ и существенными различиями в строении и свойствах.
Опухоль представляет собой местное проявление заболевания всего организма. Различают опухоли доброкачественные и злокачественные.
Доброкачественные опухоли растут, сдавливая и раздвигая ткани (экспансивный рост), и, если не препятствуют своей локализацией и массой функционированию жизненно важных органов, обычно не приводят к смертельному исходу.
Злокачественные опухоли прорастают, инфильтрируют окружающие ткани (инвазивность), разрушая их (деструктивный рост), нередко метастазируют в регионарные лимфатические пути и вызывают истощение организма - кахексию. Кахексия - результат системного действия злокачественной опухоли, которая может привести к смерти даже при отсутствии метастазов из-за расстройства метаболизма и деятельности различных физиологических систем, а также дистрофии жизненно важных органов.
Дата добавления: 2016-01-04; просмотров: 35; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
