Multicomponent Natural Gas Systems
In Figure 4.2c for natural gases without a liquid hydrocarbon (or when liquid
hydrocarbons exist below 273 K), the lower portion of the pressure–temperature
phase diagram is very similar to that shown in Figure 4.2a. Two changes are
(1) the LW–H–V line would be for a fixed composition mixture of hydrocarbons
rather than for pure methane (predictions methods for mixtures are given in
Section 4.2 and in Chapter 5) and (2) quadruple point Q1 would be at the
intersection of the LW–H–V line and 273 K, at a pressure lower than that for
methane. The other three-phase lines of Figure 4.2a (for I–LW–H and I–H–V)
have almost the same slope at Q1. Otherwise, the same points in Section 4.1.1
apply.
However, for the case in which natural gases contain heavier components, the
upper portion of the diagram is more like that shown in Figure 4.2b. A straight
line labeled LW–H–V represents the hydrate formation region equivalent to the
region between quadruple point Q1 (I–LW–H–V) and the upper quadruple point
Q2 (LW–H–V–LHC) in Figure 4.2b. One significant change in Figure 4.2c is that
quadruple point Q2 becomes a line, as indicated in the next paragraph.
When a liquid hydrocarbon mixture is present, the LW–V–LHC line in
Figure 4.2b broadens to become an area, such as that labeled CFK in Figure 4.2c.
This area is caused by the fact that a single hydrocarbon is no longer present, so
a combination of hydrocarbon (and water) vapor pressures creates a broader phase
equilibrium envelope. Consequently, the upper quadruple point (Q2) evolves into
a line (KC) for the multicomponent hydrocarbon system.
Line KC may not be straight in the four-phase region but is drawn that way
for illustration. The location of the lower point K is determined by the intersection
point of the phase envelope ECFKL with the LW–H–V line, determined
by the methods of Section 4.2 or Chapter 5. To determine the upper point C,
first a vapor–liquid equilibrium calculation is performed, assuming the liquid
phase (exiting the envelope at point C) equals the vapor composition at point K.
That liquid is used to calculate a vapor composition which is used in a vapor–
liquid water–hydrate calculation to determine the upper intersection with the phase
envelope ECFKL.Amore thorough treatment of the calculation of multicomponent
equilibrium with a condensed hydrocarbon phase is given in Sections 4.3.2.
|
|
|
На основе измерения значений энтальпии на участке ID (плавление льда) и полученных ранее данных удельной теплоты плавления льда была определена доля воды в гидрате и во льду (как показано на рис. 7а).
Гидраты смесей углеводородных и неуглеводородных компонентов.
Результаты исследования термических параметров состояния системы вода (лёд) – гидрат (sI, sII) – газовая смесь.
Далее представлены результаты измерения термических и калорических параметров состояния системы вода (лёд) – гидрат (sI, sII) – шестикомпонентная смесь, моделирующая пластовый флюид Ботуобинской залежи Чаяндинского нефтегазоконденсатного месторождения, а также построенные на основе этих данных фазовые диаграммы этой системы.
Кривые равновесия фаз вода (лёд) – гидрат (sI, sII) – газовая смесь
Измерение фазовой диаграммы для модельной смеси проводилось в соответствии с методикой ГСССД [1]. При построении кривых равновесия фаз использовался факт аномального поведения термодинамической системы и её термодинамических параметров при фазовых переходах. Так, при нагревании вещества теплоёмкость испытывает скачок при температуре перехода из одной фазы в другую (например, при пересечении пограничной кривой из двухфазного состояния в однофазное). Зависимость давления от температуры также испытывает излом (в производной также будет скачок). По этим аномалиям и определяются температура и давление на кривой фазовых равновесий исследуемой системы [1].
|
|
|
Кривые фазовых равновесий вода - гидрат – шестикомпонентная газовая смесь, а также лёд – гидрат – шестикомпонентная газовая смесь были измерены как в процессе образования, так и разложения гидратов. Равновесные значения кривых фазовых равновесий в процессе образования и разложения гидратов изо льда, а также в процессе образования из переохлаждённой воды определялись в режиме релаксации.
Фазовое поведение модельной шестикомпонентной смеси при термобарических условиях возможного гидратообразования, как уже было показано в предыдущем разделе, носит достаточно сложный характер. Термобарическая область существования газогидратов распадается на ряд областей существования гидратов различных структур. Перевод системы из одной области в другую сопровождается структурными фазовыми переходами. На основе проведенных экспериментов получены фазовые диаграммы области существования газовых гидратов различных структур, а также выделена область безгидратного состояния системы.
|
|
|
На рис. 13 представлены результаты измерения фазовой диаграммы системы вода (лёд) – гидрат (sI, sII) – газовая смесь в водонасыщенной пористой среде в области гидратообразования.
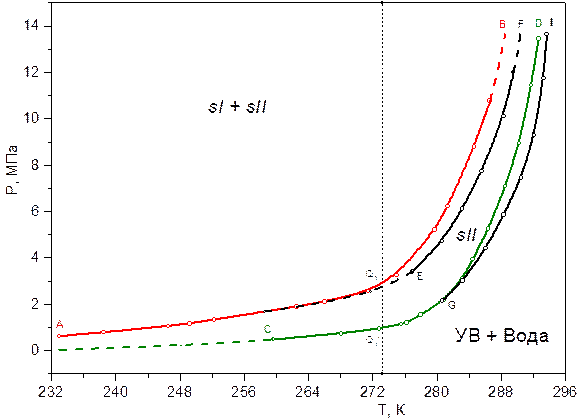
Рис. 13. Фазовая диаграмма системы вода (лёд) - модельная шестикомпонентная смесь в термобарической области возможного гидратообразования во всём исследованном диапазоне.
Линия АВ на рис. 13 соответствует равновесию вода (лёд) – гидрат sI - шестикомпонентная газовая смесь. Линия СD соответствует равновесию вода (лёд) – гидрат sII - шестикомпонентная газовая смесь.
Для сравнения и последующего анализа на рис. 14 представлены фазовые диаграммы системы вода (лёд) – индивидуальные углеводороды (метан, этан, пропан) в термобарической области возможного гидратообразования.
Как уже было отмечено ранее, термическая предыстория воды предопределяет характер процесса образования гидратных структур исследованной нами шестикомпонентной газовой смеси (sI, sII, метастабильные структуры).
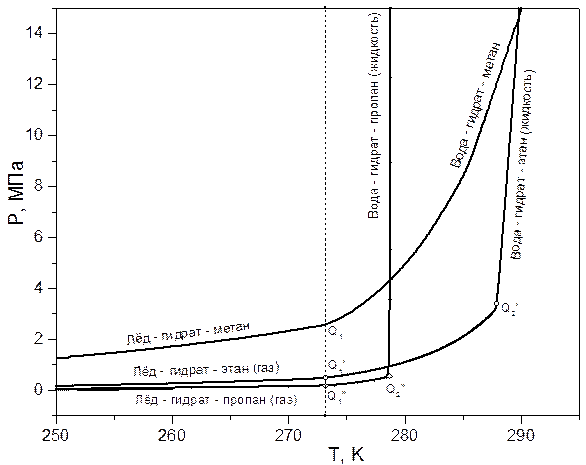
Рис. 14. Фазовые диаграммы системы вода (лёд) – индивидуальные углеводороды (метан, этан, пропан) в термобарической области возможного гидратообразования
|
|
|
В случае свежей воды из метастабильного состояния системы вода – модельная смесь формируются две структуры (sI, sII). Этим структурам соответствуют линии АВ и СД на рис. 13, а также точки E1 и F1 на рис. 8.
В случае воды расплавленного гидрата из метастабильного состояния системы вода – модельная смесь также формируются структура гидрата sI. Однако линия, соответствующая структуре sII расщепляется на две. Этим структурам соответствуют линии EF и GI на рис. 13 и 14 а также точки F’2 и F”2 рис. 8.
Следует подчеркнуть, что на рис. 13 и 15 линии фазовых равновесий представляют проекции измерений более высокого порядка, сжатые в двухмерное давление – температура представление.
Гидраты природных углеводородных газов.
Дата добавления: 2018-10-26; просмотров: 237; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
