Реакции обнаружения соединений мышьяка.
а) Реакции обнаружения мышьяка основаны на восстановлении мышьяка до арсина с дальнейшим обнаружением его методами Марша, Гутцайта и Зангер-Блека:
As2O3 + 6Zn + 6H2SO4 ® 2AsH3↑ + 6ZnSO4 + 3H2O
Метод Марша :
2AsH3  2As¯ + 3H2↑
2As¯ + 3H2↑
Образуется серо-черный налет с металлическим блеском – «мышьяковое зеркало».
Метод Гутцайта :
AsH3 + 6AgNO3 ® Ag3As∙3AgNO3¯ + 3HNO3
желтое пятно на фильтровальной бумаге
Ag3As∙3AgNO3 + 3H2O ® 6Ag¯ + H3AsO3 + 3HNO3
черное пятно на фильтровальной бумаге
Метод Зангер-Блека:
2AsH3 + 3HgCl2 ® Hg3As2¯ + 6HCl
желтое пятно на фильтровальной бумаге
б) Реакция с сульфидами (фармакопейная реакция):
2AsCl3 + 3H2S ® As2S3¯ + 6HCl
желтый
2AsCl5 + 5H2S ® As2S5¯ + 10HCl
желтый
в) Сульфиды в сильнокислой среде образуют с солями мышьяка осадки As2S3 и As2S5 желтого цвета, которые не растворяются в концентрированной НС1, но растворимы в растворах Na2S, (NH4)2S, (NH4)2CO3 и аммиака:
As2S3 + 3Na2S ® 2Na3AsS3
тиоарсенит натрия
As2S5 + 3Na2S ® 2Na3AsS4
тиоарсенат натрия
г) Реакция с магнезиальной смесью (MgSO4 + NH3 + NH4Cl):
Арсенат-ионы в растворах образуют белый кристаллический осадок арсената аммония магния, растворимый в хлороводородной кислоте:
|
|
|
HAsO42- + Mg2+ + NH3 ® NH4MgAsO4¯
MgNH4AsO4 + 3HCl ® MgCl2 + NH4Cl + H3AsO4
Реакции обнаружения соединений сурьмы.
а) Соли сурьмы(III) в слабокислых растворах легко гидролизуются, при этом выпадают осадки белого цвета:
SbCl3 + H2O ® SbOCl¯ + 2HCl
б) Тиосульфат натрия Na2S2O3 образует в кислых растворах с солями сурьмы (III) оранжево-красный осадок Sb2OS2:
2SbCl3 + 2Na2S2O3 + 3H2O ® Sb2OS2¯ + 2Na2SO4 + 6HCl
в) Сероводород образует с солями сурьмы в кислой среде ярко-оранжевые осадки Sb2S3 и Sb2S5, растворимые в избытке Na2S с образованием тиосолей:
2SbCl3 + 3H2S ® Sb2S3¯ + 6HCl
Sb2S3 + 3Na2S ® 2Na3SbS3
тиоантимонит натрия
2H[SbCl6] + 5H2S ® Sb2S5¯ + 12HCl
Sb2S5 + 3Na2S ® 2Na3SbS4
тиоантимонат натрия
Реакции обнаружения соединений висмута.
Для качественного обнаружения соединений висмута используются осадочные реакции:
а) с йодидом калия образуется черный осадок BiI3, растворимый в избытке реактива с образованием комплексной соли – тетрайодовисмутата (III) калия:
Bi3+ + 3I- ® BiI3¯
BiI3 + KI ® K[BiI4]
б) с сульфидами (фармакопейная реакция) соли висмута (III) образуют коричнево-черный осадок Bi2S3, нерастворимый в разбавленных кислотах, кроме азотной кислоты:
|
|
|
2Bi3+ + 3S2-® Bi2S3¯
Bi2S3 + 8HNO3 ® 2Bi(NO3)3 + 2NO + 3S + 4H2O
Тема IV. p-Элементы VI группы: кислород. Озон, вода, пероксид водорода
Биологическая роль кислорода, озона, воды
Кислород. Кислород входит в состав всех жизненно важных органических веществ – белков, жиров, углеводов. При участии кислорода осуществляется один из важнейших жизненных процессов – дыхание, благодаря которому идет непрерывное поступление кислорода к тканям. Человек вдыхает и выдыхает в сутки 20-30 м3 воздуха. Потребность человека в кислороде в покое составляет 25 л/ч. Если концентрация кислорода в воздухе снижается до 9% – это представляет угрозу для жизни. У человека и высших животных кислород, проникая в кровь, соединяется с гемоглобином, образуя оксигемоглобин:
HbFe2+ + O2 « HbFe2+∙O2
Через стенки капилляров кислород поступает в клетки, где расходуется на окисление различных веществ (жиров, углеводов, белков и др.), в результате этих процессов образуется СО2 и Н2О, выделяется энергия, обеспечивающая жизнедеятельность живых организмов.
HbO2 ® Hb + O2
В митохондриях атомы водорода, отщепленные в виде Н+ от субстрата под действием фермента дегидрогеназы, связываются с кислородом:
|
|
|
4H+ + O2 + 4e- ® 2H2O
В природе у зеленых растений на свету идет процесс фотосинтеза, при котором поглощается СО2 и выделяется молекулярный кислород О2:
хлорофилл
6nCО2 + 5nН2О  (С6Н10О5)n + 6nО2
(С6Н10О5)n + 6nО2
свет
Озон. Аллотропное видоизменение кислорода – озон – на высоте 25 км над уровнем земли образует озоновый слой, который поглощает жесткое ультрафиолетовое излучение (l≤ 260 нм). Разрушение озонового слоя может привести к гибели живых организмов на Земле.
Вода. В организме взрослого человека массовая доля воды составляет 65%. Благодаря своему строению вода, является универсальным растворителем, практически все химические реакции в организме человека осуществляются в воде, жизнь без воды невозможна. Вода является одновременно средой и участником реакций гидролиза жиров, АДФ и АТФ:
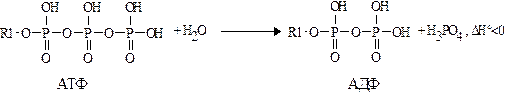
При гидролизе в первую очередь разрывается связь 1, затем 2. При этом выделяется энергия, используемая организмом. Большая часть воды (около 70%) находится внутри клеток в протоплазме. Остальная часть воды (около 30%) – это внеклеточная вода, которая образует плазму крови и межтканевую воду.
|
|
|
Дата добавления: 2018-09-20; просмотров: 1187; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
