Сумма кинетической и потенциальной энергии тел, составляющих замкнутую систему и взаимодействующих между собой посредством сил тяготения и сил упругости, остается неизменной.
Билет № 9
Перечислите основные положения молекулярно-кинетической теории и приведите примеры их экспериментального доказательства. Дайте определение идеального газа. Сформулируйте основное уравнение МКТ идеального газа. Дайте определение абсолютной температуры как меры средней кинетической энергии движения молекул.
Молекулярно-кинетическая теория (МКТ) – это учение, которое объясняет тепловые явления в макроскопических телах и внутренние свойства этих тел движением и взаимодействием атомов, молекул и ионов, из которых состоят тела. В основе МКТ строения вещества лежат три положения:
- Вещество состоит из частиц – молекул, атомов и ионов.
- Частицы, из которых состоит вещество, находятся в непрерывном хаотическом (беспорядочном) движении.
- Частицы вещества взаимодействуют друг с другом – притягиваются и отталкиваются.
Эти основные положения подтверждаются экспериментально и теоретически.
- Доказательствами первого положения являются: наблюдение молекул в электронный микроскоп, испарение, растворение, дробление веществ.
- Доказательствами второго положения являются: диффузия (процесс взаимного проникновения молекул или атомов одного вещества между молекулами или атомами другого вещества),
Броуновское движение (беспорядочное движение микроскопических видимых взвешенных в жидкости или газе частиц твердого вещества),
Давление газов.
- Доказательством третьего положения является сопротивляемость тел упругой деформации.
ИДЕА́ЛЬНЫЙ ГАЗ - теоретическая модель газа; в которой пренебрегают размерами частиц газа, не учитывают силы взаимодействия между частицами газа, предполагая, что средняя кинетическая энергия частиц много больше энергии их взаимодействия, и считают, что столкновения частиц газа между собой и со стенками сосуда абсолютно упругие.
Предельную температуру, при которой давление идеального газа обращается в нуль при фиксированном объеме или при которой объем идеального газа стремится к нулю при неизменном давлении, называют абсолютным нулем температуры. Это самая низкая температура в природе, та «наибольшая или последняя степень холода», существование которой предсказывал Ломоносов.
Абсолютная шкала температур. Английский ученый У. Кельвин (1824-1907) ввел абсолютную шкалу температур. Нулевая температура по абсолютной шкале (ее называют также шкалой Кельвина) соответствует абсолютному нулю, а каждая единица температуры по этой шкале равна градусу по шкале Цельсия.
Единица абсолютной температуры в СИ называется Кельвином (обозначается буквой К).
Один кельвин и один градус шкалы Цельсия совпадают. Поэтому любое значение абсолютной температуры T будет на 273 градуса выше соответствующей температуры t по Цельсию
Т= t +273, К
Но изменение абсолютной температуры 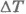 равно изменению температуры по шкале Цельсия
равно изменению температуры по шкале Цельсия 
 .
.
Абсолютному нулю соответствует температура t = -273,15 °С.
Абсолютный нуль температуры недостижим!
Абсолютная температура есть мера средней кинетической энергии движения молекул.

Средняя кинетическая энергия хаотичного поступательного движения молекул газа пропорциональна абсолютной температуре. Чем выше температура, тем быстрее движутся молекулы.
Газы в технике, применяются главным образом в качестве топлива; сырья для химической промышленности: химических агентов при сварке, газовой химико-термической обработке металлов, создании инертной или специальной атмосферы, в некоторых биохимических процессах и др.; теплоносителей; рабочего тела для выполнения механической работы (огнестрельное оружие, реактивные двигатели и снаряды, газовые турбины, парогазовые установки, пневмотранспорт и др.): физической среды для газового разряда (в газоразрядных трубках и др. приборах). В технике используется свыше 30 различных газов.
Билет №10
Дата добавления: 2018-06-01; просмотров: 399; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
