Лабораторная работа № 4. Диагностика галогенидов.
К галогенидам относятся соединения Cl, F, Br и I главным образом со щелочными и щелочно-земельными элементами. Всего известно около 100 минералов этого типа соединений. Ведущими катионами хлоридов являются литофильные элементы - Nа, К, Мg. Для фторидов это также литофильные элементы, но на первое место среди них выходит Са, затем Na, Al, Mg. Подавляющее большинство фторидов являются безводными минералами. Наибольшее распространение имеют соединения Cl и F. Соединения Br и I самостоятельных минералов практически не образуют и встречаются чрезвычайно редко.
В галогенидах простого состава преобладают связи ионного типа и координационные изодесмические структуры. Изоморфные замещения в большинстве галогенидов ограничены и только в высокотемпературных фторидах они проявляются иногда широко (флюорит).
Иногда галогениды известны в виде изометричных кристаллов, щеток, а также сплошных плотных масс разной степени зернистости до гигантозернистых. Для многих из них характерны также налеты, выцветы, возгоны. Основная масса галогенидов бесцветна или имеет белый цвет с сероватым или желтоватым оттенком. Окраска галогенидов возникает либо за счет дефектов их кристаллической решетки, либо за счет механических примесей.
Хлориды литофильных элементов хорошо растворимы в воде, тогда как фториды - не растворимы. Большая часть галогенидов имеет стеклянный блеск и низкую до средней твердость. Они часто прозрачны, для них обычна совершенная спайность.
|
|
|
Хлориды литофильных элементов, будучи хорошо растворимы, практически не встречаются в гипогенных ассоциациях. Они накапливаются в морской воде и при ее упаривании могут образовывать крупные хемогенные месторождения.
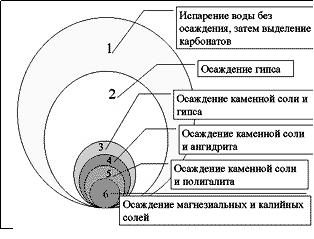
Выделение их в этом случае происхо-дит сразу же вслед за выделением карбонатов и гипса в следующей последовательности: карбонаты - гипс (ангидрит) - галит + гипс - галит + ангидрит - галит + полигалит (K2Ca2Mg[SO4]4·2H2O ) - Мg и К - хлориды , причем характер ассоциаций определяется в первую очередь температурой кристалл-лизации. Кристаллизация хлоридов может происходить и из замкнутых водоемов. В этом случае в ассоциации с ними обычны мирабилит (или тенардит), бораты, нитраты.
Подавляющая масса фторидов - гипогенные минералы. Они известны в магматических породах, где встречаются в качестве акцессорных минералов, пегматитах,
грейзенах и гидротермальных жилах. Во всех этих процессах образуется флюорит. В процессе выветривания фтор редко достигает морских бассейнов и обычно связывается во флюорит (ратовкит).
 В процессе метаморфизма основная масса галогенидов неустойчива, исключение составляет флюорит. Галогены рассеиваются в галогенсодержащих силикатах (амфиболы, слюды и многие другие).
В процессе метаморфизма основная масса галогенидов неустойчива, исключение составляет флюорит. Галогены рассеиваются в галогенсодержащих силикатах (амфиболы, слюды и многие другие).
|
|
|
Рис.34. Схема последовательности осаждения солей при выпаривании морской воды
Некоторые галогениды, накапливаясь в больших количествах, представляют промышленный интерес. Это прежде всего галит, сильвин, флюорит. Галит и сильвин являются сырьем для химической промышленности. Основная масса галита используатся в пищевой промышленности. Сильвин служит в качестве агрохимического сырья. Флюорит используется в технологическом процессе выплавки алюминия из глинозема, а также является источником редких земель. Прозрачные кристаллы флюорита находят применение в оптике.
Галогениды зоны гипергенеза принадлежат к числу редких и мало изученных минералов. В большей степени распространены хлориды, характерные для окисленных руд свинцовых, медных, висмутовых и ртутных месторождений. Фториды в виде фтороалюминатов (галогеносолей) в основном Ca, реже Sr и редких земель типичны для сравнительно поздних этапов формирования зоны гипергенеза флюоритсодержащих месторождений. Флюорит обычно упоминается в качестве источника фтора. Наиболее редкими являются йодиды и бромиды, йод связан главным образом с серебром.
|
|
|
Общее число галогенидов, соотносящихся с зоной гипергенеза рудных месторождений, около 75. За последнее десятилетие в этом классе было обнаружено 15 новых минералов, найденных в окисленных рудах. За счет этих находок существенно расширился список соединений Pb (грандрифит, пиналит и др. ) и Hg (кузьминит, кадырэлит и др.).
Среди известных галогенидов зоны гипергенеза около 1/3 минералов приходится на хлориды свинца. На втором месте по числу минеральных видов стоят хлориды Сu и Hg.
В составе галоидных соединений нередко содержится вода (в виде ОН и Н2О), а также добавочные анионы (О, SO4, NО3, S). Некоторые среди новых минералов принадлежат к галогенидсульфидным соединениям (лаврентьевит, арзакит).
Галоидные соединения в составе окисленных руд, представлены рядами ведущих катионов (Рb, Сu, Ag, Hg, Co, Ni, Sn, Ca). Внутри рядов выделены группы с учетом содержания в составе минералов добавочных анионов и воды. В соответствии с предложениями по систематике галогенидов (Годовиков, 1984) галоидные соединения Ca и Sr обособлены в группу фторалюминатов.
Находки галогенидов в зонах гипергенеза служат показателем аридных, в том числе и криогенных, условий их формирования.
|
|
|
Соединения Рb могут быть отнесены к шести основным группам.
1. Группа минералов, близких по составу к котунниту (PbCl2) с заменой Cl на F и ОН, – котунит, лорелит, матлокит, лаурионит, бликсит и фидлерит. Это белые или слабо-зеленоватые галогениды, которые в виде кристаллических корочек выделяются на англезите, церуссите, фосгените. Кристаллы их таблитчатые или игольчатые с алмазным блеском. Известны в таких месторождениях, как Маммот и Аравайпа в шт. Аризона (США), Лаврион (Греция), Матлок (Великобритания) и некоторые чилийские рудники, Надор в Алжире.
2. Более сложные по составу оксигалогениды Рb с добавочным кислородным анионом представлены мендипитом и паркинсонитом, для которых характерны белые с желтоватым, иногда с медовым оттенком и алмазным блеском призматические кристаллы, а также корочки, желваки и прожилки.
Группа оксихлоридов Pb с Sb, As и Bi – надорит, экдемит, гелиофиллит и перит, – принадлежит к числу очень редких образований зоны гипергенеза (рудник Маммот в шт. Аризона, США; месторождение Надор в Алжире). Для них типичны тонкие корочки из желтых и красно-коричневых таблитчатых кристаллов и розетковидные агрегаты. Экдемит и гелиофиллит диморфны. Отлагаясь обычно на вульфените, они нередко прорастают друг друга. Перит обнаружен на месторождении Караоба (Ц. Казахстан) в виде массивных агрегатов замещающих сульфиды Bi. Ассоциируется с ярозитом и штольцитом. В первоисточнике данных о содержании воды в минерале нет, но формула дается в виде Pb2+Bi3+Cl(OH)4. Указана примесь СО2 (до 1,5%).
Гидроксидхлориды свинца и одновременно меди, а также олова: перцилит, диаболеит, хлороксифит и куменгит. Эти минералы яркой синей окраски обнаружены в ассоциации с церусситом, вульфенитом, смитсонитом и болеитом в окисленных рудах ряда мексиканских и чилийских месторождений и рудника Маммот в США. Отдельно следует отметить абхурит (бесцветные, хрупкие шестигранные таблички) – возможный продукт рудного гипергенеза, обнаруженный на поверхности оловянного слитка, пролежавшего на дне Красного моря после кораблекрушения около 100 лет.
5. Гидроксидхлориды Рb с Сu, Ag и Cr – болеит (темно-синие псевдокубические кристаллы со спайностью по (101), твердостью 3,5–4 в ассоциации с фосгенитом, атакамитом, церусситом), бидоит (корочки из белых изометричных кристаллов, чаще на болейте) и йедлинит (красно-фиолетовые призматические кристаллы в ассоциации с диаболеитом, вульфенитом и бидоитом) – редкие минералы в окисленных рудах Мексики (Болео и др.) и Чили.
6. Оксихлориды Рb с добавочными анионами (SО4 и IO3) – недавно обнаруженный сундиусит (бесцветные перистые агрегаты с твердостью 3 в ассоциации с гидроцерусситом и мендипитом в Лонгбане, Швеция) и зеелигерит, найденный в чилийских месторождениях в срастании с болеитом в виде желтых таблитчатых кристаллов. На месторождении Гранд-Риф и Маммот (округ Пинал, рудник Аравайпа шт. Аризона, США) обнаружена большая группа хлоридов и фторидов Pb с добавочными анионами (SO4, CO3, WO4): пиналит, барстоуит, грандрифит, псевдограндрифит и аравайпаит, ассоциирующихся с ледхиллитом, матлокитом, церусситом, диаболеитом. Эти минералы ярко-желтые, оранжевые, чаще игольчатые, с алмазным блеском.
Среди соединений Bi более распространен бисмоклит, образующийся в виде псевдоморфоз по висмутину или землистых сферолитовых агрегатов серой окраски. Отмечается в зоне окисления месторождения Караоба (Казахстан). Очень редкий заварицкит, известный среди продуктов окисления висмутина Шерловой Горы, и добреит, отмеченный в боливийских месторождениях. Оба серовато-белые, в виде землистых корочек, похожие на бисмоклит.
Галогениды Сu по особенностям химического состава могут быть разделены на три группы:
1. Простые галогениды меди, в основном хлориды, без молекулярной воды – нантокит, маршит, атакамит и параатакамит. Первые два минерала белые или слегка желтоватые, в виде зернистых корочек на лимоните, псиломелане. Известны в Гайском месторождении (Урал), в чилийских (Нантоко и др.) и австралийских (Брокен-Хилл) месторождениях. Более распространен атакамит. Для него типичны зеленые сферические и почковидные агрегаты в ассоциации с гипсом, формирующиеся на куприте, самородной меди, малахите, брошантите. Минерал обнаружен не только в зарубежных (Чили, Перу, Мексика) медных рудниках, но и в ряде месторождений бывшего СССР – Урала (Меднорудянское и Турьинское), Казахстана, Рудного Алтая, Средней Азии (Витовская, 1962; Голованов, 1965; Ермилова, 1964; Чухров, 1950). Характерен для средних стадий развития зоны окисления, формирующейся в условиях аридного климата. Параатакамит содержит помимо меди до 16% Zn. Обнаружен в руднике Герминия в Чили в ассоциации с атакамитом. Имеет сходство не только с атакамитом, но и брошантитом, либетенитом и пироморфитом;
2. Группа медных (реже цинковых) хлоридов, содержащих молекулярную воду, – кальюметит, антониит, кларингбуллит и симонколлеит. Первые два минерала очень редкие, описанные в окисленных рудах медных месторождений шт. Мичиган (США). Кальюметит лазурно-голубой, антониит лиловый. Ассоциируютcя с малахитом, атакамитом, купритом. Кларингбуллит голубой, в виде пластинчатых кристаллов со спайностью. Найден в месторождениях Нчанга (Замбия) и Мсеса (Заир) вместе с брошантитом, малахитом и купритом. Симонколлеит (Zn-хлорид) обнаружен среди продуктов окисления древних шлаков в горах Рихельсдорф (Германия) в ассоциации с церусситом, диаболеитом и гидроцинкитом в виде бесцветных таблитчатых кристалликов с твердостью 1–1,5;
3. Хлориды меди с добавочными анионами – хлоротионит, арцрунит и буттгенбахит. Это ярко-синие, игольчатые, иногда тонковолокнистые агрегаты на куприте, малахите и брошантите. Известны из медных месторождений Заира (Ликази и др.). Изучены очень слабо.
Соединения Ag представлены хлоридами, бромидами и йодидами. Хлораргирит (кераргирит), бромаргирит и промежуточный член в этом изоморфном ряду кубических галогенидов – эмболит – в ассоциации с малахитом, англезитом, ярозитом, церусситом, деклуазитом, ванадинитом, гидрогётитом выделяются в виде восковидных корочек, пленок, дендритов и псевдоморфоз по различным серебряным минералам. Минералы ковкие, с большой плотностью. Окраска серая, на свету переходит в серо-фиолетовую. Указываются в месторождениях Казахстана (Джеламбет, Майкаин и др.), Средней Азии (Кургашинкан), Мексики. Йодаргирит описан из месторождения Майкаин, где выделяется среди ярозита с серой и другими самородными элементами, а также на лимоните как более поздняя генерация. Майерсит и купройодаргирит (медьсодержащие йодиды) отмечаются в Чукикамате (Чили) и Брокен-Хилле. (Австралия). Оба желтые (особенно яркий – майерсит) с алмазным блеском, в форме восковидных корочек на сульфидах и на лимонит-ярозитовых агрегатах.
Галоидные соединения Fe, Co и Ni представлены шестиводными хлоридами этих элементов. Гидромолизит (Fe) описан в смеси с гипсом и галитом в составе оранжево-красной корки на магнетите железорудного месторождения Эльбы. Албриттонит (Со) и никельбишофит (Ni) найдены в серпентинитовом карьере Оксфорд (шт. Техас, США) в виде продуктов окисления кобальтина, никелина и зигенита в ассоциации с эритрином, заратитом и аннабергитом. Типичны кристаллические корочки и налеты. Твердость минералов около 1,5. Албриттонит сиренево-красный, никельбишофит изумрудно-зеленый. Оба со спайностью, полупрозрачные.
Среди галогенидов Hg много минералов, обнаруженных в ртутных месторождениях России. Более известна каломель – хлорид белого цвета, характерный для зоны гипергенеза таких киноварных месторождений, как Никитовка (Украина), Кубадру (Алтай), Келянское (Бурятия). Иногда каломель отлагается на эглестоните – оранжевом оксихлориде, с которым нередко ассоциируется ярко-желтый терлингуаит (землистые агрегаты и призматические кристаллики), бурый пластинчатый пинчит, самородная ртуть, кварц и кальцит. Эти минералы известны из месторождений Чукотки, Киргизии, США (Терлингуа).
В группе новых галогенидов Hg поярковит (оксихлорид Hg) описан из Хайдаркана (Киргизия), где найден в виде малиново-красных зерен, чернеющих на изломе, в ассоциации с каломелью и эглестонитом. Твердость минерала 2,5. Каманчеит, также оксихлорид Hg, содержащий Вr, известен из месторождения Марипоза (шт. Техас, США). Типичные красные звездчатые хрупкие агрегаты с твердостью 2. Кристаллы игольчатые. Кузнецовит содержит дополнительно As. Окраска минерала медовая, светло-бурая. Твердость 2,5–3. Характерны хрупкость и легкость разложения в кислотах. Ассоциируется с каломелью, самородной Hg, эглестонитом, гидрогётитом, шаховитом, терлингуаитом. Найден в рудных месторождениях Арзак (Тува) и Хайдаркан (Киргизия). Келянит – сурьмяно-ртутный оксихлорид (бромид) – обнаружен в месторождении Келяна (Бурятия). Характерны хрупкие буровато-красные зерна с твердостью 3. Ассоциируется с каломелью и эглестонитом. Содержит до 1% Вr.
Сульфид-галогениды – лаврентьевит и арзакит – обнаружены в Арзакском и Кадырэльском рудопроявлениях ртути (Тува). Лаврентьевит – хлорид, арзакит – бромид. Образуются в пустотах между шаровидными агрегатами каолинита, окружающими киноварь. Реже покрывают корочками киноварь непосредственно. Лаврентьевит оливково-болотный, арзакит светло-бурый. На свету быстро темнеют. Блеск алмазный, твердость 2–2,5. Ассоциируются с каломелью, эглестонитом, самородной ртутью, кузнецовитом.
Мозезит и клейнит принадлежат к числу очень редких хлоридов Hg, содержащих добавочные анионы (SO4, СО3), воду и азот. Оба канареечно-желтые (Терлингуа, США).
Большой интерес вызывают находки хлор-бромидов Hg – кузьминита, кадырэлита и гречищевита, связанные с окислением ртутных руд Тувинских месторождений Арзак и Кадыральское. Эти минералы ярко-оранжевые со смолистым блеском. Чаще связаны с пустотками выщелачивания в карбонатах. Вместе с ними обычными являются Br эглестонит, каломель, лаврентьевит, ртуть.
Фториды Са и Sr – стронций-кальциевые фторалюминаты: – хотя и не концентрируют “рудные” элементы, служат показателем глубокой проработанности зоны гипергенеза и активной роли фтора в этом процессе. Источником фтора считаются флюорит, топаз и слюды. Образование фторалюминатов, очевидно, происходило из кислых сульфатных вод, так как наблюдалось замещение кридитом и герксутитом сидерита (Ермилова, 1964).
Гипергенный флюорит в виде белых и фиолетовых кристаллических корочек описан из Кызыл-Эспе, Караобы, Кургашинкана. Отлагается на ярозите, кварце, бедантите. Минерал редкий.
Кридит и геарксутит выделяются в форме желваков и глинистых белых агрегатов в тектонических трещинах, в виде корочек на пирите, кварце и сидерите, иногда вместе с галлуазитом. Известны не только в казахстанских рудных месторождениях (Караоба, Акчатау и др.), но и зарубежных (в штатах Калифорния и Колорадо, США).
Чухровит, впервые найденный в месторождении Караоба (Ермилова, 1964), принадлежит к очень редким редкоземельным фторалюминатам. Характерны кубические белые кристаллы. Отлагается в полостях кварца в ассоциации с геарксутитом, кридитом, англезитом. Источником редких земель и фтора в чухровите (до 18%) считается флюорит. В зоне гипергенеза одного из сибирских месторождений в ассоциации с геарксутитом и чухровитом обнаружен ярославит, для которого характерны белые сферические агрегаты. В качестве источника фтора также указывается флюорит.
Формула розенбергита приведена условно, в стиле фторалюмината. Возможно, это простой водный фторид AlF3·3(H2O).
Классификация галогенидов по кристаллхимическим параметрам:
1. Простые галогениды координационной структуры.
Фториды:
- флюорит СaF2,
- виллиомит NaF,
- грайсит LiF,
- кароббиит KF,
- селлаит MgF2,
- франкдиксонит BaF2,
- твейтит CaYF2,
- флюоцерит (La,Ce)F3,
- гананит BiF3,
Иодиды:
- майерсит (Ag,Cu)I
- маршит CuI
- токорналит (Ag,Hg)I
- йодаргирит AgI
- мошелит Hg2I2
Бромиды и минералы переходные от бромидов к хлоридам:
- бромаргирит
- кузминит Hg2(Br,Cl)2
- кадирелит Hg4(Br,Cl)2
- команчеит Hg13(Cl,Br)8O9
Хлориды:
- галит NaCl ,
- сильвин КCl,
- нашатырь NH4C1,
- нантокит CuCl,
- хлораргирит AgCl,
- каломель Hg2Cl2,
- лавренсит (Fe,Ni)Cl2,
- толбачит CuCl2,
- скаккит MnCl2
2. Сложные водные и безводные галоидные соединения.
- карналлит KMgCl3 6H2O,
- атакамит CuCl2·3Cu(OH)2,
- гагаринит NaCaY(F,Cl)6,
- лорелит Pb7F12Cl2,
- эриохальцит CuCl2·2(H2O)
- бишофит MgCl2·6(H2O)
- никельбишофит NiCl2·6(H2O)
- лесукит Al2(OH)5Cl·2(H2O)
- авогадрит (K,Cs)BF4
- барбериит (NH4)BF4 P
- ярлит Na(Sr,Na)7(Mg)Al6F32(OH,H2O)2
- симмонсит Na2LiAlF6
- криолит Na3AlF6
- эльпасолит K2NaAlF6
- богвадит Na2SrBa2Al4F20
- геарксутит CaAl(OH,F)5·(H2O)
- акуминит SrAlF4(OH)·(H2O)
- ярославит Ca3Al2F10(OH)2·( H2O)
- веберит Na2MgAlF7
- усовит Ba2CaMgAl2F14
- розенбергит AlF3·3(H2O)
- карналлит KMgCl3·6(H2O)
- кемпит Mn2Cl(OH)3
- атакамит Cu2Cl(OH)3
- абхурит Sn3O(OH)2Cl2
- заварицкит BiOF
- бисмоклит BiOCl
- иттроцерит CaF2 (Y,Ce)F3
3. Минералы переходные от галогенидов к другим классам:
- кридит Ca3Al2(SO4)(F,OH)10·2(H2O)
- чухровит Ca3(Ce,Y)Al2(SO4)F1310(H2O)
- малладрит Na2SiF6
- барарит (NH4)2SiF6
- стенонит (Sr,Ba,Na)2Al(CO3)F5
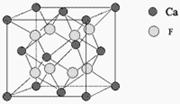
Флюорит СaF2
 Название от латинского "флюре" - течь, так как дает легкоплавкие смеси со многими минералами, что издавна используется в металлургии, где он применяется в качестве плавня (флюса). Отсюда происходит его другое название - плавиковый шпат. Ратовкит - землистый фиолетовый флюорит, встречающийся в мергелистых породах или доломитизиро-ванных известняках.
Название от латинского "флюре" - течь, так как дает легкоплавкие смеси со многими минералами, что издавна используется в металлургии, где он применяется в качестве плавня (флюса). Отсюда происходит его другое название - плавиковый шпат. Ратовкит - землистый фиолетовый флюорит, встречающийся в мергелистых породах или доломитизиро-ванных известняках.
Химический состав. Минерал часто cодержит изоморфные примеси иттрия, церия и других редких земель, стронция. Здесь проявляетcя гетеровалентный изоморфизм типа:
Ca2+ + F- = Y3+ + O2-; 2Ca2+ = Na+ + Y3+.
Рис.35. Структура флюорита
Примеси флюорита являются типоморфными. Так, флюориты, генетически связанные с гранитами, содержат в своем составе, больше иттрия, чем церия. В щелочных породах, наоборот, в составе флюорита преобладает церий. Флюориты же доломитов практически не содержат редких земель. Они вообще содержат
наименьшее количество примесей и являются наиболее чистыми.
Кристаллы кубического и октаэдричеокого габитуса характерны для флюорита. Известны друзы, массивные агрегаты от крупнокристаллических до скрытокрис-таллических, порошковатых и землистых.
 Цвет. бесцветный, фиолетовый или зеленый разных оттенков. Характерна зональная окраска, может быть прозрачным. Часто полихромный. Окраска флюорита связана, как правило, с дефектами его кристаллической структуры.
Цвет. бесцветный, фиолетовый или зеленый разных оттенков. Характерна зональная окраска, может быть прозрачным. Часто полихромный. Окраска флюорита связана, как правило, с дефектами его кристаллической структуры.
Блеск стеклянный до жирного.
Спайность совершенная по октаэдру.
Твердость 4. Хрупкий.
Излом ступенчатый.
Черта бесцветная.
Диагностика. По кубическому облику кристаллов,
спайности совершенной по октаэдру, стеклянному блеску, Рис.36. Кристаллы флюорита
низкой твердости, нередко полихромной окраске.
Происхождение. Гидротермальный с кварцем, баритом, кальцитом и сульфидами; а также с халцедоном, киноварью, антимонитом; в грейзенах с кварцем, бериллом, турмалином, касситеритом, вольфрамитом и топазом. Редко в скарнах с гранатом и кальцитом.
Ратовкит - осадочного происхождения. В поверхностных условиях устойчив и накапливается в корах выветривания.
Значение. Используется в металлургии в качестве флюса при выплавке алюминия. Прозрачные бесцветные разности флюорита используются в оптике. Является источником различных соединений фтора.
Галит NaCl
Название от греческого названия слова "гальс" - соль. Кристаллы кубического габитуса, иногда крупные. Обычно плотные массы от мелко- до гигантозернистых.
Цвет. Бесцветный, прозрачный, белый, сероватый, иногда желтый или красный (механические включения гематита), голубой (радиационные дефекты структуры), черный (органическое вещество, битумы) . Примеси как правило механические.
Блеск стеклянный.
Спайность совершенная по кубу.
Твердость 2. Хрупкий.
Прозрачен или просвечивает.
Черта белая.
Излом ступенчатый до ровного. Хорошо растворим в воде, имеет соленый вкус.
Сингония кубическая.
Диагностика. По легкой растворимости в воде, кубической форме кристаллов, совершенной спайности по кубу, низкой твердости и соленому вкусу.
Происхождение. Хемогенные осадки морского и озерного происхождения.
 Сопутствующие минералы. В ассоциации с сильвином, гипсом, доломитом, ангидритом и другими солями.
Сопутствующие минералы. В ассоциации с сильвином, гипсом, доломитом, ангидритом и другими солями.
Значение. Галит - сырье для химической и пищевой промышленности, идет для получения НСl, соды, хлора, NaОН.
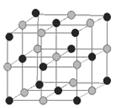
Рис.37. Структура галита
Сильвин КСl
Название в честь французского химика Сильвио-ля-Баш.
Форма кристаллов Характерны сплошные плотные зернистые массы, реже кубические и кубоктаэдрические кристаллы.
Цвет минерала белый, серый, часто бесцветен; иногда красноватый от механических примесей гематита. Обычно прозрачен или просвечивает.
Блеск стеклянный,
Спайность совершенная по кубу.
Твердость 2.
Черта белая. Легко растворим в воде, по вкусу горько-соленый.
Диагностика. По легкой растворимости в воде, низкой твердости, кубической форме кристаллов, совершенной спайности, горько-соленому вкусу.
Происхождение. Типичный минерал химических осадков морей и озер. Ассоциация с галитом, гипсом, ангидритом и другими солями. Образует также возгоны при вулканической деятельности. В небольших количествах встречается как выцветы почв.
Значение. Сырье для получения калийных удобрений.
Виллиомит NaF
Название по имени французского исследователя Биллиона.
Химический состав — содержание (в %): Na — 54,76; F — 45,24.
Цвет карминово-красный, темно-вишневый; изредка бесцветный.
Черта бледно-розовая до белой.
Блеск стеклянный.
Прозрачность Прозрачен до просвечивающего.
Твердость 2 – 2,5.
Плотность 2,79 г/см3.
Излом кристаллов раковистый, агрегатов — неровный. Хрупок.
Спайность по (100) совершенная.
Агрегаты зернистые.
Форма кристаллов несовершенные кубы.
П. п. тр - становится бесцветным. Легко плавится, по охлаждении образуется мутное бесцветное стекло.
Поведение в кислотах — Легко растворим в холодной воде.
Местонахождение. Ввиду растворимости в воде близ поверхности не сохраняется, поэтому считался исключительно редким. Впервые был установлен в составе особенно крупнозернистых разновидностей нефелиновых сиенитов о-ва Рума (о-ва Лос) в Гвинее, где является поздним первичным минералом пород, содержащих астрофиллит и ловенит, и наблюдается в тесной ассоциации с эвколитом. Широко распространен в Ловозерском массиве (Мурманская обл.), как показало изучение кернов буровых скважин. Характерен для пород комплекса луявритов, фойяитов, уртитов; в луявритах распространен более или менее равномерно, среди фойяитов отмечаются зоны, обогащенные виллиомитом, Присутствует и в ловозерских пегматитах. Повсюду является одним из самых поздних первичных минералов.
В подземных выработках Кукисвумчоррского месторождения апатита (Хибинский массив, Мурманская обл.) слагает жилки в рисчорритах, составляющих кровлю апатитового тела: наблюдался в полевошпатовом прожилке, содержащем ловчоррит, эвдиалит, ферсманит, в пектолито-виллиомитовых прожилках, слагает собственно впллиомитовые прожилки;
Изменения. Во влажном воздухе расплывается. Очень легко выщелачивается водой, поэтому может сохраниться лишь в породах, не подвергавшихся увлажнению. Возможно, что многочисленные характерные для Хибинского и Ловозерского массивов ячеистые и ельчатые пустоты (“элатолиты”), наблюдающиеся в разных породах и среди скоплений минералов, образовались в результате растворения виллиомита.
Искусств. В виде мелких кубических кристаллов кристаллизуется при выпаривании водных растворов NaF.
Гагаринит NaCaY(F,Cl)6,.
Название по имени первого в мире летчика-космонавта Ю. А. Гагарина.
Химический состав — содержание (в %): Na2O — 7,5 – 10,4; CaO — 8,8 – 14,2; TR2O3 — 54 – 55; F — 33 – 36.
Цвет бесцветный, кремовый, реже розовато-желтый. Черта — белая.
Блеск матовый до стеклянного.
Прозрачность — чистый неизмененный минерал прозрачен, но обычно полупрозрачен до непрозрачного.
Твердость 4 – 4,5. Хрупок.
Плотность 4,2—4,5 г/см3.
Спайность несовершенная по призме.
Излом кристаллов раковистый,
Сингония Тригональная.
Кристаллы призматические, шестигранные, обычно деформированные
Агрегаты Скрытокристаллические агрегаты неправильной формы, редко кристаллы..
П. п. тр - осколки спекаются, становятся розоватыми. При нагревании выше 1050° происходит быстрое спекание с выделением газов и вспучивание, после чего остается шлако-подобная масса розоватого или буроватого цвета. Полного расплавления не происходит. Перлы с бурой, фосфорной солью и содой желтовато-зеленые, при охлаждении быстро обесцвечиваются.
Прочие свойства. Частью слабо радиоактивен. Очень слабо магнитен. При электромагнитном разделения попадает в ту же фракцию, что и рибекит, эгирин и астрофиллит.
Поведение в кислотах — Частично растворяется в воде, причем в водную вытяжку переходит большая часть Na. Хорошо разлагается НNО3, НС1 и крепкой Н2SO4 (особенно при нагревании) с выделением HF.
Происхождение. Впервые обнаружен среди интенсивно альбитизированных щелочных гранитов и связанных с ними пегматоидных кварцево-микроклиновых жил в ассоциации с бастнезитом в Казахской ССР. Там же найден в жильных зонах альбититов и в альбитизированных породах песчано-сланцевой толщи на контакте с гранитами. Характерным для пород, содержащих гагаринит, является присутствие рибекита, эгирина, а из акцессорных минералов — пирохлора и циркона. Возникновению гагаринита благоприятствует щелочной метасоматоз при активном участии фтора. В Тувинской АССР гагаринит обнаружен в качестве акцессорного минерала в альбититах, залегающих в субщелочных кварцевых сиенитах, которые приурочены к зоне тектонического нарушения в гранитном массиве.
Сопутствующие минералы. Ассоциируется гагаринит с рибекитом, эгирином, циркелитом, фергусонитом, полилитионитом, сидеритом, клейофаном, флюоритом.
Практическое значение Может быть использован для получения редких земель.
Карналлит KMgCl3·6(H2O)
Название по фамилии Карналь
Химический состав. Mg - 8,7%, К - 14,1%, С1 - 38,3%, Н2O - 38,9%.
Цвет. Красный (благодаря мелкочешуйчатым включениям гематита), желтый, белый, бесцветный.
Блеск. Стеклянный.
Прозрачность. Мутный, просвечивающий, прозрачный.
Черта. Белая.
Твердость. 1—2, хрупкий.
Плотность. 1,60.
Излом. Раковистый.
Сингония. Ромбическая.
Форма кристаллов. Кристаллы крайне редки, имеют псевдогексагональный облик.
Класс симметрии. Ромбо-бипирамидальный — mmm.
Спайность. Отсутствует.
Агрегаты. Массивные грубозернистые агрегаты и массы.
П. тр. Легко плавится; легко растворяется в воде.
Прочие свойства. Специфической особенностью карналлита является жгучий соленый вкус; он сильно гигроскопичен.
Сопутствующие минералы. Ангидрит, сильвин, каинит, кизерит, борацит, галит.
Сходные минералы. Каинит, красная каменная соль.
Практическое значение. Важное сырье для извлечения калия.
Происхождение. Кристаллизуется вместе с другими солями в соляных озерах при испарении в условиях жаркого сухого климата; образует крупные соляные залежи.
Месторождения. Многочисленные соляные разработки в округах Магдебург, Эрфурт, Зуль и Галле, Гессен, Ганновер (Германия); Франция; Канада; Соликамск (Россия) и другие районы
Атакамит Cu2Cl(OH)3
Название - по пустыне Атакама в Чили и Перу.
Химический состав. 59% меди
Цвет. Травяно-зеленый, черновато-зеленый.
Блеск. Стеклянный, алмазный.
Прозрачность. Прозрачный, просвечивающий.
Черта. От светло-зеленой до яблочно-зеленой.
Твердость. 3,5.
Плотность. 3,76.
Сингония. Ромбическая.
Класс симметрии. Ромбо-бипирамидальный — mmn.,
Форма кристаллических выделений. Сплошные, плотные, зернистые, листоватые агрегаты.
Спайность. Совершенная по (010), средняя по (101).
П. тр. Плавится.
Поведение в кислотах. Нерастворим; слабо растворяется в воде.
Сопутствующие минералы. Лимонит, гематит, оливенит.
Сходные минералы. Малахит, диоптаз.
Практическое значение. Медная руда.
Происхождение. В зонах окисления медных месторождений в аридном климате.
Месторождения. Пустыня Атакама.
Нашатырь NH4C1.
Название от арабского nuhadir — вздыхать, нюхать (толковый словарь Ушакова).
Химический состав содержание (в %): NH4 - 33,72; Cl - 66,28. Часто содержит значительное количество Fe (вероятно, в виде субмикроскопических вростков хлоридов), Вr — до 0,12%; по данным спектрального анализа — следы Сu, Ag, Co, Ni, Zr, Mo, Ga, Cr, V, Ва. В виде изоморфной примеси может содержать при комнатной температуре до 3,24 % КСl.
Цвет бесцветен или белый, часто окрашен в желтые, оранжевые до красного и бурые тона благодаря примеси серы и железосодержащих минералов. Иногда серый от включений углистого вещества.
 Черта белая.
Черта белая.
Блеск стеклянный.
Прозрачность Прозрачные кристаллы из отложений
фумарол при остывании на воздухе растрескиваются и мутнеют.
Твердость 1 – 2.
Плотность 1,53 г/см3.
Излом раковистый. Пластичен; в порошок истирается с трудом.
Сингония Кубическая. Рис.38. Кристалл нашатыря
Спайность по (111) несовершенная.
Агрегаты Рыхлые землистые массы, пушистые игольчатые налеты; друзы кристаллов, сталактиты, полые наросты, натечные корочки. каплевидные формы в нишах и пещерах, веерообразные, шестоватые. ячеистые и параллельно-волокнистые агрегаты; иногда заполняетпорылавы, цементирует куски лавы, слагает устья некоторых фумарол.
Кристаллы тетрагонально-триоктаэдрического, ромбо-додэкаэдрического, изредка кубического облика. Часто удлинены по оси третьего или четвертого порядка и имеют псевдотригональный, псевдотетрагональный, редко псевдоромбический облик. Обычно кристаллы развиты очень несовершенно, характерны скелетные формы в виде “елочек”, скипетровидные кристаллы. Известны скелетные сростки лучистого сложения, ромбододекаэдры со ступенчато-вогнутыми гранями и кристаллы, уплощенные по двум граням куба. Двойники по (111). Нередки включения газов, обычно немногочисленные, иногда расположенные параллельными рядами.
П. п. тр - легко улетучивается без плавления с образованием дыма; в закр. тр. возгоняется, не плавясь; при нагревании с щелочами и при сплавлении с содой — запах аммиака. Из водного раствора AgNO3 осаждает белый осадок AgCl.
Поведение в кислотах — В воде легко растворяется. Вкус вяжущий и соленый, жгучий.
Происхождение. О происхождении нашатыря в вулканических возгонах имеются следующие гипотезы: 1)нашатырь образуется в результате воздействия магматических масс на растительный покров; 2) азот нашатыря находился в магме в виде гипотетических соединений типа N2Fe5, Si3N4 н т. п.; 3) аммиак образуется в результате воздействия раскаленных масс лавы на азот воздуха в присутствии катализаторов.
Наблюдения на Ключевской сопке показали, что при равных условиях застывания лавы и одинаковом составе летучих компонентов, большие скопления нашатыря наблюдались лишь на лавовых потоках, заливших растительность, но с другой стороны, он отмечался также на только что упавших лапиллях и на поверхности лавы в кратере. Образуется, как правило, спустя некоторое время после излияния лавы в температурном интервале 150—300° как из кислых, так и из щелочных газов, иногда и в очень значительных количествах; является главным минералом возгонов некоторых фумарол. Форма выделения зависит от условий отложения: в открытых местах образует пушистые или землистые налеты, в закрытых от ветра участках — плотные образования.
Сопутствующие минералы. Ассоциируется с кермезитом, серой, гипсом, галитом, сильвином, криптогалитом, которые часто образуют в нем мелкие включения.
Крупные скопления встречены на Ключевском вулкане и на вулкане Толбачек (Камчатка), в Италии на Везувии, Этне, о-ве Стромболи; наблюдается на Гавайских о-вах, в Исландии и в других вулканических областях.
В качестве продукта возгона при подземном горении каменного угля отмечался с серой, квасцами, реже с реальгаром, аурипигментом, масканьитом в Дутвайлер, Саарская обл. Плауеншен Грунд близ Дрездена (Германия), близ Сент-Этьенна (Франция), в Ньюкастле и Нортумберленде (Англия), в Хамарин-Хурал-Хид (МНР) [3] и др. В отложениях гуано на о-вах Гуаньяпе и Чинча в Перу, на о-ве Тарапака в Чили. В виде выцветов на поверхности почвы на Апшеронском п-ве (Азербайджан), в Венгрии, в Южной Америке.
Соли кислородных кислот.
Принципы классификации минералов даны в лекционном курсе. Остается напомнить, что соли кислородных кислот являются сложными химическими соединениями, образовавшимися в результате различных геологических процессов.
Среди солей выделяют соли водные и безводные. Среди тех и других различают:
- кислые соли – содержащие вместо одного металлического катиона протон H1+, который в кристаллических решетках обусловливает водородную связь. В природных условиях кислые соли мало распространены. Например: нахколит - NaH[CO3], или гайдингерит - CaH[AsO4] H2О.
- нормальные или средние соли, пользующиеся наибольшим распространением в природе. Например: кальцит –Ca[CO3] , гипс – Ca[SO4] 2H2O.
- основные соли – содержащие в составе ионы гидроксила (OH)1-, нейтрализующие избыточный положительный заряд катионов. Также, как и средние соли широко распространены в приоде. Примером может служить: малахит – Cu2[CO3]2 (OH)2.
В основных солях анион (OH)1- может быть частично или полностью заменен анионами F1-или Cl1-. Двойные и более сложные соли отличаются тем, что катионы или анионы представлены разными ионами изоморфно замещающими друг друга.
В солях переменного состава имеет место как изовалентный, так и гетеровалентгый изоморфизм.
Характерной особенностью кристаллохимии кислородных солей являеется наличие комплексных анионов (радикалов). Катионы располагающиеся в центрах этих групп, обладают малыми размерами и высокими зарядами. Очень важно обратить внимание в этих группах на прочность связи ионов кислорода с центральным катионом, определяемую величиной заряда, приходящегося от катиона на каждый окружающий его ион кислорода.во всех соединениях, кроме боратов и островных силикатов это отношение превышает 1. это означает, что ионы кислорода прочнее связаны с малыми катионами внутри комплексов, чем с катионами расположенными в решетках. Таким образом, комплексные анионы учавствуют в кристаллических структурах как самостоятельные структурные единицы. При растворении солей эти группы не распадаются.
Подавляющая масса кислородных солей представляет собой типичные ионные соединения. Естественно, что устойчивость кристаллических структур в значительной мере зависит от соотношений размеров катионов и анионов, как структурных единиц. Анионы в простых соединениях типа АХ (где Х представлен комплексным анионом) наиболее устойчивы только в сочетании с крупными катионами. Такие соли являются наиболее устойчивыми, труднорастворимыми, тугоплавкими и труднолетучими. Например: двухвалентный анион [SO4]2- в соединениях типа АХ (соотношение катион : анион =1:1) образует следующие минералы - барит Ba[SO4] и англезит Pb[SO4]. С этой точки зрения становятся понятными изоморфные примеси Ra2+ в баритах (ионный радиус Ra больше Ba). Не удивительно, чт в зонах окисления урановых месторождений, содержащих сульфиды при воздействии сульфатных вод, концентрация радия по отношению к урану выше, чем в первичных рудах (соединения шестивалентного урана в таких условиях более растворимы, по сравнению с сульфатом радия).
Что касается двухвалентных катионов с малыми ионными радиусами, то они в природных условиях могут образовывать только водные сульфаты, кристаллизующиеся при низких температурах и на последних стадиях кристаллизации растворов. Чаще всего водные соли содержат 2, 4, 6 или 7 молекул воды.
Водные соли обладают повышенной или высокой растворимостью, легко обезвоживаются. При этом их кристаллические структуры перестраиваются или разрушаются.
Систематика кислородных солей по кислотным радикалам приведена в приложениях.
Дата добавления: 2018-05-12; просмотров: 382; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
