Среднеарифметическая скорость
Лекция №11.
Основы молекулярно – кинетической теории газов.
Молекулярная физика – раздел физики изучающий строение и свойства вещества исходя из молекулярно – кинетических представлений.
Основные положения МКТ:
1.Вещество состоит из большого числа атомов, молекул.
2.Молекулы вещества находятся в хаотическом тепловом (не имеющим преимущественного направления) движении.
3.Молекулы вещества взаимодействуют друг с другом.
Молекулярно – кинетическая теория объясняет свойства тел, наблюдаемых на опыте (температуру, давление и т.д.), как суммарный результат действия всех молекул.
Система – объект, состоящий
Статистический метод состоит в том, что при изучении процессов, протекающих в системе, мы оперируем среднестатистическими параметрами ее структурных элементов.
Молекулярная физика – статистическая физика.
Термодинамика – раздел физики так же изучающий разные состояния вещества, тепловые процессы, происходящие в веществе.
Термодинамический методсостоит в том, что при изучении процессов, протекающих в системе, мы оперируем макропараметрами системы, не рассматривая поведение и параметры ее структурных элементов.
Термодинамика базируется на ряде фундаментальных законов, установленных в результате обобщения большого числа опытных фактов.
Термодинамика и статическая физика взаимно связанны и дополняют друг друга.
Атомистическая теория строения вещества была развита как научная теория в 17 – 18 веке, хотя гипотезы об атомистическом строении (догадки) высказывались ещё древними греками.
М.В. Ломоносов развил эту теорию, пытаясь дать единую картину известных химических и физических свойств вещества исходя из корпускулярного строения вещества. В противовес теории «теплорода» Ломоносов причину «тепла» видит в движении корпускул.
Идеальный газ.
1.Молекулы – материальные точки т.е.  объём молекул равен нулю.
объём молекул равен нулю.
2.Молекулы не взаимодействуют друг с другом.
3.Молекулы хаотически движутся упруго сталкиваясь со стенками сосуда и друг с другом.
Сильно разряженный газ  идеальный.
идеальный.
Основное уравнение молекулярно – кинетической теории.
Полагаем:
а) Давление газа на стенки сосуда обусловлено упругим соударением молекул со стенками. При ударе происходит изменение импульса молекул, т.е. оказывается силовое воздействие на стенки сосуда.
Допустим, что за время  по поверхности стенки площадью Sударяет большое количество молекул и суммарное приращение их импульса равно
по поверхности стенки площадью Sударяет большое количество молекул и суммарное приращение их импульса равно  . Точно такое же превращение импульса получает поверхность стенки. Причём
. Точно такое же превращение импульса получает поверхность стенки. Причём 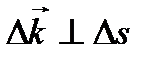 .
.
По второму закону Ньютонанормальная сила, действующая на стенку равна:

По определению давление равно:

б). Молекулы движутся хаотически. Все направления равновероятны. Если бы не так, то давление газа на разные стенки было бы разное.
в). Скорости молекул могут быть различными по величине. При соударениях скорости молекул равновероятно как возрастают, так и убывают. При упругом столкновении (центральном ударе) двух шаров одинаковой массы они обмениваются скоростями. Суммарная энергия молекул не изменяется.
Упрощения:
- Молекулы движутся только по трём взаимно перпендикулярным направлениям. Пусть в объёме N молекул. Вдоль одного направления движутся
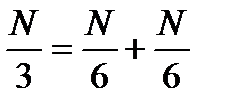 (в одну и другую сторону).
(в одну и другую сторону).

|

|

|

|

|

|
-



Все молекулы имеют одинаковую скорость.
Приращение импульса молекул при упругомударе.

|

|

|

В проекции на нормаль к стенке
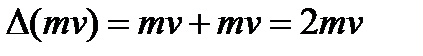
Приращение импульсамолекулыравно приращению импульса стенки.
За время  в стенку ударяется
в стенку ударяется  часть молекул в объёме.
часть молекул в объёме.

Суммарное приращение импульса стенки равно:

Основное уравнение МКТ

|
Давление газа равно  кинетической энергии поступательно движения молекул газа, содержащихся в единице объёма.
кинетической энергии поступательно движения молекул газа, содержащихся в единице объёма.
Строгий вывод, учитывающий распределение молекул по скоростям, различные направления полёта рассеяния молекул при столкновениях приводит к тому же результату.
Среднеарифметическая скорость

Дата добавления: 2018-05-12; просмотров: 338; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
