Периодический закон Д.И. Менделеева – свойства элементов находятся в периодической зависимости от их порядкового номера.
Задачи с расчетами по уравнениям реакций,
происходящих в растворах
При обучении школьников способам решения задач очень большое значение придаю применению алгоритмов. Я считаю, что вначале нужно уверенно овладеть небольшим числом стандартных приемов, получить представление о возможных типах задач. Это позволит ученику выйти на творческий уровень в своем дальнейшем химическом образовании и самообразовании.
Одно из заданий высокого уровня сложности (оно входит в третью часть экзаменационной работы – задание С4) проверяет умение производить расчеты по уравнениям реакций, происходящих в растворах.
В учебной литературе недостаточно подробно объясняются особенности решения таких задач. Поэтому мы с учениками вначале разбираем все моменты, на которые нужно обратить внимание, записываем алгоритмы в общем виде, рассматриваем решение задач каждого типа, затем отрабатываем умения на самостоятельном решении целого ряда подобных задач.
Прежде всего ученик должен усвоить понятие о массовой доле растворенного вещества, или, иначе, процентной концентрации раствора. Эта величина показывает отношение массы растворенного вещества к массе раствора:
 р.в-во = mр.в-во / mр-р.
р.в-во = mр.в-во / mр-р.
Производные формулы:
mр.в-во = mр-р•  р.в-во,
р.в-во,
mр-р = mр.в-во /  р.в-во.
р.в-во.
Если в условии задачи указан объем раствора с определенной плотностью, то прежде всего находят массу раствора:
mр-р = Vр-р• 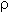 р-р,
р-р,
|
|
|
затем – массу растворенного вещества:
mр.в-во = mр-р•  р.в-во.
р.в-во.
Количество вещества находят по массе растворенного вещества:
 = mр.в-во / М.
= mр.в-во / М.
Рассмотрим некоторые типы задач с расчетами по уравнениям реакций, происходящих в растворах.
•Нахождение массовых долей веществ в растворе после реакции.
При решении таких задач прежде всего нужно найти количества вещества реагентов. Если задача на избыток и недостаток, то количества вещества продуктов реакции находят по веществу, которое дано в недостатке.
Один из важных моментов – это нахождение массы раствора после реакции (массы полученного раствора, mр-р получ). Если какое-либо вещество взаимодействует с веществом, находящимся в растворе, то складывают массу вещества и массу раствора; в случае, когда оба реагирующих вещества даны в виде растворов, складывают массы двух растворов. Если в результате реакции образуется осадок или газ, то из полученной суммы вычитают массу вещества, ушедшего из раствора в виде осадка или газа:
mр-р получ = mв-во + mр-р – mосадок (газ),
mр-р получ = mр-р1 + m р-р2 – mосадок (газ).
При решении задач на избыток и недостаток нужно помнить о том, что в растворе после реакции будет находиться в растворенном виде не только продукт реакции, но и вещество, которое было дано в избытке.
|
|
|
Чтобы найти количество вещества, которое не прореагировало – избытка, нужно от исходного количества вещества отнять количество прореагировавшего вещества:
 изб =
изб =  исх –
исх –  прор.
прор.
Затем найти его массу и массовую долю в растворе, полученном после реакции.
Задача 1. 4,8 г магния растворили в 200 мл 12%-го раствора серной кислоты ( 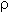 = 1,05 г/мл). Найти массовую долю соли в полученном растворе.
= 1,05 г/мл). Найти массовую долю соли в полученном растворе.
Дано:
m(Mg) = 4,8 г,
Vр-р(H2SO4) = 200 мл,
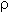 р-р(H2SO4) = 1,05 г/мл, р-р(H2SO4) = 1,05 г/мл,
 р.в-во(H2SO4) = 12 %. р.в-во(H2SO4) = 12 %.
| Найти:  р.в-во(MgSO4). р.в-во(MgSO4).
|
Р е ш е н и е

 (Мg) = m / M = 4,8 (г) / 24 (г/моль) = 0,2 моль.
(Мg) = m / M = 4,8 (г) / 24 (г/моль) = 0,2 моль.
mр-р(H2SO4) = Vр-р• 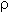 = 200 (мл)•1,05 (г/мл) = 210 г.
= 200 (мл)•1,05 (г/мл) = 210 г.
mр.в-во(H2SO4) = mр-р•  р.в-во = 210•0,12 = 25,2 г.
р.в-во = 210•0,12 = 25,2 г.
 р.в-во(H2SO4) = m/M = 25,2 (г) / 98 (г/моль) = 0,26 моль.
р.в-во(H2SO4) = m/M = 25,2 (г) / 98 (г/моль) = 0,26 моль.
В недостатке – Mg. Следовательно:
 (MgSO4) = 0,2 моль,
(MgSO4) = 0,2 моль,
 (H2) = 0,2 моль.
(H2) = 0,2 моль.
mр.в-во(MgSO4) = M•  = 120 (г/моль)•0,2 (моль) = 24 г.
= 120 (г/моль)•0,2 (моль) = 24 г.
m(H2) = M•  = 2 (г/моль)•0,2 (моль) = 0,4 г.
= 2 (г/моль)•0,2 (моль) = 0,4 г.
mр-р получ = mр-р(H2SO4) + m(Mg) – m(H2) = 210 (г) + 4,8 (г) – 0,4 (г) = 214,4 г.
 р.в-во(MgSO4) = mр.в-во(MgSO4) / mр-р получ = 24 (г) / 214,4 (г) = 0,112, или 11,2 %.
р.в-во(MgSO4) = mр.в-во(MgSO4) / mр-р получ = 24 (г) / 214,4 (г) = 0,112, или 11,2 %.
О т в е т.  р.в-во(MgSO4) = 11,2 %.
р.в-во(MgSO4) = 11,2 %.
Задача 3. Карбонат кальция массой 10 г растворили при нагревании в 150 мл хлороводородной кислоты ( 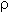 = 1,04 г/мл) с массовой долей 9 %. Какова массовая доля хлороводорода в получившемся растворе?
= 1,04 г/мл) с массовой долей 9 %. Какова массовая доля хлороводорода в получившемся растворе?
О т в е т.  р.в-во(HCl) = 4,2 %.
р.в-во(HCl) = 4,2 %.
|
|
|
Задача 4. 5,6 г железа растворили в 100 мл 10%-го раствора соляной кислоты ( 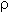 = 1,05 г/мл). Вычислить массовую долю хлороводорода в полученном растворе.
= 1,05 г/мл). Вычислить массовую долю хлороводорода в полученном растворе.
О т в е т.  р.в-во(HCl) = 2,9 %.
р.в-во(HCl) = 2,9 %.
Задача 5. 5,6 г железа растворили в 200 мл раствора соляной кислоты ( 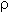 = 1,05 г/мл) с массовой долей 10 %. Найти массовую долю соли в полученном растворе.
= 1,05 г/мл) с массовой долей 10 %. Найти массовую долю соли в полученном растворе.
О т в е т.  р.в-во(FeCl2) = 5,9 %.
р.в-во(FeCl2) = 5,9 %.
Задача 6. Смешали 110,4 г раствора карбоната калия с концентрацией 25 % и 111 г раствора хлорида кальция с концентрацией 20 %. Найти концентрацию вещества в полученном растворе.
О т в е т.  р.в-во(KCl) = 14,8 %.
р.в-во(KCl) = 14,8 %.
Задача 7. Смешали 320 г раствора сульфата меди(II) с концентрацией 5 % и 120 г раствора гидроксида натрия с концентрацией 10 %. Найти концентрации веществ в полученном растворе.
О т в е т.  р.в-во(Na2SO4) = 3,3 %,
р.в-во(Na2SO4) = 3,3 %,  р.в-во(NaOH) = 0,9 %.
р.в-во(NaOH) = 0,9 %.
• Более сложными являются задачи на нахождение массы (или объема) вещества, которое нужно добавить к раствору другого вещества для того, чтобы его концентрация изменилась в результате произошедшей реакции.
В этом случае алгоритм решения следующий:
1)нужно обозначить за x количество добавленного вещества – реагента;
2) выразить через х количества прореагировавшего с реагентом вещества и полученного в результате реакции газа или осадка;
|
|
|
3) найти количество растворенного вещества в исходном растворе и его количество, оставшееся после реакции (  оставш =
оставш =  1 –
1 –  прор);
прор);
4) выразить через х массу оставшегося в растворе вещества;
5) найти массу раствора, полученного после реакции:
mр-р получ = mреаг + mр-р1 – mосадок (газ);
mр-р получ = mр-р1 + mр-р2 – m осадок (газ).
6) все данные подставить в формулу:
 р.в-во2 = mоставш / mр-р получ.
р.в-во2 = mоставш / mр-р получ.
7) найти количество вещества реагента, его массу или объем.
Задача 8. Найти массу карбоната кальция, которую следует добавить к 600 г раствора азотной кислоты с массовой долей 31,5 %, чтобы массовая доля кислоты уменьшилась до 10,5 %.
Дано:
mр-р1(HNO3) = 600 г,
 р.в-во1(HNO3) = 31,5 %, р.в-во1(HNO3) = 31,5 %,
 р.в-во2 (HNO3) = 10,5 %. р.в-во2 (HNO3) = 10,5 %.
| Найти: m(CaCO3). |
Р е ш е н и е

 (СаСО3) = х моль;
(СаСО3) = х моль;  (HNO3)прор = 2х моль;
(HNO3)прор = 2х моль;
 (СО2) = х моль, m(CO2) = 44x г;
(СО2) = х моль, m(CO2) = 44x г;
m(CaCO3) = M•  = 100 (г/моль)•х (моль) = 100х г;
= 100 (г/моль)•х (моль) = 100х г;
mр.в-во1(HNO3) = mр-р1•  р.в-во1 = 600 (г)•0,315 = 189 г;
р.в-во1 = 600 (г)•0,315 = 189 г;
 1(HNO3) = m р.в-во /М = 189 (г) / 63 (г/моль) = 3 моль,
1(HNO3) = m р.в-во /М = 189 (г) / 63 (г/моль) = 3 моль,
 оставш(HNO3) =
оставш(HNO3) =  1 –
1 –  прор = 3 – 2х моль,
прор = 3 – 2х моль,
mоставш(HNO3) = М•  = 63 (г/моль)•(3 – 2х) = (189 – 126х) г;
= 63 (г/моль)•(3 – 2х) = (189 – 126х) г;
mр-рполуч = m(CaCO3) + mр-р1(HNO3) – m(CO2) = 100x + 600 – 44x = 600 + 56x,
 р.в-во2(HNO3) = mоставш(HNO3) / mр-р получ.
р.в-во2(HNO3) = mоставш(HNO3) / mр-р получ.
0,105 = (189 – 126х) / (600 + 56х),
х = 0,955 моль,  (СаСО3) = 0,955 моль,
(СаСО3) = 0,955 моль,
m(CaCO3) = M•  = 100 (г/моль)•0,955 (моль) = 95,5 г.
= 100 (г/моль)•0,955 (моль) = 95,5 г.
О т в е т. m(CaCO3) = 95,5 г.
Задача 9. Найти массу кристаллогидрата CaCl2•6H2O, которую необходимо добавить к 47 мл 25%-го раствора карбоната натрия ( 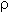 = 1,08 г/мл), чтобы получить раствор, в котором массовая доля карбоната натрия составила бы 10 %.
= 1,08 г/мл), чтобы получить раствор, в котором массовая доля карбоната натрия составила бы 10 %.
Дано:
Vр-р1(Na2CO3) = 47 мл,
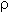 р-р1(Na2CO3) = 1,08 г/мл, р-р1(Na2CO3) = 1,08 г/мл,
 р.в-во1(Na2CO3) = 25 %, р.в-во1(Na2CO3) = 25 %,
 р.в-во2(Na2CO3) = 10 %. р.в-во2(Na2CO3) = 10 %.
| Найти: m(CaCl2•6H2O). |
Р е ш е н и е

 (СaCl2•6H2O) = x моль,
(СaCl2•6H2O) = x моль,  (CaCl2) = x моль,
(CaCl2) = x моль,
 прор(Na2CO3) = х моль,
прор(Na2CO3) = х моль,  (СаСО3) = х моль;
(СаСО3) = х моль;
m(CaCl2•6H2O) = M•  = 219 (г/моль)•х (моль) = 219х г;
= 219 (г/моль)•х (моль) = 219х г;
m(CaCO3) = M•  = 100x г;
= 100x г;
mр-р1(Na2CO3) = Vр-р1• 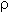 р-р1 = 47 (мл)• 1,08 (г/мл) = 50,76 г,
р-р1 = 47 (мл)• 1,08 (г/мл) = 50,76 г,
mр.в-во1(Na2CO3) = mр-р1•  р.в-во1 = 50,76 (г)•0,25 = 12,69 г,
р.в-во1 = 50,76 (г)•0,25 = 12,69 г,
 1(Na2CO3) = mр.в-во1 / M = 12,69 (г) / 106 (г/моль) = 0,12 моль,
1(Na2CO3) = mр.в-во1 / M = 12,69 (г) / 106 (г/моль) = 0,12 моль,
 оставш(Na2CO3) =
оставш(Na2CO3) =  1 –
1 –  прор = 0,12 – х,
прор = 0,12 – х,
mоставш(Na2CO3) = M•  = 106(0,12 – x) = 12,69 – 106x;
= 106(0,12 – x) = 12,69 – 106x;
mр-р получ = m(CaCl2•6H2O) + mр-р1(Na2CO3) – m(CaCO3),
219x + 50,76 – 100x = 50,76 + 119x,
 р.в-во2 = mоставш(Na2CO3) / mр-р получ,
р.в-во2 = mоставш(Na2CO3) / mр-р получ,
0,1 = 12,69 – 106х / 50,76 + 119х,
х = 0,0646 моль.
m(CaCl2•6H2O) = М•  = 219 (г/моль)•0,0646 (моль) = 14,14 г.
= 219 (г/моль)•0,0646 (моль) = 14,14 г.
О т в е т. m(CaCl2•6H2O) = 14,4 г.
Задача 10. Какой объем 30%-го раствора аммиака ( 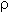 = 0,892 г/мл) необходимо добавить к 200 мл 40%-го раствора соляной кислоты (
= 0,892 г/мл) необходимо добавить к 200 мл 40%-го раствора соляной кислоты ( 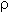 = 1,198 г/мл), чтобы массовая доля кислоты уменьшилась вчетверо?
= 1,198 г/мл), чтобы массовая доля кислоты уменьшилась вчетверо?
О т в е т. Vр-р(NH3) = 108,2 мл.
Задача 11. Какой объем углекислого газа нужно добавить к 100 мл 20%-го раствора гидроксида натрия ( 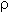 = 4,1 г/мл), чтобы массовая доля гидроксида натрия уменьшилась вдвое?
= 4,1 г/мл), чтобы массовая доля гидроксида натрия уменьшилась вдвое?
О т в е т. V(CO2) = 10,9 л.
Задача 12. Найти объем раствора соляной кислоты ( 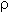 = 1,05 г/мл) с массовой долей 10 %, который нужно добавить к 350 г раствора гидроксида калия с массовой долей 10,5 %, чтобы концентрация щелочи составила 3 %.
= 1,05 г/мл) с массовой долей 10 %, который нужно добавить к 350 г раствора гидроксида калия с массовой долей 10,5 %, чтобы концентрация щелочи составила 3 %.
О т в е т. Vр-р(HCl) = 135,6 мл.
• Внимание:растворенное вещество – реагент!
При решении задач на растворы нужно помнить о том, что при обычных условиях с водой реагируют следующие вещества:
1) щелочные и щелочно-земельные металлы, например:
2Na + 2H2O = 2NaOH + H2  ;
;
2) оксиды щелочных и щелочно-земельных металлов, например:
СаО + Н2О = Са(ОН)2;
3) оксиды неметаллов, например:
SO3 + H2O = H2SO4;
4) многие бинарные соединения – гидриды, карбиды, нитриды и другие, например:
KН + Н2О = KОН + Н2  .
.
Дата добавления: 2018-05-12; просмотров: 294; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
