Изменение энтропии в физико-химических процессах.
Энергетика химических процессов.
Скорость химической реакции – это изменение количества реагирующего вещества или продукта реакции за единицу времени в единице объема (для гомогенной реакции) или на единице поверхности раздела фаз (для гетерогенной реакции).
Закон действующих масс: зависимость скорости реакции от концентрации реагирующих веществ. Чем выше концентрация , тем большее число молекул содержится в объеме. Следовательно, возрастает число соударений, что приводит к увеличению скорости процесса.
Кинетическое уравнение– зависимость скорости реакции от концентрации.
Твердые тела равны 0 Молекулярность реакции– это минимальное число молекул, участвующих в элементарном химическом процессе. По молекулярности элементарные химические реакции делятся на молекулярные (А →) и бимолекулярные (А + В →); тримолекулярные реакции встречаются чрезвычайно редко. Общий порядок реакции- это сумма показателей степеней концентрации в кинетическом уравнении. Константа скорости реакции — коэффициент пропорциональности в кинетическом уравнении. Правило Вант-Гоффа: При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два — четыре раза
Теория активных соударений (ТАС), есть три условия, необходимых для того, чтобы произошла реакция:
Энергия активации— минимальное количество энергии, которое требуется сообщить системе, чтобы произошла реакция.
Уравнение Аррениуса устанавливает зависимость константы скорости химической реакции от температуры
A - характеризует частоту столкновений реагирующих молекул R — универсальная газовая постоянная. Влияние катализаторов на скорость реакции. Катализатор – это вещество, изменяющее скорость химической реакции, но само в реакции не расходуется и в конечные продукты не входит. При этом изменение скорости реакции происходит за счет изменения энергии активации, причем катализатор с реагентами образует активированный комплекс. Катализ -химическое явление, суть которого заключается в изменении скоростей химических реакций при действии некоторых веществ (их называют катализаторами). Гетерогенный катализ - реагент и катализатор находятся в разных фазах - газообразной и твердой. Гомогенный катализе -реагенты (реактивы) и катализатор находятся в одной фазе - например, оба являются газами или оба растворены в каком-либо растворителе .
Условия химического равновесия состояние химического равновесия сохраняется до тех пор, пока остаются неизменными условия реакции: концентрация, температура и давление. Принцип Ле-Шателье:если на систему, находящуюся в равновесии оказано какое-либо внешнее воздействии, то равновесии сместится в сторону той реакции, которое это действие будет ослаблять. Константа равновесия –это мера полноты протекания реакции, чем больше величина константы равновесия, тем выше степень превращение исходных веществ в продукты реакции.
Δ ΔG>0 Кр<1 Спр <Сисх | Задачи химической термодинамики:
Первый закон термодинамики
Изменение ΔU внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты Q, переданной системе, и работой A, совершенной системой над внешними телами.
Энтальпия - это тепловой эффект реакции, измеренный (или вычисленный) для случая, когда реакция происходит в открытом сосуде (т.е. при неизменном давлении). Обозначается как ΔH. Стандартная энтальпия образования простых веществ и химических соединений-энтальпия при стандартных условиях Т-289К P=1,013*103 Па µ=1 моль Следствие из Закона Гесса Тепловой эффект реакции равен сумме энтальпии образования продуктов минус энтальпии образования исходных веществ с учетом стехиометрических коэффициентов. aA+bB=cC+dD ΔH=cΔH(C)+dΔH(D)-aΔH(A)-bΔH(B) Энтропия –это мера беспорядка системы, состоящая из многих элементов. Второй закон термодинамики: все самопроизвольные процессы в замкнутой неравновесной системе происходят в таком направлении, при котором энтропия системы возрастает; в состоянии теплового равновесия она максимальна и постоянна.
Изменение энтропии в физико-химических процессах. ΔS=S2-S1
 Мы поможем в написании ваших работ! |

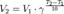
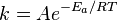

 G<0 Кр >1 Спр >Сисх
G<0 Кр >1 Спр >Сисх