ПРОТИВООПУХОЛЕВАЯ ЗАЩИТА ОРГАНИЗМА
Различают антиканцерогенные, антимутационные и антицеллюлярные механизмы противоопухолевой защиты.
Антиканцерогенные механизмы
Антиканцерогенные механизмы обеспечивают торможение и/или блокаду проникновения канцерогенов в клетку, её ядро, действие их на геном и инактивацию и элиминацию бластомогенных агентов из клетки и организма.
Механизмы, препятствующие действию химических канцерогенных факторов
- Физико-химическая фиксация и удаление из организма
- Поглощение канцерогенов в процессе фагоцитоза, сочетающееся с их инактивацией и разрушением.
- Инактивация бластомогенных агентов как гаптенов при помощи AT и Т-лимфоцитов с последующей их деструкцией и элиминацей из организма.
- Конкурентная блокада неканцерогенными метаболитами клеточных рецепторов, с которыми способны взаимодействовать истинные бластомогенные вещества.
- Разрушение и/или инактивация канцерогенов в клетках и биологических жидкостях в процессе их окисления, восстановления, деметилирования, глюкуронизации, сульфатирования.
- Ингибирование («гашение») свободных радикалов и гидроперекисей органических и неорганических соединений ферментативными и неферментными факторами антиоксидантной защиты.
Механизмы, препятствующие действию онкогенных вирусов
- Инактивация вирусов Ig, образуемыми плазматическими клетками под влиянием антигенных вирусных белков.
|
|
|
- Ингибирование ИФН — белками, тормозящими или блокирующими процесс внутриклеточной репликации вирусов.
- Обнаружение и разрушение вируссодержащих клеток организма неспецифическими цитолитическими клетками.
Механизмы, препятствующие действию канцерогенов физической природы
- Улавливание и/или инактивация свободных радикалов кислорода, липидов, других органических и неорганических веществ.
- Разрушение перекисей и гидроперекисей различных веществ.
Антимутационные механизмы
Антимутационные механизмы обеспечивают обнаружение, устранение или подавление активности онкогенов. Реализуются антимутационные механизмы при участии онкосупрессоров и систем репарации ДНК.
При недостаточности антимутационных механизмов и активации онкогенов нормальная клетка приобретает опухолевый генотип и характерные для него фенотипические признаки. Это служит сигналом для включения антицеллю-лярных механизмов противоопухолевой защиты.
Антицеллюлярные механизмы
Антицеллюлярные механизмы обеспечивают обнаружение и разрушение гено-типически и фенотипически чужеродных для организма опухолевых клеток или торможения их роста. Сигналом для активации антицеллюлярных механизмов противоопухолевой защиты организма является генетическая чужеродность клеток бластомы.
|
|
|
Различают неиммунные (неспецифические) и иммунные (специфические) антицеллюлярные механизмы.
Неиммунные механизмы. Эти механизмы осуществляют надзор за сохранением нормального (индивидуального и однородного) клеточного состава организма. Реализуют эти механизмы как клетки, так и гуморальные факторы.
Иммунные механизмы. Эти механизмы реализуют клеточное и гуморальное звенья иммунитета.
ПРОФИЛАКТИКА ОПУХОЛЕЙ
Цель профилактики новообразований:предупредить действие на клеточный геном клеток канцерогенов,значительно снизить их бластомогенное действие и предотвратить тем самым возникновение опухолевой клетки.
Мероприятия
• Снижение содержания или устранение в окружающей человека среде канцерогенных агентов.
• Индивидуальную защиту организма, особенно на производстве
• Повышение общей и противоопухолевой устойчивости организма.
• Своевременное (максимально раннее) обнаружение и ликвидацию так называемых предопухолевых состояний.
ПРИНЦИПЫ ЛЕЧЕНИЯ ОПУХОЛЕЙ Общие подходы
Лечение опухолей может быть радикальным и паллиативным.
|
|
|
Радикальное лечениенаправлено на ликвидацию опухоли и предполагает возможность полного выздоровления либо длительной ремиссии.
Паллиативное лечениеприменяют при невозможности проведения радикальной терапии. Лечение приводит к удлинению жизни и уменьшению страданий. Риск рецидива достаточно велик, хотя первоначально больной может чувствовать себя полностью здоровым.
Большинство онкологических больных лечат хирургически и с применением лучевой терапии, химиотерапии и иммунотерапии. Выбор метода лечения зависит от характера заболевания, стадии, гистологического типа опухоли, возраста больного, наличия сопутствующих заболеваний и цели лечения (излечение или паллиативное вмешательство).
Хирургическое вмешательствои лучевая терапиявоздействует на первичную опухоль и регионарные лимфатические узлы. Ни тот, ни другой метод не влияет на области отдалённого распространения.
Химиотерапия и иммунотерапия— системные методы лечения, способны воздействовать на области отдалённого распространения.
Дополнительное лечение— системная терапия, применяемая после местного лечения (например, резекции) при высоком риске наличия микроскопического очага в лимфатических узлах или отдалённых органах. У значительной части таких больных развивается рецидив, цель дополнительного лечения — уничтожение этих удалённых и микроскопических очагов опухоли.
|
|
|
Комплексное лечениеиспользует преимущества каждого метода лечения для компенсации недостатков других.
71. Адаптационный синдром и стресс: характеристика понятий, причины, стадии, общие механизмы развития, роль в развитии патологических процессов.
Адаптационный процесс – общая реакция организма на действие чрезвычайного фактора внешней или внутренней среды, характеризующийся стадийными специфическими и неспецифическими изменениями жизнедеятельности, обеспечивающая повышение резистентности организма к воздействующему на него фактору и как следствие – приспособляемости его к меняющимся факторам существования.
Причины возникновения:
1.Экзогенные факторы
Физические (атмосферное давление, температура окр. среды и т. д.)
Химические (Содержание О2, голодание, потребление жидкости, интоксикации)
Биологические (инфекции, интоксикации экзогенными БАВ)
2.Эндогенные факторы
Недостаточность функций тканей, органов, систем
Дефицит или избыток БАВ(гормонов, ферментов)
Стадии:
1.Стадия срочной адаптации, заключается в мобилизации предсуществующих компенсаторных и защитных механизмов, характеризуется значительной активацией исследовательской функции, гиперфункции многих систем организма, мобилизацией органов и систем, которые реагируют на воздействие любого чрезвычайного фактора для данного организма
Механизмы:
- Активация нервной и эндокринной систем и, как следствие, увеличение в крови стрессорных гормонов и нейромедиаторов – адреналина, норадреналина, глюкокортикоидов и т. д.
- Увеличение содержания в клетках местных «мобилизаторов» функций (Са, цитокины, пептиды), что ведет к увеличению функций, катализируемых ими
- Изменения в мембранном аппарате клеток, интенсификация СПОЛ, липаз, протеаз
- усиление распада органических соединений, клеточных структур, мобилизация пластических ресурсов организма
- Увеличение функций всех органов
2. Стадия повышенной резистентности – стадия долговременной адаптации
- Формируется состояние специфической устойчивости к конкретному агенту и другим факторам
- Увеличение мощности и надежности функций органов и физиологических систем, обеспечивающих адаптацию к определенному фактору
- Устранение признаков стрессорной реакции, формируется эффективное приспособление организма
Всё это достигается путем перераспределения кровотока и активации генетического аппарата длительно гиперфункционирующих клеток.
3. Стадия истощения – эта стадия необязательна, в большинстве случаев адаптация завершается на предыдущей стадии. Наступление этой стадии может быть обусловлено многократным возникновением и изменением процессов адаптации. Возможности систем энергетического и пластического обмена истощаются, нарушается синтез структур, репарации нуклеиновых кислот и т. д.
Стресс – генерализованная неспецифическая реакция организма, возникающая под действием различных факторов необычного характера силы и/или действия.
Причины возникновения: те же, что и у адаптационного синдрома
72. Экстремальные состояния: характеристика понятия, основные формы; общая этиология, патогенез, стадии, принципы терапии.
Экстремальные состояния – общие тяжелые состояния организма, развивающиеся под действием экстремальных факторов внешней и внутренней среды, характеризующиеся значительными расстройствами жизнедеятельности организма, чреватыми смертью.
Общая этиология:
1. Экзогенные:
Физические (механические, электрические, термические, барометрические, гравитационные, радиационные)
Химические (дефицит/изб.кислорода, субстратов метаболитов, жидкости, интоксикации ЛС, ядами, кислотами)
Биологические (дефицит/избыток экзогенных БАВ, микробы, токсины)
2. Эндогенные:
Выраженная органная недостаточность
Кровопотеря
Кровоизлияния
Изб.продуктов иммунных реакций
Дефицит/изб. БАВ и их эффектов
Психические перенапряжения, травмы
Общий патогенез экстремальных состояний:
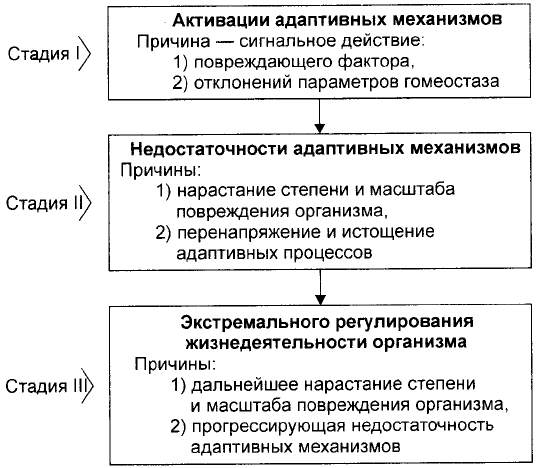
Проявления:
1.Стадия недостаточности механизмов адаптации:
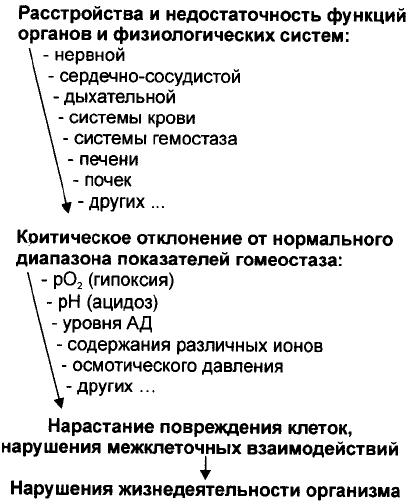
2. Стадия экстремального регулирования жизнедеятельности организма:
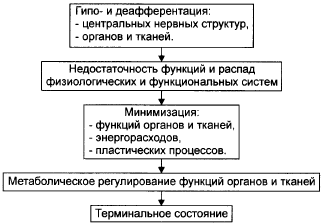
Терапия:
1. Этиотропная терапия:прекращение, снижение силы патогенного действия экстремального агента (остановка кровотечения, прекращение действия температуры, применение антитоксических в-в).
2. Патогенетическое лечение: блокировка механизмов развития экстремальных состояний.
3. Саногенетическая терапия: активация механизмов защиты, компенсации, приспособления и возмещения поврежденных структур и функций организма (стимуляция дыхания, почек, печени).
4. Симптоматическое лечение: устранение неприятных, усугубляющих состояние симптомов (головная голь, чувства страха смерти).
73. Шок: характеристика понятия, виды, этиология, патогенез, проявления, принципы лечения
Шок – общее, крайне тяжелое состояние организма, возникающее под действием сверхсильных экстремальных факторов. Характеризуется стадийным прогрессирующим расстройством жизнедеятельности организма в результате нарастающего нарушения функций нервной, эндокринной, сердечно-сосудистой систем.
Причины:
Различные варианты травм (механическое повреждение — разрушение, разрывы, отрывы, раздавливание тканей; обширные ожоги, воздействие электрического тока).
Массивная кровопотеря (как правило, сочетающаяся с травмой).
Переливание большого объёма несовместимой крови.
Попадание во внутреннюю среду сенсибилизированного организма аллергенов.
Значительная ишемия или обширный некроз органов (сердца, почек, печени, кишечника).
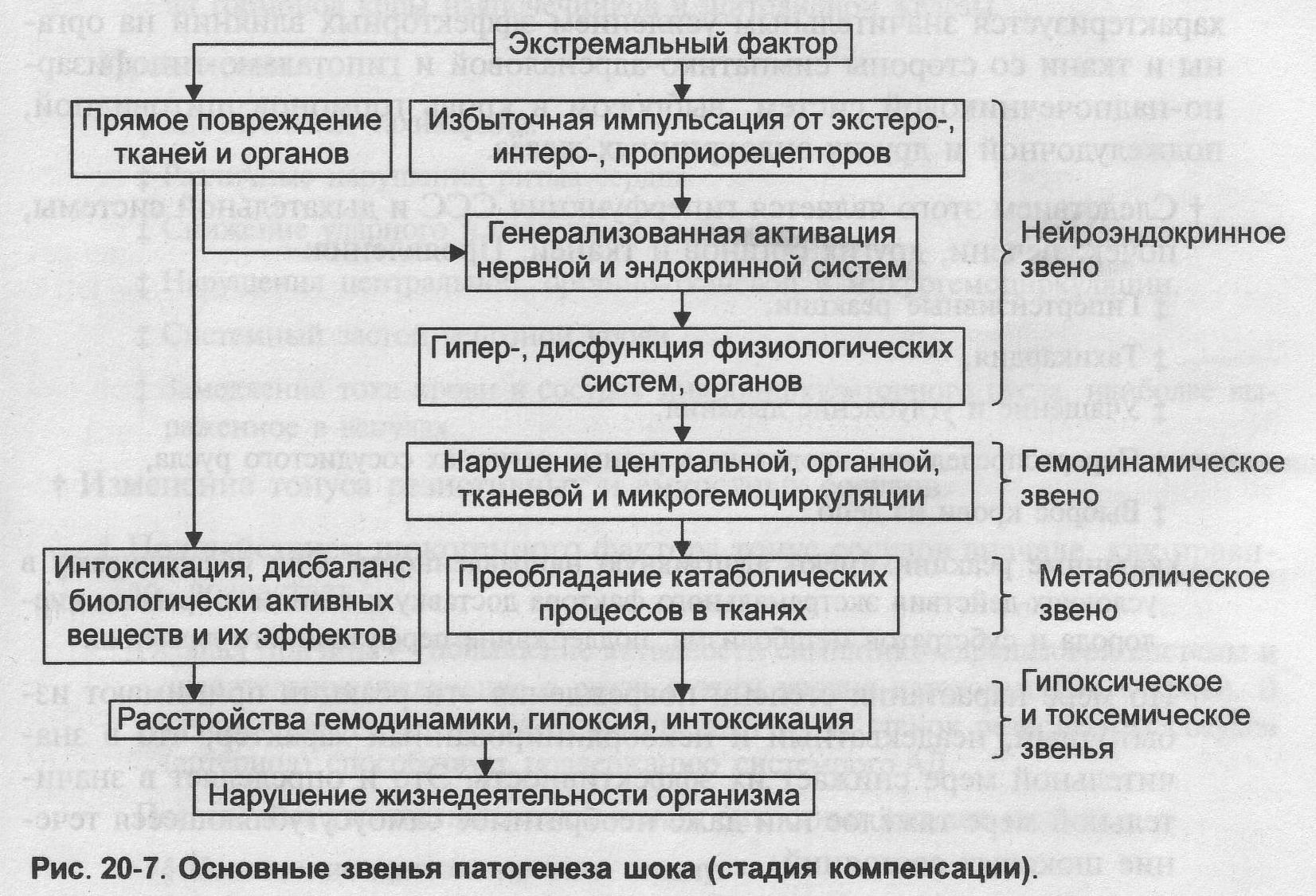
Проявление шока (стадия компенсации):
Нервная и эндокринная: психическое и двигательное возбуждение, активация симпатико-адреналовой систем.
ССС: тахикардия, гипертензивные реакции, централизация кровообращения, аритмии.
Легкие: тахипноэ с развитием гипокапнии
Печень: активация гликогенолиза, снижение дезинтоксикационной функции.
Почки: Олигурия, уремия.
Проявления шока (стадия декомпенсации):
Нервная и эндокринная: Психическая и двигательная заторможенность, спутанность сознания, низкая эффективность нейроэндокринной регуляции, гипорефлексия.
ССС: Сердечная недостаточность, аритмии, артериальная гипотензия и коллапс, перераспределение кровотока, капилляротрофическая недостаточность.
Легкие: дыхательная недостаточность (шоковые легкие)
Система крови и гемостаза: депонирование крови, изменение вязкости крови, тромбогеморрагический синдром.
Печень: печеночная недостаточность (шоковая печень).
Почки: почечная недостаточность (шоковые почки).
Виды шока:
С учётом: шок травматический (раневой), ожоговый, посттрансфузионный, аллергический (анафилактический), электрический, кардиогенный, токсический, психогенный (психический).В практической медицине шоковые состояния подразделяют в зависимости от тяжести их течения: шок I степени (лёгкий), шок II степени (средней тяжести), шок III степени (тяжёлый).
Стадии:
1. активация специфических и неспецифических адаптивных реакций. Эту стадию ранее называли стадией генерализованного возбуждения. Адаптивная, компенсаторная, непрогрессирующая, ранняя.
2. Если процессы адаптации недостаточны, развивается вторая стадия шока. Стадия деадаптации, или декомпенсации (стадия общего торможения).. На этой стадии выделяют две подстадии: прогрессирующую (заключающуюся в истощении компенсаторных реакций и гапоперфузии тканей) и необратимую (в ходе которой развиваются изменения, не совместимые с жизнью).
Принципы лечения: этиотропная терапия – устранение действия шокогенного фактора (прекращение воздействия повреждающего агента).
Патогенетическая терапия: устранение расстройств центральной, органо-тканевой и микроциркуляции; ликвидация степени расстройств кровоснабжения, устранение недостаточность внешнего дыхания.
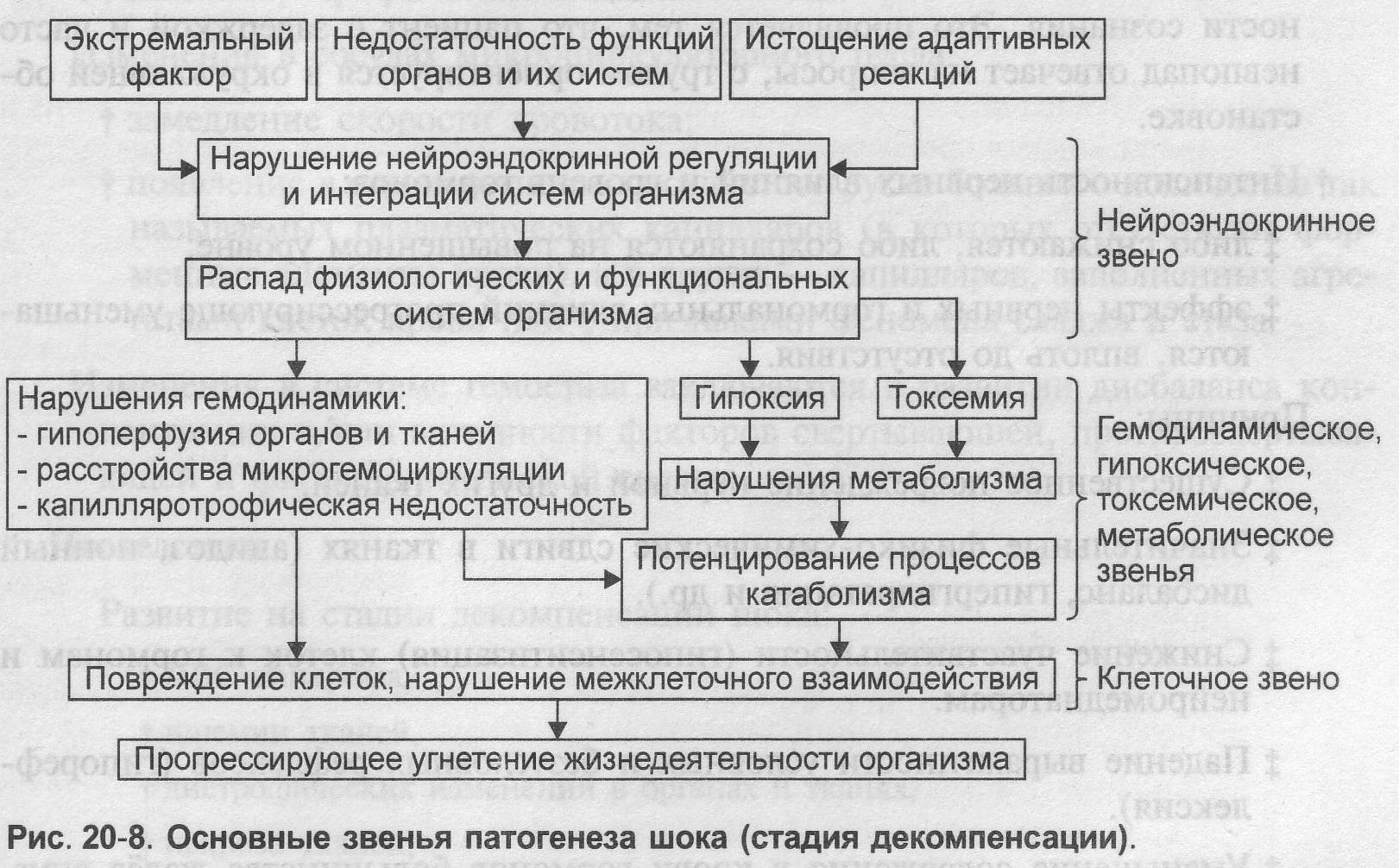
74. Кома: характеристика понятия, этиология, общий патогенез, проявления; принципы терапии коматозных состояний
Кома— состояние ареактивности, из которого больного невозможно вывести путём стимуляции, при глубокой коме могут отсутствовать даже примитивные защитные рефлексы: умеренная (I), глубокая (II), запредельная (III).
Причины комы:
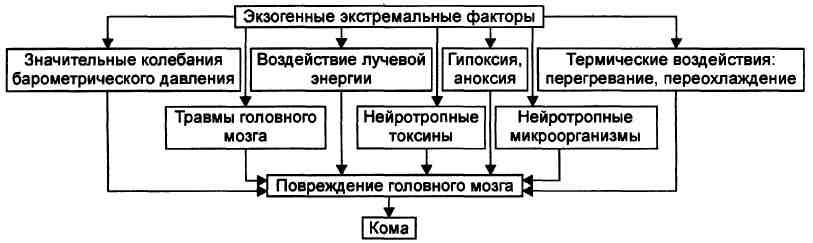 Экзогенные и эндогенные (могут быть инфекционными и неинфекционными).
Экзогенные и эндогенные (могут быть инфекционными и неинфекционными).
Экзогенные факторы — патогенные агенты окружающей среды, чрезвычайной силы, токсичности и/или разрушительного характера.
Эндогенные факторы,приводящие к развитию комы, являются результатом тяжёлых расстройств жизнедеятельности организма. Они наблюдаются при неблагоприятном течении различных болезней и болезненных состояний. Эти состояния приводят к значительным отклонениям от нормы жизненно важных параметров и констант, избытку или дефициту субстратов обмена веществ и/или кислорода в организме.
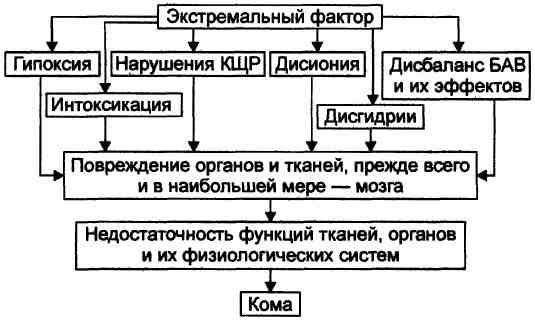 Патогенез и проявления:
Патогенез и проявления:
Патогенез коматозных состояний, независимо от вызвавших их причин, включает несколько общих ключевых звеньев.
Гипоксия, нарушения процессов энергообеспечения клеток, интоксикация, расстройства КЩР, дисбаланс ионов и жидкости, нарушения электрогенеза, дисбаланс содержания БАВ и их эффектов развиваются во всех органах и тканях.
Нервная система: расстройство сознания, потеря сознания;
ССС- сердечная недостаточность, аритмии, артериальная гипотензия, коллапс.
Легкие – дыхательная недостаточность;
Система крови – депонирование крови, изменение вязкости;
Печень – печеночная недостаточность;
Почки – почечная недостаточность.
Принципы терапии: 1. этиотропное лечение: при травматической коме – устраняется повреждающий фактор, применяется обезболивание. При коме, вызванной интоксикацией – антидоты, антитоксины, диуретики. При диабетической коме – инсулин.
2. патогенетическая терапия – антигипоксическая терапия (ИВЛ, введение антиоксидантов).; устранение степени интоксикации организма (переливание крови, плазмы). 3. нормализация показателей КЩР и уровня БАВ (используют гормоны надпочечников, поджелудочной железы).
4. систематическая терапия – устранение судорог, боли, оптимизация функций органов (противосудорожные средства, болеутоляющие).
75. Нарушения объёма крови и гематокрита: олиго- и полицитемическая нормоволемия. Гипо- и гиперволемические состояния: виды, причины, механизмы развития
Олигоцитемическая нормоволемия - состояние, характеризующееся нормальным общим объемом крови при уменьшении количества её форменных элементов (главным образом эритроцитов), что сопровождается падением величины гематокрита ниже нормы.
Основные причины олигоцитемической нормоволемии:
1. Массированный гемолиз эритроцитов; 2. Длительное и выраженное угнетение гемопоэза, главным образом эритропоэза. 3.Состояния после острой значительной кровопотери.
Проявления олигоцитемической нормоволемии:
1. Анемия (в связи со снижением числа эритроцитов) и как следствие — гемическая гипоксия.
2. Тромбоцитопения.
3. Снижение свёртываемости крови, сочетающееся нередко с геморрагическим синдромом.
4. Лейкопения, обусловливающая понижение противоинфекционной резистентности организма.
5. Уменьшение вязкости крови.
Полицитемическая нормоволемия — состояние, характеризующееся нормальным общим объёмом крови при увеличении числа её форменных элементов, что сопровождается увеличением Ht выше нормы.
Причины полицитемической нормоволемии: инфузии пациентам фракций форменных элементов крови (эритроцитной, лейкоцитной или тромбоцитной массы), хроническая гипоксия (вызывает эритроцитоз вследствие активации эритропоэза) и эритремии.
Проявления полицитемической нормоволемии: увеличение показателя вязкости крови, развитие тромботического синдрома, нарушения микрогемо-циркуляции (замедление тока крови в микрососудах, стаз), которые обусловливают снижение транскапиллярного обмена в тканях, а также артериальная гипертензия (например, в результате увеличения сердечного выброса).
Гиперволемии — состояния, характеризующиеся увеличением общего объёма крови и обычно изменением Ht. Различают нормоцитемическую, олигоците-мическую и полицитемическую гиперволемии.
Нормоцитемическая гиперволемия — состояние, проявляющееся эквивалентным увеличением объёма форменных элементов и жидкой части ОЦК. Ht остаётся в пределах нормы.
Основные причины: переливание большого объёма крови острые гипоксические состояния, сопровождающиеся выбросом крови из её депо, а также значительная физическая нагрузка, приводящая к гипоксии.
Олигоцитемическая гиперволемия – увеличение общего объема крови вследствие возрастания её жидкой части. Показатель Ht при этом ниже нормы.
Причины олигоцитемической гиперволемии.
1. Избыточное поступление в организм жидкости при патологической жажде и введении в сосудистое русло большого количества плазмы крови.
2. Снижение выведения жидкости из организма в результате недостаточности экскреторной функции почек, гиперпродукции АДГ, гиперосмоляльности плазмы крови.
Полицитемическая гиперволемия - состояние, проявляющееся увеличением общего объема крови вследствие преимущественного повышения числа её форменных элементов. В связи с этим Ht превышает верхнюю границу нормы.
Проявления гиперволемий – увеличении сердечного выброса и повышение АД.
Гиповолемии- состояния, характеризующиеся уменьшением общего объёма крови и, как правило, нарушением соотношения её форменных элементов и плазмы. Различают нормоцитемическую, олигоцитемическую и полицитемическую гиповолемии.
Нормоцитемическая гиповолемия - состояние, проявляющееся уменьшением общего объёма крови при сохранении Ht в пределах нормы. Наиболее частые причины нормоцитемической гиповолемии: острая кровопотеря, шоковые состояния, вазодилатационный коллапс.
Олигоцитемическая гиповолемия - состояние, характеризующееся уменьшением общего объёма крови с преимущественным снижением числа её форменных элементов. Ht при этом ниже нормы. Частые причины – состояния после острой кровопотери.
Проявления олигоцитемической гиповолемии: 1. Снижение показателя кислородной ёмкости крови 2. Признаки гипоксии 3.Расстройства органотканевого кровообращения и микрогемоциркуляции..
Полицитемическая гиповолемия - состояние, при котором снижение общего объема крови в организме обусловлено в основном уменьшением объёма плазмы. Показатель Ht при этом состоянии выше диапазона нормы.
Причины полицитемической гиповолемии:1. Состояния, вызывающие повышенную потерю организмом жидкости- повторная рвота, длительная диарея, полиурия 2. Состояния, препятствующие достаточному поступлению жидкости в организм водное «голодание»: отсутствие питьевой воды и невозможность питья воды.
Проявления полицитемическойгиповолемии:
1. Нарушения органотканевой микрогемоциркуляции в связи с гиповолемией и полицитемией.
2. Повышение вязкости крови, агрегация форменных элементов крови в микрососудах органов и тканей и диссеминированный микротромбоз.
Дата добавления: 2018-04-15; просмотров: 2645; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
