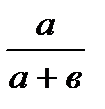Опыт 1. Влияние концентрации реагирующих веществ на скорость химической реакции
В настоящем опыте исследуется влияние концентрации реагентов на скорость взаимодействия тиосульфата натрия с серной кислотой
Na2S2O3+ H2SO4 = Na2SO4 + SO2 + S + H2O
О скорости реакции можно судить по времени, прошедшем от начала реакции до момента появления в объеме раствора серы (желтоватая муть).
В четыре пробирки налить из бюретки по 6 мл 0,5М раствора серной кислоты. В четыре пронумерованных стаканчика (по 50мл) налить указанное в табл. 1 количество
33
0,5М раствора тиосульфата натрия и воды. Вылить в стаканчик №1 отмеренные 6 мл серной кислоты, быстро перемешать и измерить время (секунды) до начала появления в объеме раствора мути. Скорость реакции определить как величину, обратно пропорциональную найденному времени. Повторить опыт со стаканчиками №2-№4 и данные занести в табл. 1.
Таблица 1
| № стакана | Объем раствора, мл
| Относительная концентрация Na2S2O3
| Время (t), с | Скорость реакции V = 1/t,с-1 | |
| Na2S2O3 а | H2O в | ||||
| 1 | 6 | 0 | 1 | ||
| 2 | 4 | 2 | 2/3 | ||
| 3 | 3 | 3 | 1/2 | ||
| 4 | 2 | 4 | 1/3 | ||
Результаты наблюдений представить в виде графика: по оси абсцисс отложить относительную концентрацию раствора тиосульфата натрия, по оси ординат – скорость реакции.
Сделать вывод о зависимости скорости реакции от концентрации реагентов.
Опыт 2. Влияние величины поверхности раздела реагирующих веществ на скорость гетерогенной химической реакции
а) налить в две пробирки на ¼ их объема 2М раствор соляной кислоты. Выбрать два одинаковых кусочка CaCO3(тв) (мел, мрамор и т.д.), поместить один из них в фарфоровую ступку и растереть в порошок. Пересыпать порошок на листок бумаги. Одновременно в первую пробирку бросить кусочек мела, а во вторую – порошок. Наблюдать выделение газа. В какой из пробирок реакция протекает быстрее? Объяснить наблюдаемое, записать уравнение реакции.
34
б) в сухой фарфоровой ступке смешать небольшое количество сухих солей KI и Pb(NO3)2 . Происходит ли изменение окраски?
Растереть смесь пестиком и наблюдать изменение окраски. Составить уравнение реакции. Из капельницы добавить несколько капель воды: смесь моментально окрашивается в ярко-желтый цвет. Дать объяснение проведенному опыту.
Опыт 3. Влияние катализатора на скорость химической реакции
а) гетерогенный катализ. В три пробирки налить по ¼ объема перекиси водорода. Одновременно добавить: в первую пробирку – оксид марганца (II) (MnO2), во-вторую – оксид кремния (IV) (SiO2), в третью – оксид железа (II) (FeO). Наблюдать реакцию разложения перекиси водорода. Выделение кислорода можно определить, опустив в пробирку тлеющую лучинку. Одинаково ли быстро протекает реакция в пробирках? Какое вещество не является катализатором реакции разложения? Записать уравнение реакции.
б) гомогенный катализ. В две пробирки на 1/3 объема налить 0,5М раствор серной кислоты. В каждую пробирку бросить по кусочку цинка и добавить по 5 капель раствора перманганата калия (KМnO4). Одну пробирку оставить в качестве эталона, а в другую – добавить несколько кристаллов нитрата калия (KNO3) в качестве катализатора. В какой из пробирок обесцвечивание раствора происходит быстрее? Запишите суммарную реакцию.
При взаимодействии металлического цинка с раствором серной кислоты образуется атомарный водород, который рекомбинируя, выделяется в виде газа Н2. В первой пробирке восстановление перманганата калия происходит непосред-ственно атомарным водородом (реакция протекает довольно медленно). Во второй пробирке атомарный водород вначале восстанавливает ион NO3- до иона NO2-, который реагирует с перманганатом калия значительно быстрее.
35
При этом ион MnO4- восстанавливается до Mn2+, а ион NO2- вновь окисляется до NO3-.
1) Zn + H2SO4 = ZnSO4 + 2H
2) 2H = H2 – рекомбинация
3) 5KNO3 + 10H = 5KNO2 + 5H2O
4) 5KNO2 + 2KMnO4 + 3H2SO4 = 5KNO3 + 2MnSO4 + K2SO4 + 3H2O
Таким образом, нитрат калия, участвуя в промежуточных стадиях процесса, способствует более быстрому протеканию реакции восстановления перманганата калия. Сам же KNO3 в результате реакции не расходуется и остается в первоначально взятом количестве.
Дата добавления: 2018-04-04; просмотров: 1393; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!