ПРИМЕРЫ РЕШЕНИЯ ТИПОВЫХ ЗАДАЧ
Задача 1
Как изменится скорость прямой реакции (Т=const) 2SO2(г) + O2(г) ⇄ 2SO3(г) при увеличении общего давления в реакционном сосуде в три раза?
Решение. Из уравнения Клапейрона–Менделеева следует, что p = n/VRT = CRT, где С - концентрация в моль/л. Согласно закону действующих масс скорость прямой реакции до повышения давления 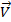 =
= 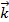 [SO2]2[O2]. После повышения давления в 3 раза концентрация всех газовых компонентов возрастет также в 3 раза, при этом константа скорости реакции останется неизменной, так как она не зависит от концентрации реагирующих веществ.
[SO2]2[O2]. После повышения давления в 3 раза концентрация всех газовых компонентов возрастет также в 3 раза, при этом константа скорости реакции останется неизменной, так как она не зависит от концентрации реагирующих веществ.
Уравнение скорости прямой реакции будет иметь следующий вид:  =
= 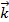 [3SO2]2[3O2] = 27
[3SO2]2[3O2] = 27 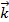 [SO2]2[O2].
[SO2]2[O2].
Таким образом, скорость прямой реакции возрастет в 27 раз.
Задача 2 
Для реакции 2NO2(г) ⇄ 2NO(г) + O2(г) константа скорости прямой реакции при 600К равна 83,9 л/моль∙с, а при 645К она составляет 407л/моль∙с. Рассчитать энергию активации этого процесса.
17
Решение. Константа скорости реакции связана с энергией активации уравнением Аррениуса
 ,
,
в котором предэкспоненциальный множитель А0 и энергия активации Еа считаются независимыми от температуры. Перейдя к десятичным логарифмам и прологарифмировав уравнение, получим lgk =  + lgA0. Запишем это уравнение для двух температур:
+ lgA0. Запишем это уравнение для двух температур:
lgk1 =  + lgA0 ; lgk2 =
+ lgA0 ; lgk2 =  + lgA0 .
+ lgA0 .
Вычитая из второго уравнения первое и решая относи-тельно энергии активации, получим Ea =  lg
lg  . Подставляя численные значения величин в это уравнение, получим Еа =
. Подставляя численные значения величин в это уравнение, получим Еа =  lg
lg  = 113,2 кДж/моль.
= 113,2 кДж/моль.
|
|
|
Задача 3
При 5000С равновесие реакции N2(г) + 3H2(г) ⇄ 2NH3(г) установилось при следующих концентрациях (моль/л) реагентов: [N2] = 1,8; [H2] = 7,4; [NH3] = 0,4. Определить: а) исходные концентрации азота и водорода; б) давление в реакционном сосуде в начальный момент и в момент наступления равновесия.
Решение. Обозначим исходные концентрации веществ как [N2]исх, [H2]исх, количество исходных веществ, прореагиро-вавших к моменту наступления равновесия, как [N2]изр, [H2]изр, а равновесные концентрации как [N2]равн, [H2]равн, [NH3]равн. В начальный момент времени в реакционной смеси присутствуют только азот и водород в начальных концентрациях. В процессе реакции их концентрации убывают, а концентрация аммиака увеличивается. После установления равновесия (когда скорости прямой и обратной реакций равны) в равновесной смеси присутствуют не успевшие прореагировать азот и водород и успевший
18
образоваться аммиак, таким образом равновесные концен-трации исходных веществ будут равны разности между их исходными концентрациями и тем количеством, которое прореагировало к моменту равновесия
[N2]равн = [N2]исх - [N2]изр; [H2]равн = [H2]исх - [H2]изр.
|
|
|
Равновесные концентрации всех веществ даны в условии задачи, остается определить количества азота и водорода прореагировавших к моменту равновесия. Из уравнения реакции следует, что на каждые 2 моля образовавшегося аммиака затрачивается 1 моль азота и три моля водорода. По условию задачи к моменту равновесия успело образоваться 0,4 моля аммиака. Для этого потребовалось:
из 3 молей H2 образуется 2 моля NH3, а
из Х молей H2 образуется 0,4 моля NH3,
откуда Х =  = 0,6 моля = [H2]изр.
= 0,6 моля = [H2]изр.
Аналогично находим, что к моменту равновесия израсходовалось [N2]изр =  = 0,2 моля.
= 0,2 моля.
Рассчитаем исходные концентрации веществ
[N2]исх = [N2]равн + [N2]изр = 1,8 + 0,2 = 2,0 моль/л; [H2]исх = [H2]равн + [H2]изр = 7,4 + 0,6 = 8,0 моль/л.
Для решения этой задачи удобно составить схему:
N2(г) + 3H2(г) ⇄ 2 NH3 (г)
Сисх 2,0 8,0 0
Сизр 0,2 0,6 0
Сравн 1,8 7,4 0,4
С помощью этой схемы можно сделать любые расчеты, учитывая условия задачи;
б) согласно условию, Т = 500 + 273 = 773К, V= 1л. Исходное число молей реагентов nнач = nначN2 + nначH2 = 2 + 8 = 10 молей. В состоянии равновесия число молей газов будет равно nравн = nравн H2 + nравнN2 + nравнNH3 = 7,4 + 1,8 + 0,4 = 9,6 моль.
|
|
|
19
Подставляя полученные значения в уравнение ( P = CRT), рассчитаем давление газовой смеси в начальный момент и в момент равновесия (R=8,31Дж/моль∙К=0,082 л∙атм/моль∙град).
Рнач = 10∙0,082∙773 = 633,86 атм;
Рравн = 9,6∙0,082∙773 = 608,5 атм.
Очевидно, что давление к моменту равновесия умень-шилось, так как реакция идет с убылью числа молей газов.
Задача 4
При 250С для реакции 1) SO2(г) + 1/2O2(г) ⇄ SO3(г)  = 1,7∙1012. Рассчитать Кр и Кс при этой температуре для реакции 2) 2SO3(г) ⇄ 2SO2(г) + O2(г)
= 1,7∙1012. Рассчитать Кр и Кс при этой температуре для реакции 2) 2SO3(г) ⇄ 2SO2(г) + O2(г)
Решение. Согласно закону действующих масс для реакции 1) выражение константы химического равновесия будет иметь вид
 =
=  , а для реакции 2)
, а для реакции 2)  =
= 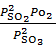 . Нетрудно установить, что между
. Нетрудно установить, что между  и
и  существует связь в виде
существует связь в виде  =
=  . Подставляя численные значения, получим:
. Подставляя численные значения, получим:  =
=  = 0,345∙10-24.
= 0,345∙10-24.
Известно, что а) Кр = Кс (RT) Dn , где Dn = ånпрод. - ånисх.веществ –изменение числа молей газообразных веществ в ходе реакции. Для реакции 2) Dn = (2+1) – 2 =1моль. Подставляя в уравнение а) Т = 298К, R = 0,082 л∙атм/моль∙К, получим
Кс =  = 1,4∙10-26.
= 1,4∙10-26.
Задача 5
Для реакции CO(г) + Cl2(г) ⇄ COCl2(г) вычислить константу равновесия Кр, используя табличные значения термо-динамических функций при стандартных условиях. По значению величины Кр ответить на вопрос: исходные вещества или продукты реакции преобладают в равновесной смеси?
|
|
|
20
Решение. Константа равновесия реакции связана со стандартным изменением свободной энергии Гиббса соотношением DG0х.р = - 2,303RT lgKp (1). В свою очередь, DG0х.р (химической реакции) можно рассчитать по изменению стандартных величин энтальпии и энтропии в ходе этой реакции DG0х.р = DН0х.р - ТDS0х.р∙10-3 (2). Значения DН0х.р и DS0х.р вычисляют по первому следствию из закона Гесса, используя табличные значения стандартных энтальпий образования и энтропий веществ DН0х.р. = å(DН0298)кон - å(DН0298)исх и DS0х.р = å(S0298)кон - å(S0298)исх. Значения DН0298 и S0298 веществ, участвующих в реакции, приведены в таблице.
| Вещество | DН0298, кДж/моль | S0298, Дж/моль∙К |
| CO (г) | -110,6 | 197,7 |
| Cl2(г) | 0 | 222,9 |
| COCl 2 (г) | -220,3 | 283,9 |
DН0х.р = DН0298 (COCl2) - DН0298(Cl2) - DН0298(CO) =
= -220,3 – 0 – (-110,6) = -109,7кДж
DS0х.р = S0298(COCl2) - S0298(Cl2) - S0298(CO) =
= 283,9 – 222,9 – 197,7 = -136,7 Дж/К
DG0х.р = -109,7 – 298 ∙(-136,7)∙10-3 = - 69,3 кДж
Из уравнения (1) следует
lgКр =  =
= 
 = 12,13 Кр= 1012,13, так как Кр >> 1, то при Т = 298К в равновесной смеси будут преобладать продукты реакции.
= 12,13 Кр= 1012,13, так как Кр >> 1, то при Т = 298К в равновесной смеси будут преобладать продукты реакции.
Задача 6
При некоторой температуре константа равновесия реакции H2(г) + I2(г) ⇄ 2HI(г) равна 50. Рассчитать равновесные концентрации веществ, если исходные концентрации водорода и йода были соответственно 0,6 и 0,8 моль/л.
Решение. Предположим, что к моменту равновесия прореагировало x молей водорода и, значит, х молей йода.
21
Тогда их равновесные концентрации будут  = 0,6 - х моль/л ,
= 0,6 - х моль/л ,  ) = 0,8 - х моль/л, а равновесная концентрация йодистого водорода составит
) = 0,8 - х моль/л, а равновесная концентрация йодистого водорода составит  = 2х моль/л. Выражение константы равновесия для этой реакции будет Кс =
= 2х моль/л. Выражение константы равновесия для этой реакции будет Кс =  .
.
Подставляя в него соответствующие выражения, получим 50 =  , откуда х2 - 1,52х + 0,52 = 0,
, откуда х2 - 1,52х + 0,52 = 0,
х1,2 = 0,76 ± 0,24, х1 = 1, х2 = 0,52.
Первое значение не подходит по смыслу, так как уменьшение концентрации не может быть больше, чем исходные концентрации водорода и йода. Поэтому искомое значение х составляет 0,52моль/л. Следовательно, равновесные концентрации веществ будут равны:  = 0,6 - 0,52 = = 0,08 моль/л,
= 0,6 - 0,52 = = 0,08 моль/л,  = 0,8 - 0,52 = 0,28 моль/л,
= 0,8 - 0,52 = 0,28 моль/л,  = = 2∙0,52 = 1,04 моль/л.
= = 2∙0,52 = 1,04 моль/л.
Задача 7
Для реакции CaCO3(тв) ⇄ CaO(тв) + CO2 (г) при 6000С и 7000С равновесные парциальные давления CO2 соответственно равны 0,0024 атм и 0,029 атм. Определить: 1) константы равновесия 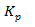 для данных температур; 2) тепловой эффект реакции при Р = const, считая его постоянным для интервала температур 600-7000С.
для данных температур; 2) тепловой эффект реакции при Р = const, считая его постоянным для интервала температур 600-7000С.
Решение. 1) реакция термического разложения карбоната кальция является гетерогенным процессом. Выражение константы равновесия будет  =
=  . Следовательно, при указанных температурах константы равновесия будут иметь следующие значения:
. Следовательно, при указанных температурах константы равновесия будут иметь следующие значения:  = 0,0024 и
= 0,0024 и  = 0,029.
= 0,029.
2) Тепловой эффект при Р,Т = const равен изменению энтальпии химической реакции DН0х.р. Для расчета DН0х.р можно воспользоваться следующим уравнением:
22
DН0х.р =  lg
lg 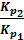 =
= 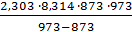 lg
lg  = = 176,65 кДж.
= = 176,65 кДж.
КОНТРОЛЬНЫЕ ЗАДАЧИ
1. Во сколько раз изменится скорость прямой реакции (реакцию считать элементарной) при изменении давления в n раз?
а) 2C(тв) + H2(г) ⇄ C2H2(г) м) CO2(г)+ H2(г) ⇄ CO(г) + H2O(ж)
б) 2CO(г) + O2(г) ⇄ 2CO2(г) н) N2(г) + O2(г) ⇄ 2NO(г)
в) 2C(тв) + O2(г) ⇄ 2CO(г) o) H2(г) + I2(г) ⇄ 2HI(г)
г) 2NO(г) + Cl2(г) ⇄ 2NOCl(г) п) 2NO(г) + O2(г) ⇄ 2NO2(г)
д) CO(г) + H2O(г) ⇄ H2(г) + CO2(г) р) 2HI(г) ⇄ H2(г) + I2(г)
е) C(тв) + 2H2(г) ⇄ CH4(г) c) C(тв) + O2(г) ⇄ CO2(г)
ж) PCl5(г) ⇄ PCl3(г) + Cl2(г) т) COCl2(г) ⇄ CO(г) + Cl2(г) з)SO2Cl2(г) ⇄ SO2(г) + Cl2(г) у) 2SO2(г) + O2(г) ⇄ 2SO3(г)
и) N2O4(г) ⇄ 2NO2(г) ф) H2(г) + 1/2O2(г) ⇄ H2O(г)
к) 2CO2(г) ⇄ O2(г) +2CO(г) x) 2NO(г) + O2(г) ⇄ N2O4(г)
л) CO(г) + MgO(тв) ⇄ CO2(г) + Mg(тв)
2.Во сколько раз надо увеличить давление в сосуде, чтобы скорость реакции H2(г) + I2(г) = 2HI(г) возросла в 100 раз?
3. Реакция идет по уравнению 2NO(г) + O2(г) ⇄ 2NO2(г) Начальные концентрации реагирующих веществ были [NO] = = 0,8 моль/л; [O2] = 0,6 моль/л. Как изменится скорость реакции, если концентрацию кислорода увеличить до 0,9 моль/л, а концентрацию оксида азота до 1,2 моль/л (Т = const)?
4. Скорость реакции H2(г) + I2(г) ⇄ 2HI(г) при [H2] = 0,5моль/л и [I2] = 0,3 моль/л равна 0,018 моль/ л∙мин. Рассчитать констан-ту скорости прямой реакции.
5. Скорость реакции 2NO(г) + O2(г) ⇄ 2NO2(г) при [NO] = = 0,3моль/л; [O2] = 0,15 моль/л равна 1,2 ∙10-3 моль/л∙с. Рассчи-тать константу скорости.
6. Константа скорости реакции образования HI из простых веществ при 781К равна 0,16. Чему равна скорость реакции в начальный момент времени, когда:
23
а) [I2] = 0,05 моль/л; [H2] = 0,09 моль/л; [HI] = 0 моль/л,
б) когда успело образоваться 0,04 моль/л HI.
7. Константа скорости реакции 2NO(г) + O2(г) ⇄ N2O4(г) при некоторой температуре равна 0,5∙10-3 л2 /мол2∙с. Рассчитать скорость реакции:
а) при [NO] = 0,8 моль/л, [O2] = 0,6 моль/л; [N2O4] = 0 моль/л
б) через некоторый промежуток времени, за который прореа-гировало 0,2 моль/л кислорода.
8. Разложение N2O на поверхности золота при высоких температурах протекает по уравнению 2N2O(г) ⇄ 2N2(г) + O2(г). Константа скорости данной реакции равна 5∙10-4 л∙моль-1∙ мин-1 при 1173К. Начальная концентрация [N2O] = 3,2 моль/л. Определите скорость реакции при заданной температуре в начальный момент времени и в тот момент, когда разложится 25% N2O.
9. Во сколько раз изменится скорость реакции при повы-шении температуры с 20 до 1000С, если g = 2?
10. Скорость некоторой реакции при охлаждении с 60 до 300С уменьшилась в 8 раз. Рассчитать g.
11. Рассчитать температурный коэффициент реакции, если ее скорость при 1200С составляла 5,88 ∙10-4 моль/л∙мин, а при 1700С она была равна 6,70∙10-2 моль/л∙мин.
12. При увеличении температуры на 600 скорость реакции возросла в 150 раз. Рассчитать температурный коэффициент.
13. При температуре 200С в результате некоторой реакции через 1час накопилось определенное количество продукта. При какой температуре следует вести процесс, чтобы то же количество продукта накопилось за 10 минут? g = 2,4.
14. На сколько градусов нужно повысить температуру, чтобы скорость реакции возросла в 90 раз? Температурный коэффициент равен 2,7.
15. Во сколько раз увеличится скорость растворения железа в 5%-ной HCl при повышении температуры на 32˚, если температурный коэффициент скорости растворения равен 2,8?
24
16. Определите температурный коэффициент скорости реакции, если при понижении температуры на 45˚ реакция замедлилась в 25 раз.
17. Какой должна быть энергия активации, чтобы скорость реакции увеличилась в 3 раза при возрастании температуры от 300 до 310К?
18. Энергия активации процесса термического разложения йодистого водорода равна 198 кДж/моль. Какая доля молекул обладает достаточной энергией, чтобы вступить в эту реакцию при температуре 500К?
19. Определить энергию активации реакции С12Н22О11 + Н2О = 2С6Н12О6, если константа скорости при 210С равна 4,42∙10-4, а при 410С = 7,35∙10-3.
20. Для реакции COCl2(г) ⇄ CO(г) + Cl2(г) константы скорости при 665К и 745К соответственно равны 0,53∙10-2 и 76,6∙10-2. Вычислить энергию активации.
21. Константа скорости реакции H2(г) + I2(г) ⇄ 2HI(г) при 781К равна 0,16. Энергия активации процесса равна 166,3 кДж/моль. Рассчитать константу скорости этой реакции при 900К. Предэкспоненциальный множитель считать незави-сящим от температуры.
22. Для реакции SO2(г) + 1/2 O2(г) ⇄ SO3(г) энергия актива-ции равна 249,9 кДж/моль. В присутствии платинового катали-затора энергия активации снижается до 62,4 кДж/моль. Во сколько раз изменится скорость реакции в присутствии катализатора при температуре 4000С. Предэкспоненциальный множитель считать независящим от температуры.
23.Энергия активации прямого процесса H2(г) + I2(г) ⇄ 2HI(г) равна 166,3кДж/моль, а для обратной реакции Еа = =182,9кДж/моль. Рассчитать DН0 химической реакции.
24. Во сколько раз увеличится скорость реакции, если при температуре 500К ее энергия активации, за счет введения в реакционную среду катализатора, уменьшится на а) 4 кДж/моль; б) 8кДж/моль; в) 12кДж/моль; г) 16кДж/моль; д) 20кДж/моль; е) 30кДж/моль; ж) 35кДж/моль; з) 40кДж/моль; и) 45кДж/моль. 25
25. Для следующих обратимых процессов:
а) N2(г) + 3H2(г) ⇄ 2NH3(г)
б) H2(г) + Cl2 (г) ⇄ 2HCl(г)
в) N2O4(г) ⇄ 2NO2(г)
г) CO(г) + H2O(г) ⇄ H2(г) + CO2(г)
д) СН4(г)+ 2О2(г) ⇄ СО2(г) + 2Н2О(г)
е) C(тв) + O2(г) ⇄ CO2(г)
ж) CO(г) +NO2(г) ⇄ CO2(г) + NO(г)
з) FeO(тв)+ CO(г) ⇄ Fe(тв)+ CO2(г)
и) 2NO(г) + Cl2(г) ⇄ 2NОCl(г)
к) COCl2(г) ⇄ CO(г) + Cl2(г)
л) 4HCl(г) + О2(г) ⇄ 2H2O(г) + 2Cl2(г)
м) 2C(тв) + O2(г) ⇄ 2CO(г)
н)3CO(г) + 2H2O(г) ⇄ СH3ОН(г) + 2CO2(г )
о) SO2(г) ⇄ S(ромб) +О2(г)
п) CO(г) + Cl2(г) ⇄ COCl 2(г)
р) CO(г) + 3H2(г) ⇄ H2О(г) + CН4(г)
с) Fe2O3(тв)+3H2(г) ⇄ 2Fe(тв)+ 3H2O(г)
т) 2C(тв) + H2(г) ⇄ C2H2(г)
1) записать математические выражения констант равновесия Кс и Кр;
2) вычислить соотношение между Кс и Кр при 250С;
3) используя таблицы термодинамических величин, найти значение Кр.
26. Для реакции N2O4(г) ⇄ 2NO2(г) Кр = 0,141 при 250С и Кр = 1,34 при 600С. На основании этих данных определить знак DН реакции (DН > 0 или DН < 0).
27. Для реакции SO2(г) + 1/2O2(г) ⇄ SO3(г) Кр = 2,043∙10-2 при 9000С и Кр = 1,062∙10-2 при 9500С. На основании этих данных определить знак DН реакции. (DН>0 или DН<0).
28. По данным значениям констант равновесия найти значения DG0 химических реакций.
26
| № | Процесс | Т, К | Кр |
| 1 | C(тв) + O2(г) ⇄ CO2(г) | 1300 | 4,17∙1015 |
| 2 | N2O4(г) ⇄ 2NO2(г) | 298 | 0.141 |
| 3 | N2(г) + 3H2(г) ⇄ 2NH3(г) | 298 | 6.3·105 |
| 4 | SO2(г) + 1/2O2(г) ⇄ SO3(г) | 298 | 1.7∙1012 |
| 5 | H2(г) + D2(г) ⇄ 2HD(г) | 670 | 3,78 |
| 6 | 2CO2(г) ⇄ O2(г) +2CO(г) | 1393 | 1,4∙10-12 |
| 7 | CН4(г) + 2H2S(г) ⇄ CS2(г) + 4H2(г) | 298 | 2,05·109 |
| 8 | CO2)г)+ H2(г) ⇄ CO(г) + H2O(г) | 1023 | 0,77 |
| 9 | 2HI(г) ⇄ H2(г) + I2(г) | 698 | 1,83∙10-2 |
| 10 | 4HCl(г) + О2(г) ⇄ 2H2O(г) + 2Cl2(г) | 703 | 40,33 |
| 11 | H2O(г) ⇄ H2(г) + 1/2O2(г) | 1600 | 6,53·10-6 |
| 12 | C2H6(г) ⇄ C2H4(г) + H2(г) | 900 | 5,02∙10-2 |
29. Для реакции N2(г) + O2(г) ⇄ 2NO(г) Кр = 4,08∙10-4 при 2000К и Кр=3,60∙10-3 при 2500К. На основании этих данных определить знак DН реакции. (DН>0 или DН<0).
30. Для реакции Н2(г) ⇄ 2Н(г) Кр = 1,52∙10-7 при 1800К и Кр = 3,10∙10-6 при 2000К. На основании этих данных определить знак DН реакции. (DН>0 или DН<0).
31. Константа равновесия Кр реакции
2SO2(г) + O2(г) ⇄ 2SO3(г) при 950К равна 1,062∙10-2 . Вычислите Кс для этой реакции.
32. При 873К константа равновесия Кс реакции CO(г) + Cl2(г) ⇄ COCl2(г) равна 12,12. Вычислите Кр реакции при этой температуре.
33. DG0298 образования NH3 равна -16,64 кДж/моль. Вычислите Кр реакции N2(г) + 3H2(г) ⇄ 2NH3(г) для данной температуры.
34. Реакция хлорирования монооксида углерода протекает
27
по схеме CO(г) + Cl2(г) ⇄ COCl2(г). Исходные концентрации СО и Cl2 были, соответственно, 0,5 и 0,2 моль/л. Вычислить концентрации всех веществ в момент времени, когда концентрация хлора стала 0,1 моль/л.
35. Концентрации веществ в реакции
CO(г) + H2O(г) ⇄ H2(г) + CO2(г) составляли: [CO] = 0,2 моль/л, [H2O] = 0,4 моль/л, [CO2] = 0,3 моль/л, [H2] = 0,1 моль/л. Вычислить концентрации всех веществ в момент, когда прореагировало 40% СО.
36. Исходные концентрации монооксида азота и хлора в системе 2NO(г) + Cl2(г) ⇄ 2NОCl(г) составляют соответственно 0,4 моль/л и 0,3 моль/л. Вычислить Кс, если при этой темпера-туре к моменту равновесия прореагировало 20% NO. Рассчи-тать, как при этом изменится давление в реакционном сосуде?
37. Рассчитать константу равновесия Кс реакции N2O4 (г) ⇄ 2NO2(г), если исходная концентрация N2O4 равна 0,02 моль/л и к моменту равновесия прореагировало 60% этого количества.
38. Иодистый водород при нагревании диссоциирует по уравнению 2HI (г) ⇄ H2(г) + I2(г) . При некоторой температуре Кс = 1,64. Рассчитать количество HI (в процентах), подверг-шееся диссоциации при данной температуре, если его исходная концентрация составляла 4 моль/л.
39. Константа равновесия реакции H2(г) + I2(г) ⇄ 2HI(г) при некоторой температуре равна 50. Сколько молей йодистого водорода получится, если нагреть до этой температуры в замкнутом сосуде объемом 1л 0,5 молей водорода и 1 моль иода?
40. При температуре 4940С в системе
2NO(г) + O2(г) ⇄ 2NO2(г) в момент равновесия концентрация кислорода стала 0,1 моль/л, а концентрация двуокиси азота – 0,25 моль/л. Определить исходную концентрацию монооксида азота, если для данной температуры Кс = 2,2.
41. При нагревании смеси CO2 и H2 в закрытом сосуде
28
установилось равновесие CO2 (г)+ H2 (г) ⇄ CO(г) + H2O(г). При Т= =1123К Кс = 1. Сколько молей диоксида углерода надо взять на 1 моль водорода, чтобы 70% последнего превратилось в воду?
42. Вычислить степень диссоциации (a) молекулярного хлора на атомы Cl2(г) ⇄ 2Cl(г), если Кс = 4,2∙10-4 , а исходная концентрация молекулярного хлора составляла 0,5 моль/л.
43. При 2500С для процесса PCl5 (г) ⇄ PCl3(г) + Cl2(г) Кс = 0,041. Сколько молей PCl5 при этой температуре было помещено в литровый сосуд, если в момент равновесия концентрация хлора была 0,1 моль/л.
44. Константа равновесия реакции H2(г) + I2(г) ⇄ 2HI (г) при 4450С равна 50. Сколько молей Н2 надо взять на 1 моль I2, чтобы 90% иода превратилось в HI?
45. Общее давление газов в системе 1 атм. Определить объемный процент содержания монооксида углерода в момент равновесия для реакции FeO(тв) + CO(г) ⇄ Fe(тв) + CO2(г), если при Т = 1273К Кр = 0,4.
46.Исходные концентрации азота и водорода в системе N2 (г) + 3H2 (г) ⇄ 2NH3(г) были [N2] = 2 моль/л, [H2]= 8 моль/л. К моменту наступления равновесия прореагировало 10% исходного количества азота. Вычислить давление газовой смеси в момент равновесия при 5000С.
47. При 630С Кр = 1,27 для реакции N2O4 (г) ⇄ 2NO2(г). Определить равновесные парциальные давления газов, если общее давление в состоянии равновесия было 1атм.
48. Как изменится давление к моменту наступления равновесия в системе N2O4(г) ⇄ 2NO2(г) при постоянной температуре, если исходная концентрация N2O4 составляла 2моль/л, и к моменту наступления состояния равновесия прореагировало 25% от первоначального его количества?
49. При каком общем давлении должна находиться равновесная система PCl5(г) ⇄ PCl3(г) + Cl2(г), чтобы парциальное давление PCl5 при 250оС было равно 1атм. Кр = 1,78.
50. Для реакции C(гр) + 2H2(г) ⇄ CH4(г) Кс = 21,85 при
29
1000К. Рассчитать общее давление в состоянии равновесия, когда при Т = 1000К в сосуде емкостью 1л образовалось 0,1 моль метана.
51. Вычислить равновесные концентрации веществ в обратимой химической реакции CO(г) + H2O(г) ⇄ H2(г) + CO2(г), для которой Кс = 1 (Т=8500С), если исходные концентрации веществ составляли: [CO] = 2 моль/л, [H2O]=3 моль/л.
52. Вычислить константы равновесия (Кр) реакций: а) C(гр) + O2(г) ⇄ CO2(г); б) C(гр) + СO2(г) ⇄ 2CO(г), в которых парциальные давления СО2 в момент равновесия составляют 0,2 атм, а общее давление газов равно 1 атм (для каждого случая отдельно).
53. В начальный момент протекания реакции N2(г) + 3H2(г) ⇄ 2NH3(г) концентрации были равны: [N2] = 1,5 моль/л; [H2] = 2,5 моль/л; [NH3] = 0 моль/л. Каковы концентрации азота и водорода при [NH3] = 0,5 моль/л?
54. Концентрации веществ в реакции
CO(г) + H2O(г) ⇄ H2(г) + CO2(г) были: [CO] = 0,05 моль/л; [H2O] = 0,06 моль/л; [H2] = 0,2 моль/л; [CO2] = 0,4 моль/л. Вычислите концентрации всех участвующих в реакции веществ после того, как прореагировало 60% H2O.
55. Реакция протекает по уравнению
4HCl(г) + О2(г) ⇄ 2H2O(г) + 2Cl2(г). Через некоторое время после начала реакции концентрации участвующих в ней веществ стали [HCl] = 0,85 моль/л; [O2] = 0,44 моль/л; [Cl2] = = 0,30 моль/л. Какими были концентрации HCl и O2 в начале реакции?
56. Константа равновесия реакции N2(г) + 3H2(г) ⇄ 2 NH3(г) Кс = 0,1 при 673К. Равновесные концентрации [H2] = 0,6 моль/л; [NH3] = 0,18 моль/л. Вычислить начальную и равновесную концентрации азота.
57. Равновесные концентрации участников реакции CO(г) + H2O (г) ⇄ H2 (г) + CO2 (г) были: [CO] = 0,02 моль/л; [H2O] = 0,32 моль/л; [H2] = 0,08 моль/л; [CO2] = 0,08 моль/л.
30
Какими станут равновесные концентрации всех компонентов после сдвига равновесия, вызванного увеличением концентрации СО в 2 раза?
58. Имеется система, в которой протекает реакция Ag2O (тв) ⇄ 2Ag(тв) + 1/2O2(г) DН0298 = 32,2 кДж. Как скажется на концентрации кислорода над поверхностью твердой фазы: а) введение дополнительного количества Ag2O; б) повышение температуры?
59. Для реакции 3Fe(тв) + 4H2O(г) ⇄ Fe3O4(тв) + 4H2(г) DН0298 = -148,4кДж. Указать, как будет сказываться на концентрации водорода в равновесной смеси: а) повышение температуры; б) увеличение общего давления; в) увеличение весового количества железа; г) введение дополнительного количества водяного пара; д) как соотносятся энергии активации прямого и обратного процесса?
60. Дана обратимая реакция:4HCl(г)+ O2(г) ⇄ 2H2O(г) + 2Cl2(г) DН0298 = -112,24 кДж. Как повлияют на равновесную концен-трацию хлора следующие изменения:
а) повышение температуры; б) увеличение общего давления; в) увеличение концентрации кислорода; г) увеличение объема реакционного сосуда; д) введение катализатора.
61. Для реакции CaCO3(тв) ⇄ CaO(тв) + CO2(г) DН0298 = = 176,04 кДж. Указать, как повлияют на равновесную концен-трацию диоксида углерода следующие изменения: а) понижение температуры; б) увеличение весового количества карбоната кальция; г) введение катализатора; д) измельчение имеющегося количества карбоната кальция?
62. Для обратимой реакции SO2(г) + 1/2O2(г) ⇄ SO3(г) DН0298 = -95,6 кДж ответить на вопросы: а) что можно сказать о соотношении энергий активации прямого и обратного процессов; б) как скажется на концентрации диоксида серы введение дополнительного количества кислорода; в) изменится ли концентрация триоксида серы при увеличении общего давления (Т=const); г) как изменится концентрация кислорода
31
при повышении температуры; д) в каком направлении сместится равновесие при увеличении объема реакционного сосуда; е) скажется ли на равновесной концентрации триоксида серы введение в реакционную смесь катализатора?
63. В каком направлении сместится равновесие при увеличении общего давления и почему?
а) H2(г) + I2(г) ⇄ 2HI(г); б) N2(г) + 3H2(г) ⇄ 2NH3(г);
в) N2O4(г) ⇄ 2NO2(г); г) 2C(тв) + H2(г) ⇄ C2H2(г).
64. В каком направлении сместится равновесие при понижении температуры и почему?
а) SO2(г)+1/2O2(г) ⇄ SO3(г) DН0298 = -95кДж;
б) C(гр) + O2(г) ⇄ CO2(г) DН0298 = -393,8кДж;
в) N2(г)+3H2(г) ⇄ 2NH3(г) DН0298 = -92кДж;
г) CaCO3(тв) ⇄ CaO(тв)+CO2(г) DН0298 = 176кДж
65. Для следующих реакций рассчитать DН0х.р и определить, в каком направлении сместится равновесие при повышении температуры?
a) CaCO3(тв) ⇄ CaO(тв) + CO2(г);
б) 2Mg(тв) + O2(г) ⇄ 2MgO(тв);
в) O2(г) + N2(г) ⇄ 2NO(г);
г) N2(г) + 3H2(г) ⇄ 2NH3(г);
д) N2O4(г) ⇄ 2NO2(г)
66. При каких условиях надо вести реакцию N2(г) + 3H2(г) ⇄ 2NH3(г), DН0298 = -92,3кДж, чтобы получить мак-симальный выход аммиака? Как объяснить, что на практике синтез аммиака ведут при высокой температуре (400-5000С)?
67.Используя табличные данные, рассчитать DН0298 и с учетом знака (DН0298)х.р определить, как отразится на положении равновесия повышение температуры. В каком направлении сместится равновесие, если при Т=const увеличить внешнее давление?
а) 2SO2(г) + O2(г) ⇄ 2SO3(г)
б) H2S(г) ⇄ H2(г) + Sромб.
в) H2(г) + Br2(г) ⇄ 2HBr(г)
г) C(графит) + 2H2(г) ⇄ CH4(г)
32
д) C2 H4(г) ⇄ C2 H2(г) + H2(г)
е) 2C(гр) + H2(г) ⇄ C2H2(г)
ж) CO(г) + Cl2(г) ⇄ COCl2(г)
з) Fe2O3(тв) + 3CO(г) ⇄ 2Fe(тв) + 3CO2(г)
и) Fe3O4(тв)+4H2(г) ⇄ 3Fe(тв)+ 4H2O(г)
к) CН4(г) + H2О(г) ⇄ CО(г) + 3H2(г)
л) 2HBr(г) + Cl2 (г) ⇄ 2HCl(г) + Br2(ж)
м) PCl5 (г) ⇄ PCl3(г) + Cl2(г)
н) CО(г)+ 2H2(г) ⇄ CН3OН(г)
о) 2NO(г) + Br2(г) ⇄ 2NOBr(г)
п) CO(г) + H2O(г) ⇄ H2(г) + CO2(г)
68. В каком направлении будет смещаться равновесие с повышением: а) температуры и б) давления для следующих обратимых реакций:
а) 2SO2(г) + O2(г) ⇄ 2SO3(г); DН0298 = -196,6 кДж;
б) O2(г) + N2(г) ⇄ 2NO(г); DН0298 = +180,7 кДж;
в) 3SO2(г) ⇄ 2SO3(г); DН0298 = +184,6 кДж;
г) 2CO(г) + O2(г) ⇄ 2CO2(г); DН0298 = -566 кДж?
ЛАБОРАТОРНЫЕ РАБОТЫ.
Дата добавления: 2018-04-04; просмотров: 4266; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
