СПИСОК ИСПОЛЬЗОВАННОЙ И РЕКОМЕНДОВАННОЙ
ЛИТЕРАТУРЫ……………………………………………………………..…235
ВВЕДЕНИЕ
Цветные металлы – это промышленное название всех металлов, за исключением железа и его сплавов (сталь, чугун, ферросплавы), которые принято причислять к так называемым чёрным металлам. К этой группе часто условно относят также такие металлы, как хром, марганец, которые в основном используются в качестве добавок к железу. Однако их правильнеё относить в отдельную группу цветных металлов – легирующих металлов (легирующих элементов). В зарубежной литературе используют вместо наименования "цветные металлы" термин "нежелезные металлы" (non-ferrous metals).
Все цветные металлы разделяются на несколько групп (однако общепринятая классификация отсутствует). Так, в зависимости от плотности цветные металлы принято делить на лёгкие и тяжелые. К первой группе относятся такие, которые имеют плотность меньше 5 г/см3 (алюминий, магний, титан, бериллий, литий и др.), ко второй группе – те, у которых плотность больше 5 г/см3 (медь, никель, кобальт, свинец, олово, цинк и др.). Самым лёгким металлом является литий (плотность 0,53 г/см³). Наиболее тяжёлый металл в настоящеё время назвать невозможно, так как плотности осмия и иридия – двух самых тяжёлых металлов – почти равны (около 22,6 г/см³ – ровно в два раза выше плотности свинца), однако вычислить их точную плотность крайне сложно: для этого нужно полностью очистить металлы, поскольку любые примеси снижают их плотность.
В зависимости от температуры плавления используется градация на легкоплавкие и тугоплавкие металлы. Температуры плавления металлов лежат в диапазоне от −39 °C (ртуть) до 3410 °C (вольфрам). В качестве пороговой принимается температура, равная 1000 °С (в некоторых справочных изданиях подобное разделение основывается на сравнении с температурой плавления железа, т.е. 1539 °С). Соответственно к числу легкоплавких металлов относятся ртуть, олово, кадмий, свинец, цинк, магний, висмут, таллий, сурьма, алюминий; тугоплавкими являются серебро, медь, золото, железо, никель, титан, молибден, хром, ниобий, тантал и, конечно же, вольфрам.
Кроме того, металлы принято делить на благородные металлы (золото, серебро, платина, палладий, радий, рутений, иридий и осмий) и редкие металлы (вольфрам, хром, ванадий, молибден, тантал, радий и подгруппа редкоземельных – церий, торий, скандий, иттрий и др.). Появление термина редкие металлы объясняется сравнительно поздним освоением и использованием этих элементов, что связано с их малой распространённостью (или рассеянностью в земной коре), а также трудностями извлечения из сырья для выделения в чистом виде.
Из сказанного понятно, что как таковой общепринятой строгой классификации металлов нет, они в зависимости от характерных признаков могут быть в ряде случаев отнесенными к различным категориям.
Применение в технике сплавов цветных металлов поразительно разнообразно. Конечно, несомненными лидерами среди них являются лёгкие сплавы, а среди последних – алюминиевые сплавы благодаря ценному сочетанию эксплуатационных свойств. Возьмите современный авиалайнер. В нём практически не осталось деталей и узлов, выполненных не из лёгких сплавов, кроме жаропрочных деталей двигателя. Это вполне объяснимо стремлением к снижению массы самолёта, т.е. повышению удельной прочности материалов его конструкции. Это же требование применимо к любым транспортным машинам – автомобилям, железнодорожному и водному транспорту, да и к стационарным сооружениям тоже. Откройте капот вашей "тачки". Что вы увидите в первую очередь? Это головка блока цилиндров двигателя, выполненная из литейного алюминиевого сплава, который даже не надо покрывать краской из-за хорошей коррозионной стойкости. А внутри мотора? Вся электропроводка сделана из алюминия и меди. Поршни цилиндров, диски колёс, вкладыши подшипников, детали электрогенератора, стартёра, аккумулятора, свечей зажигания – успешная работа всех этих деталей и узлов немыслима без участия цветных металлов и их сплавов. И так в большинстве отраслей машиностроения.
Решение проблемы увеличения ресурса и надёжности машин при одновременном снижении их металлоёмкости возможно лишь при соединении усилий конструкторов и инженеров-расчётчиков, владеющих современными методами определения прочности, надёжности деталей машин, и грамотных материаловедов-технологов, знающих, как подобрать состав материала и технологию изготовления детали, чтобы получить нужную структуру и комплекс свойств для обеспечения расчётных эксплуатационных параметров деталей и узлов машин.
Одна из основных задач и профессиональная обязанность материаловеда-технолога – уметь технически грамотно и обоснованно решать задачи по выбору материала для конкретных деталей и технологии их обработки. Как правило, при этом не может быть однозначного и простого решения, поскольку, помимо необходимости обеспечить прочность, надёжность и долговечность детали с учётом специфических условий её службы (температура, среда, скорость нагружения, материал пары трения и т.п.), важно ещё предусмотреть по возможности простой технологический процесс, учесть экономические соображения. Ошибки в результате такого выбора материала не столь уж редки, что может привести к нежелательным или даже опасным последствиям – к преждевременному износу или даже поломке детали.
Обычно задание на выбор материала и технологии его обработки исходит от конструктора, который формирует перечень требуемых эксплуатационных и технологических показателей. Однако подобные формулировки практически всегда оказываются неполными, а иногда и не совсем точными. Поэтому материаловеду зачастую приходится решать такую задачу в ситуации неполного знания об условиях работы данной детали и об уровне потребительских свойств материала. В настоящеё время существует ряд компьютерных баз данных по свойствам стандартных материалов, включённых в ГОСТы, которые облегчают формальный поиск материала (чаще всего по показателям механических характеристик). Однако использование этого метода также может привести к неоптимальному решению, так как весьма трудно учесть множество разнонаправленных факторов, которые в совокупности определяют соотношение качества и цены изделия, обусловливающих его конкурентоспособность. Например, приблизительно равного комплекса механических свойств путём соответствующей термообработки можно достичь на разных по характеру легирования сплавах, например латунях и дуралюминах с резко различающимися технологическими, физико-химическими, эксплуатационными и экономическими характеристиками. Поэтому пользователями подобных баз данных должны быть квалифицированные материаловеды, способные принять компетентное и компромиссное решение.
Настоящеё учебное пособие продолжает выпущенное авторами аналогичное издание по выбору материалов и технологий применительно к сталям и чугунам [1] и предназначено для подготовки специалистов по разработке и применению металлических сплавов в машиностроении. Материал базируется на курсах "Металловедение", "Теория и технология термической обработки металлов", "Машиностроительные материалы", поэтому предполагается, что читатели знакомы с основными типами металлических материалов и технологиями их термической обработки, формирующей микроструктуру, а также методами механических испытаний. Не заменяя ряда известных учебников, данное учебное пособие представляет собой попытку показать в систематической форме материаловедческие принципы взаимосвязи структуры основных промышленных сплавов цветных металлов (алюминия, меди, магния, никеля и титана) с их физико-механическими и эксплуатационными свойствами в целях обоснованного решения проблем по выбору материалов и технологий их обработки для конкретных деталей.
Авторы представили данный учебный материал, придерживаясь традиций Уральской школы металловедов и используя многолетний опыт чтения соответствующих дисциплин материаловедческого цикла на металлургическом факультете Уральского федерального университета имени первого президента России Б.Н. Ельцина. Вместе с тем при написании пособия авторы использовали многие важные положения из классических учебников по материаловедению Ю.М. Лахтина, А.П. Гуляева, Б.Н. Арзамасова, Г.И. Сильмана [2–6]. Особенно близким по направленности представления материала и насыщенности конкретными примерами использования сплавов цветных металлов в машиностроении является учебник Б.А. Колачева, В.И. Елагина и В.А. Ливанова [9]. При этом из работ наших коллег заимствованы преимущественно такие разделы, которые описывают металловедческие принципы выбора материалов с учетом основного постулата металловедения: "состав материала – технология его получения и обработки – формирующаяся микроструктура – комплекс свойств". Потому приносим извинения авторам данных учебников за их подробное цитирование и выражаем признательность за возможность воспользоваться их полезным опытом.
На рисунке представлена схема, иллюстрирующая алгоритм решения материаловедческой задачи по выбору материала и технологии его получе-

Рис. Блок-схема выбора материала и технологии его обработки
ния и обработки. В зависимости от назначения и условий эксплуатации подбирается соответствующий материал по химическому составу, а также приемлемая технология его обработки. Формирующаяся в результате этого структура обеспечивает соответствующий комплекс свойств. Сравнение того, что получено (конкретный набор сформированных свойств yi), с тем, что нужно получить (заданные параметры служебных характеристик [yi]), и позволяет сделать заключение о конечном результате – выбран подходящий материал и технологический способ его обработки или же поиск следует продолжить, изменив исходные параметры (т.е. назначив иную технологию для уже выбранного материал либо поступив более радикально – заняться подбором иного материала и соответствующей ему обработки).
Представленные в тексте многочисленные фактические данные в виде таблиц и цифр позволяют ориентироваться в порядках величин и могут оказаться полезными для решения конкретных задач.
Примеры выбора материалов и технологий вместе с задачами помещёны в гл. 6. Ответы для некоторых характерных задач изложены в основном тексте.
Авторы выражают глубокую благодарность за рецензирование рукописи профессорам Б.А. Потехину, Б.Н. Гузанову, а также коллективу кафедры материаловедения, контроля в машиностроении и методики профессионального образования Российского государственного профессионально-педагогического университета-РГППУ.
Глава 1. МЕДЬ И ЕЁ СПЛАВЫ
Свойства меди
Медь – металл с кристаллической ГЦК-решеткой, период которой при 20 °С равен 0,36153 нм, имеющий температуру плавления 1083 °С. Она принадлежит к подгруппе IB периодической системы Д.И. Менделеева. Её порядковый номер 29, атомная масса 63,51. Медь относится к тяжелым металлам, её плотность при 20 °С составляет 8,94 г/см3. В земной коре содержится 0,01 % меди.
Чистая медь обладает небольшой прочностью и высокой пластичностью. Пластическая деформация меди, как и других металлов с ГЦК-решёткой, происходит путём скольжения преимущественно по плотноупаковынным плоскостям {111} в направлениях <110>. Временное сопротивление разрыву чистейшей меди составляет примерно 200 МПа, предел текучести 40¸80 МПа; поперечное сужение 80¸95 %, относительное удлинение до 35 %.
Электропроводность меди почти такая же, как и у серебра. Примеси снижают её электропроводность. Наиболее сильно повышают электрическое сопротивление меди Р, Аs, Аl, Fе, Sb, Sn. Кислород в небольших количествах повышает электропроводность меди, поскольку он способствует удалению при плавке окисляющихся примесей из расплава.
Химическая активность меди сравнительно невелика. Медь растворяется в минеральных кислотах, в частности в азотной и горячей концентрированной серной. В отсутствие кислорода и других окислителей разбавленные соляная и серная кислота на медь не действуют.
При обычной температуре сухой воздух и вода порознь не действуют на медь, и она сохраняет свой розовато-красный цвет. Во влажном воздухе медь тускнеёт из-за образования на её поверхности темно-красного оксида Сu2О. В присутствии во влажной атмосфере СO2 образуется зеленый налет основного карбоната СuСО3·Сu(ОН)2.
Благодаря уникальному сочетанию физико-механических, технологических и специальных свойств области применения меди очень разнообразны. Чистая медь и малолегированные её сплавы с высокой электро- и теплопроводностью широко используют в электротехнике, электромашиностроении, теплотехнике. Кроме того, медные сплавы применяют и в различных отраслях машиностроения.
Техническая медь. По характеру взаимодействия с медью примеси можно разделить на три группы. К первой группе относятся металлы, растворимые в твердой меди (Аl, Fе, Ni, Zn, Аg, Аu, Рt, Сd, Sb). Вторая группа представлена элементами, практически не растворимыми в меди в твердом состоянии и образующими с ней легкоплавкие эвтектики (Вi, Рb). Третью группу составляют полуметаллические и неметаллические элементы, образующие с ней химические соединения (O, S, Р, Sе, Те, Аs и др.).
Элементы первой группы не влияют на свойства меди в тех количествах, которые характерны для металла технической чистоты. В больших количествах оказывают благоприятное влияние на свойства меди и поэтому применяются для легирования.
Примеси, нерастворимые в меди, обычно отрицательно влияют на её механические и технологические свойства. Наиболее вредное влияние оказывает висмут. В системе Сu-Вi (рис. 1.1) образуется легкоплавкая эвтектика, состав которой почти совпадает с чистым висмутом (99,8 % Вi). Эвтектика кристаллизуется практически при той же температуре, что и висмут (270 и 272 °С соответственно). Растворимость висмута в меди ничтожно мала и не превышает 0,001 %, поэтому эвтектические выделения почти чистого висмута по границам зерен появляются при малых его количествах. Висмут – хрупкий металл, и его прослойки по границам зерен приводят к хладноломкости меди и её сплавов. При температурах горячей прокатки легкоплавкая эвтектика по границам зерен меди и её сплавов, состоящая по существу из чистого висмута, плавится, связь между зернами нарушается и возникают трещины. Следовательно, висмут вызывает и хладноломкость, и горячеломкость меди и её сплавов.
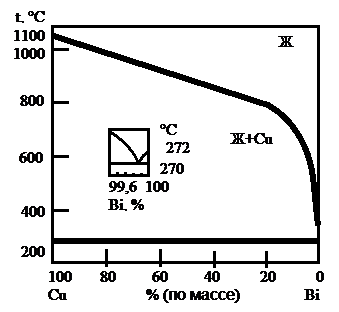
Рис. 1.1. Диаграмма состояния системы Cu-Bi
Аналог висмута – сурьма – из-за заметной её растворимости в меди оказывает значительно менее вредное влияние, но сурьма сильно уменьшает электро- и теплопроводность меди.
Для сплавов свинца с медью характерно монотектическое превращение при 953 °С и эвтектическое при 327 °С(рис. 1.2). Эвтектика в системе Сu-Рb по составу почти совпадает с чистым свинцом (99,96 % Рb). Растворимость свинца в меди ничтожно мала, поэтому эвтектические выделения свинца по границам зерен появляются при очень небольших его содержаниях, но свинец не приводит к хладноломкости меди и её сплавов, так как он пластичен, однако из-за низкой точки плавления эвтектики вызывает горячеломкость. Свинец облегчает обработку меди и её сплавов резанием, так как делает стружку более ломкой. Помимо этого, свинец повышает антифрикционные свойства меди и её сплавов.
Кислород присутствует в меди в виде оксида Сu2О, который образует с ней эвтектику при 3,4 % Сu2О или 0,38 % О (рис. 1.3). Температура плавления эвтектики в этой системе (1065 °С) выше температур горячей прокатки меди, и поэтому кислород не вызывает её горячеломкости. Растворимость кислорода в меди мала и составляет при 1065 °С всего 0,011 % (по массе). При весьма низких концентрациях кислорода в меди появляется эвтектика Сu + Сu2О. Закись меди Сu2О оказывает неблагоприятное влияние на пластические свойства, технологичность, коррозионную стойкость меди. Кислород затрудняет также пайку, сварку и лужение меди.
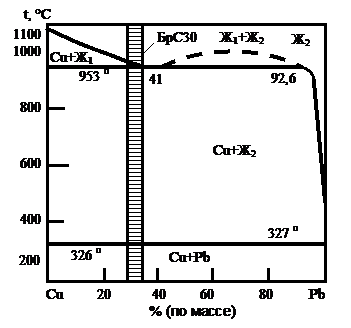

Рис. 1.2. Диаграмма состояния системы Cu-Pb Рис.1.3. Диаграмма состояния системы Cu-Cu2O
Сера образует соединение Сu2S, которое в твердой меди практически не растворяется. При самых малых добавках серы в меди формируется хрупкая эвтектика Сu + Сu2S. Эта эвтектика не вызывает горячеломкости, так как она плавится при высоких температурах, но приводит к хладноломкости и снижает технологическую пластичность при горячей обработке давлением.
Водород при содержаниях, больших его растворимости, приводит к пористости отливок. Особенно сильное отрицательное влияние оказывает водород на медь, содержащую кислород. При повышенных температурах водород диффундирует в медь и реагирует с расположенным по границам зерен оксидом меди, образуя пары воды высокого давления. Под давлением паров воды внутри металла возникают микротрещины, а на поверхности – вздутия (пузыри). Это явление называют водородной болезнью.
В зависимости от степени чистоты медь подразделяют на несколько сортов: М00, М0, М0б, М1б, М1, М1р, М2, М2р, М3, М3р (б – бескислородная медь, р – раскисленная медь). Содержание примесей наименьшее в меди марки М00 (99,99 % Cu) и наибольшее – в М3 (99,50 % Сu).
В меди марок М1, М2, М3 содержание кислорода составляет обычно 0,05¸0,08 %. Раскисленная медь отличается от указанных марок пониженным содержанием кислорода (не более 0,01 %), хотя его содержание и больше, чем в бескислородной меди (менее 0,001 % О).
Временное сопротивление разрыву меди разных марок составляет 220¸250 МПа, предел текучести равен 40¸50 МПа, относительное удлинение – до 46¸40 %. Предел выносливости при базе 3·108 циклов оказывается равным 70¸100 МПа, т.е. 30¸40 % от временного сопротивления разрыву.
С повышением температуры прочностные свойства меди уменьшаются (рис. 1.4). Относительное удлинение и поперечное сужение остаются неизменными до 200 °С, при более высоких температурах резко уменьшаются и лишь при нагреве выше 600 °С вновь начинают увеличиваться. Этот провал пластичности обусловлен примесями.
В результате пластической деформации медь нагартовывается (упрочняется), и при достаточно высокой степени деформации её временное сопротивление разрыву достигает 400¸450 МПа при одновременном падении относительного удлинения до 2¸4 % (рис. 1.5).

Сплавы меди
Медь образует непрерывные твердые растворы с соседними по таблице Д.И. Менделеева элементами: золотом, никелем, палладием, платиной, а также с марганцем. Серебро не обладает непрерывной растворимостью в твердой меди. Из металлов, образующих с медью непрерывный ряд твёрдых растворов, для легирования используют лишь никель и марганец; остальные – редки, дефицитны и дороги. Элементы, сильно отличающиеся по строению и свойствам от меди (Тi, Рb, Sе, Те), полностью не смешиваются с ней даже в жидком состоянии.
Важнейшими медными сплавами являются латуни и бронзы.
Латуни
Латуни (ГОСТ 15527-2004) – сплавы меди, в которых главным легирующим элементом является цинк. Различают двойные и многокомпонентные (специальные) латуни, содержащие дополнительные (легирующие) элементы. Двойные латуни маркируют буквой Л и числами, характеризующими среднеё содержание легирующих элементов. Так, латунь Л80 содержит 80 % Сu и соответственно 20 % Zn. Если латунь легирована помимо цинка другими элементами, после буквы Л ставят условное обозначение этих элементов: С – свинец, О – олово, Ж – железо, А – алюминий, К – кремний, Мц – марганец, Н – никель. Цифры после букв указывают среднеё содержание каждого легирующего элемента в латуни, кроме цинка. Содержание цинка определяется по разности до 100 %. Так, в латуни ЛАН-59-3-2 содержится 59 % Сu, 3 % Аl, 2 % Ni и 36 % Zn. В марке литейной латуни указывают не содержание меди, а содержание цинка, причем содержание легирующих элементов указывают не в конце марки, а после буквы, обозначающей элемент.
Латуни имеют широкое распространение благодаря сочетанию высоких механических и технологических свойств.
Двойные латуни
Фазовое состояние латуней описывается диаграммой состояния системы медь-цинк (рис. 1.6). Структура латуней состоит из α или α + β'-фаз, где α-фаза – твёрдый раствор замещения цинка в меди, имеющий решетку ГЦК, высокую пластичность, низкие значения прочности и твёрдости; β'-фаза – упорядоченный твёрдый раствор на базе интерметаллида СuZn (относящегося к группе электронных соединений) с кристаллической решеткой ОЦК. Эта фаза характеризуется более высокой твёрдостью, чем α-фаза, и хрупкостью. При нагреве в интервале 451¸468 °С нарушается упорядоченное расположение атомов в ОЦК-решётке (β'-фазы), и она обозначается как β-фаза. Нарушение упорядоченности повышает пластичность β-фазы.
С увеличением содержания цинка прочность возрастает (рис. 1.7). Поперечное сужение снижается, особенно резко при переходе от α- к (α + β)-структуре. Относительное удлинение достигает максимального значения при 30¸32 % Zn, а затем резко уменьшается, особенно при наличии β'-фазs. Временное сопротивление разрыву возрастает до 47¸50 % Zn, но как только β'-фаза полностью сменяет α-фазу, оно резко снижается. Пониженная пластичность β'-фазы обусловлена упорядоченным расположением атомов. Когда при нагреве β'-фаза переходит в неупорядоченную β-фазу, её пластичность резко возрастает и она становится пластичнеё α-фазы.
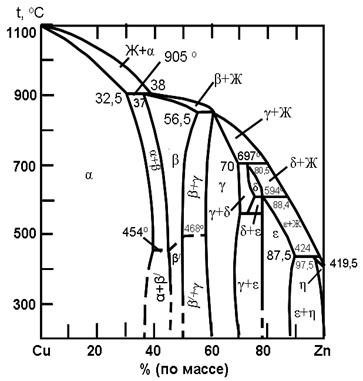
| Рис. 1.6. Диаграмма состояния системы Cu-Zn |
По структуре сплавы системы Сu-Zn разделяют на α-; (α+β)- и β-латуни; упорядочение β-фазы в этой классификации не учитывается. Структура однофазной (α) и двухфазной (α+β) латуней приведена на рис. 1.8. Однофазная латунь в отожженном состоянии имеет характерное строение в виде полиэдрических зерен с многочисленными двойниками отжига (рис.1.8, а). Структура двухфазной латуни представляет собой достаточно ясно выраженную смесь кристаллов α- и β-фаз (рис. 1.8, б).
Латуни со структурой α-фазы пластичны, имеют высокую технологичность и легко поддаются горячей и холодной обработке давлением. В температурном интервале 300¸700 °С α-латуни, как и медь, обнаруживают провал пластичности, и этого интервала температур при обработке давлением надо избегать (см. рис. 1.4). Пластичность β-латуней при комнатной температуре очень мала, и при содержании около 50 % Ζn и более они не поддаются холодной обработке давлением. Поэтому в промышленном масштабе применяют лишь α- и (α+β)-латуни. Однако β-латуни представляют интерес как основа сплавов с памятью формы и материалов с высоким пределом упругости ("сверхупругостью").
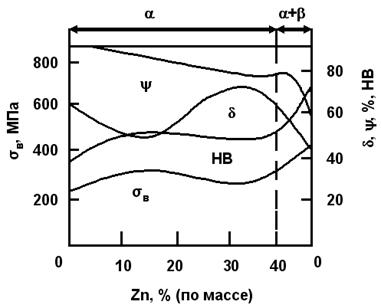
|
| Рис. 1.7. Влияние цинка на механические свойства меди |

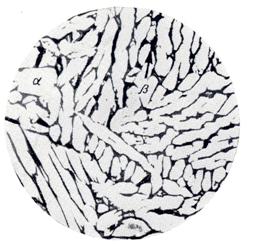
А б
Рис.1.8. Структура однофазной (а) и двухфазной (б) латуней; ´ 200
Наиболее широко применяют двойные латуни марок Л90, Л68, Л63 (табл. 1.1). Латунь Л90 называют томпаком; она обладает высокой стойкостью против коррозии и имеет красивый золотистый цвет, в связи с чем её применяют для изготовления знаков отличия и фурнитуры. Латунь Л68 называют патронной, из неё изготавливают изделия холодной штамповкой и глубокой вытяжкой, в частности гильзы патронов. Латунь Л63 называют торговой, так как она среди всех латуней занимает первое место по объему производства.
Холодная деформация приводит к существенному повышению прочности латуней при одновременном очень резком снижении пластичности (см. рис. 1.5). Отжиг деформированной латуни при температурах выше 400 °С снимает наклёп.
Отрицательное свойство латуней заключается в их склонности к самопроизвольному коррозионному растрескиванию, которое происходит во влажной атмосфере при сохранении в сплаве после деформации остаточных напряжений. Развитию растрескивания способствует присутствие в атмосфере следов аммиака, аммонийных солей, сернистых газов. Это явление называют ещё сезонной болезнью, так как оно чаще всего происходит весной и осенью, когда влажность воздуха повышена.
Растрескивание происходит из-за предпочтительной коррозии латуней по границам зерен в зоне неравномерного распределения напряжений. Это явление усиливается с увеличением содержания цинка и развивается особенно интенсивно при содержаниях его более 30 %. Для устранения склонности к растрескиванию нужно отжечь деформированные полуфабрикаты при температурах ниже температуры рекристаллизации. При таком отжиге эффективно снимаются остаточные напряжения и сохраняется высокая прочность, обусловленная наклепом.
Дата добавления: 2018-04-04; просмотров: 431; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
