Лос-Анджелеский и Лондонский смоги. Стратификация атмосферы, ее строение
Стратификация атмосферы, ее строение. Функция ионосферы и термосферы.
Атмосфера имеет слоистую структуру по вертикали:
1. Тропосфера
2. Стратосфера
3. Мезосфера
4. Термосфера
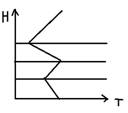
Между слоями существует небольшой переходный слой. По высоте происходит изменение температуры.
Термосфера - находится на высоте 120-500 км.Температура растет от -92 до 1200ºС. В мезосфере температура снижается от-2 до -92ºС. Начинается на высоте 50 км.
Мезосферу и термосферу объединяют в ионосферу. Остатки атмосферных газов, находящиеся в этих слоях, в состоянии ионов, которые образуются под действием кратковременного сильного излучения т.е. протекают фотохимические реакции.
|
N2+ hν →N+ + N-
О++ N2 →NO+ + N
О++ O2 →O2+ + O
Движение заряженных частиц зависит от наличия магнитного поля, частицы движутся вдоль магнитных силовых линий. В высоких широтах, где силовые линии практически вертикальны, эффективно протекает вертикальная диффузия частиц.
Изменение хим. Состава атмосферы в данных высотах влияет на концентрацию электронов в верхних слоях.
При увеличении концентрации N2 возрастает концентрация NO+. NO++ е = N+O
Электроны и ионы исчезают в ионно-молекулярных процессах, в результате рекомбинации, ионизации и диффузии.
Условия в ионосфере зависят от широты, наибольшая стабильная концентрация е̅ и ионов в средних широтах. В высоких широтах изменение е̅ наиболее сложно.
|
|
|
(22)7. Растворимость газов в воде. Основные газы в природных водоёмах. Их роль в гидросфере.
В природных водах присутствуют: O2 (расходуется на дыхание и др.окислительные процессы), H2S (вреден для организмов: снижает концентрации кислорода, смертелен в очень малых концентрациях), CH4 (ядовит для многих организмов), CO2 (расходуется в результате потребления фотосинтезирующими организмами, при связывании в соли угольной кислоты), N2 и др. Их источниками являются контактирующий с водой воздух и внутриводоёмные процессы. Концентрации газов в воде определяются их парциальными давлениями и константами Генри:
Сpi =Kiг*Pi[моль/л].
Kiг – константа Генри [моль/л*Па]; Pi – парциальное давление отдельного газа, находящегося в растворе [Па].
Растворимость газов в воде увеличивается с ростом внешнего давления и уменьшается с увеличением температуры. С этим связано уменьшение кислорода в верхнем слое водных объектов в летний период.
Устойчивость и неустойчивость приземного слоя атмосферы.
Под вертикальной устойчивостью атмосферного воздуха понимают его способность препятствовать вертикальному перемещению воздуха и сдерживать турбулентное перемешивание.
|
|
|
Различают 3 типа вертикальной устойчивости атмосферы:
а) Неустойчивое - когда объем воздуха, получивший импульс движения, не возвращается в исходное положение, а с ускорением движется в направлении первоначального смещения. Этому типу устойчивости соответствует конвекция - состояние атмосферы, при котором сильно развиты восходящие потоки воздуха, а температура почвы выше температуры воздуха (градиент температуры отрицателен).
б)Устойчивое - когда объем воздуха, сместившийся из своего исходного положения по высоте, стремится вернуться обратно. Этому типу устойчивости соответствует инверсия - состояние атмосферы, при котором восходящие потоки воздуха отсутствуют, имеют место нисходящие потоки, а температура почвы ниже температуры воздуха (градиент температуры положителен).
в) Нейтральное (безразличное) - когда смещенный объем воздуха, попав в слой с такой же температурой, остается неподвижным. Этому типу устойчивости соответствует изотермия - состояние атмосферы, при котором вертикальное перемещение воздушных масс практически отсутствует, а температуры почвы и воздуха практически равны (градиент температуры нулевой).
|
|
|
Лос-Анджелеский и Лондонский смоги.
Различают 2 смога:
1) Лондонского типа (восстановительный)
2) Лос-Анджелеский (фотохимический)
1)Образованию смога Лондонского типа способствует определённое состояние атмосферы с высоким содержанием влаги и температуры немного выше 0 градусов. Из антропогенных факторов необходимо присутствие в воздухе мелкодисперсной пыли и высокой концентрации диоксида серы (SO2).Частицы сажи являются центрами концентраций атмосферной влаги ,в которой растворяется SO2 с образованием Н2SO3.Она окисляется до Н2SO4, в результате в воздухе образуется мелко дисперсный туман Н2SO4
SO2 + Н2О = Н2SO3
Н2SO3 + О2 = Н2SO4
2)Фотохимический смог образуется в солнечную тёплую погоду за счёт фотохимического превращения УВ. Данный вид смога наблюдается вблизи крупных автодорог поскольку образуется из-за высокого содержания в атмосфере СН4 и его гомологов, оксид N и образуется в результатах прочих реакций О3.В процессе химической реакции участвует ОН, НО2 и NО2.Образовавшиеся конечные продукты имеют низкие ПДК и многие из них являются канцерогенными.
СН4 + ОН = Н2О + СН3
СН4  СН3 + Н
СН3 + Н
NO + O2H = NO2 + HO
NO2  NO + O
NO + O
O2 + O = O3
CH3 + O3 = CH3OOO
CH3OOO + NO2 = CH3O – N\ – O –/ O
O
|
|
|
Дата добавления: 2018-02-28; просмотров: 423; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
