Определяем окислитель и восстановитель в реакциях полного сгорания. Определяем стехиометрические коэффициенты в уравнениях методом электронного баланса.
Этен – C2H4
C2H4+O2→CO2+H2O
С.О.(О2) = 0. Для СО2 С.О.(С) = +4; С.О.(О) = –2.
Для Н2О С.О.(Н) = +1; С.О.(О) = –2.
В молекуле этена имеется два атома углерода со С.О.(С) = –2
Тогда:
2С–2 –12ē → 2С+4 12 ē 1 процесс окисления, углерод – восстановитель
О2 + 4ē → 2О-2 4 ē 3 процесс восстановления, кислород -окислитель
Получаем следующие стехиометрические коэффициенты: 1 и 3
C2H4+3O2→2CO2+2H2O
Данные процессы относятся к процессам окисления, а углерод является восстановителем в процессе горения. Восстановитель всегда повышает свою С.О.
О2 + 4ē → 2О-2 – процесс восстановления; кислород, являющийся составной частью воздуха, является окислителем. Окислитель всегда понижает свою степень окисления.
В реакции с С3Н6 так же углерод является - восстановителем, а кислород - окислителем
Определим стехиометрические коэффициенты в уравнении химической реакции:
2)С3Н6 + О2 → СО2 + Н2О

 3С-2 -18е → 3С+ 1 восстановитель, процесс окисления
3С-2 -18е → 3С+ 1 восстановитель, процесс окисления
О20 + 4е → 2О-2 4,5 окислитель, процесс восстановления
С3Н6 + 4,5О2 → 3СО2 + 3Н2О
Ответ: Углерод является восстановителем в процессе горения. Восстановитель всегда повышает свою С.О.
О2 + 4ē → 2О-2 – процесс восстановления; кислород, являющийся составной частью воздуха, является окислителем.
5. Определим объём воздуха, необходимый для полного сгорания смеси газов при н.у.
Найдем мольные доли веществ:


Найдем объемы, которые занимают составляющие газовой смеси в резеввуаре:
|
|
|


Для определения объёма воздуха, необходимого для полного сгорания смеси газов при н.у. воспользуемся следующими данными:
C2H4+3O2→2CO2+2H2O(I),
| Вещества: | C2H4 | O2 |
| 1.Соотношения реагирующих веществ: | ||
| 2.Масса веществ при н.у., кг: | 2,2·104 | - |
| 3.Количества реагирующих веществ, кмоль: | 
| 0,8·103 · 3 = 2,4·103 |
| 4.Объём реагирующих веществ при н.у., м3: | 17,9·103 | 53,7·103 |

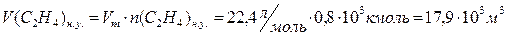
Сухой воздух содержит 21 об.% О2. Следовательно:  .
.
C3H6+4,5O2→3CO2+3H2O(II),
| Вещества: | C3H6 | O2 |
| 1.Соотношения реагирующих веществ: | 4,5 | |
| 2.Масса веществ при н.у., кг: | 2,2·104 | - |
| 3.Количества реагирующих веществ, кмоль: | 
| 0,5·103 · 4,5 = 2,3·103 |
| 4.Объём реагирующих веществ при н.у., м3: | 11,2·103 | 50,4·103 |


Сухой воздух содержит 21 об.% О2. Следовательно:  .
.
Определяем объём воздуха, необходимый для полного сгорания смеси углеводородов:

Ответ: 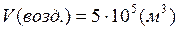
6. Определим тепловые эффекты реакций сгорания углеводородов в смеси, в расчёте на 1 моль газовой смеси.
Определим тепловые эффекты реакций сгорания углеводородов (I),(II) и (III), в расчете на 1 моль газовой смеси. Запишем термохимические уравнения протекающих реакций:
(I) C2H4(г) + 3O2(г) → 2CO2(г) + 2H2O(г) + ΔrHоIII (Дж/моль);
(II) C3H6(г) + 4,5O2(г) → 3CO2(г) + 3H2O(г) + ΔrHоII (Дж/моль)
|
|
|
Воспользуемся справочными данными для необходимых расчётов.
Справочные данные термодинамических функций при 298 К
| Участники реакций | Δ f Н°, кДж∙моль–1 | Δ f G°, кДж∙моль–1 | S°, Дж∙К–1∙моль–1 |
| C2H4(г) | 52.3 | 68.1 | 219.5 |
| C3H6 (г) | 20,41 | 62,7 | 266,94 |
| Участники реакций | Δ f Н°, кДж∙моль–1 | Δ f G°, кДж∙моль–1 | S°, Дж∙К–1∙моль–1 |
| O2(г) | 205,138 | ||
| CO2(г) | -393,51 | -394,36 | 213,74 |
| H2O(г) | -241,82 | -228,57 | 188,83 |
По следствию из закона Гесса, которое позволяет рассчитывать тепловые эффекты химических реакций:
Стандартная энтальпия химической реакции

равна разности стандартных энтальпий образования продуктов реакции и реагентов (с учетом стехиометрических коэффициентов):
 ,
,
где Δ r HоТ – изменение энтальпии реакции (тепловой эффект реакции), νj, νi – стехиометрические коэффициенты перед формулами конечных и исходных веществ соответственно, Δ f HоТ (Вj) – стандартная энтальпия образования продуктов реакции (конечных веществ), Δ f HоТ (А i) – стандартная энтальпия образования исходных веществ реакции.
Получаем:
ΔrHоI, 298 = 2*Δ f Ho298(CО2(г)) +2·Δ f Ho298(H2O(г)) – (Δ f Ho298(C2Н4 (г)) + 3·Δ f Ho298(О2(г))) = –393,51·2 + (–241,82)·2 – (–52.3 + 3·0) = –1322.96 (кДж/моль);
|
|
|
ΔrHоII, 298 = 3·Δ f Ho298(CО2(г)) + 3·Δ f Ho298(H2O(г)) – (Δ f Ho298(C3Н6(г)) + 4,5·Δ f Ho298(О2(г))) = –393,51·3 + (–241,82)·3 – (–103,85 + 4,5·0) = –1926,4 (кДж/моль).
Все реакции экзотермичны (ΔrHо << 0), согласно принципу Бертло-Томсена – самопроизвольны.
Принцип Бертло-Томсена:
А+В®АВ при ΔH<0
A+B®C+D при ΔH<0
Учитывая, что х(C2Н4) = 0.6, х(C3Н6) = 0,4 рассчитываем тепловые эффекты реакций на 1 моль газовой смеси:
ΔrHоI = ΔrHоI, 298 · х(C2Н4) = –1322.96 ·0,6 = -793,776(кДж/моль),
ΔrHоII = ΔrHоII, 298 · х(C3Н6) –1926,4 ·0,4 = -770,56 (кДж/моль).
Ответ: ΔrHоI= -793,776 (кДж/моль),ΔrH оII = -770,56 (кДж/моль),
Дата добавления: 2015-12-17; просмотров: 16; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
