Взаимодействие с металлами и щелочами
АМИНОКИСЛОТЫ
Аминокислоты – органические бифункциональные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы –NH2.
Всего известно около 150 аминокислот, но только около 20 из них встречаются в природе и служат исходными веществами для синтеза белков в живых организмах.
Природные аминокислоты можно разделить на следующие основные группы:
| 1) Алифатические предельные аминокислоты (глицин, аланин) | NH2-CH2-COOH глицин NH2-CH(CH3)-COOH аланин |
| 2) Серосодержащие аминокислоты (цистеин) | 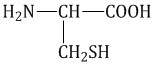 цистеин
цистеин
|
| 3) Аминокислоты с алифатической гидроксильной группой (серин) | NH2-CH(CH2OH)-COOH серин |
| 4) Ароматические аминокислоты (фенилаланин, тирозин) |  фенилаланин
фенилаланин
 тирозин
тирозин
|
| 5) Аминокислоты с двумя карбоксильными группами (глутаминовая кислота) | HOOC-CH(NH2)-CH2-CH2-COOH глутаминовая кислота |
| 6) Аминокислоты с двумя аминогруппами (лизин) | CH2(NH2)-CH2-CH2-CH2-CH(NH2)-COOH лизин |
Номенклатура аминокислот
Для природных α-аминокислот R-CH(NH2)COOH применяются тривиальные названия: глицин, аланин, серин и т. д.
По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино- и указанием места расположения аминогруппы по отношению к карбоксильной группе:
| 2 – Аминобутановая кислота | 3-Аминобутановая кислота |

| 
|
Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
|
|
|
| α-Аминомасляная кислота | β-Аминомасляная кислота |

| 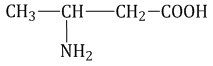
|
Физические свойства аминокислот
Аминокислоты – твердые кристаллические вещества с высокой температурой плавления. Хорошо растворимы в воде, многие обладают сладким вкусом, водные растворы хорошо проводят электрический ток.
Получение аминокислот
1. Замещение галогена на аминогруппу в соответствующих галогензамещенных кислотах:

2. Восстановление нитрозамещенных карбоновых кислот (применяется для получения ароматических аминокислот):

Химические свойства аминокислот
Кислотно-основные свойства аминокислот
Аминокислоты – амфотерные соединения. Они содержат в составе молекулы две функциональные группы противоположного характера: кислотная карбоксильная группа способна отщеплять катион водорода, а основная аминогруппа – присоединять катион водорода. Эти два эффекта взаимно усиливают друг друга, в результате чего в водном растворе аминокислоты существуют в виде биполярных ионов:

Водные растворы аминокислот имеют нейтральную, щелочную или кислую среду в зависимости от количества функциональных групп.
|
|
|
Так, глутаминовая кислота образует кислый раствор (две группы -СООН, одна -NH2), лизин – щелочной (одна группа -СООН, две -NH2).
Взаимодействие с металлами и щелочами
Как кислоты (по карбоксильной группе), аминокислоты могут реагировать с металлами, щелочами, образуя соли:

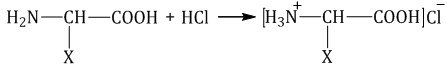
Взаимодействие с кислотами
По аминогруппе аминокислоты реагируют с кислотами:
Дата добавления: 2022-12-03; просмотров: 15; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
