ІІІ. Виведення молекулярної формули за відомими масою, об’ємами або кількістю речовини продуктів згорання
НВК «Гайворонська гімназія – загальноосвітня школа І-ІІІ ступенів №5» м. Гайворон
МЕТОДИКА РОЗВ’ЯЗУВАННЯ ЗАДАЧ НА ВСТАНОВЛЕННЯ ФОРМУЛ ОРГАНІЧНИХ СПОЛУК
Швець Наталія Миколаївна,
вчитель хімії НВК «Гайворонська гімназія загальноосвітня школа І-ІІІ ступенів №5» Кіровоградської області.
Гайворон 2013 р.
Навчальною програмою з хімії, яка розроблена на основі положень Державного стандарту базової та повної середньої освіти, передбачається вивчення найважливіших органічних сполук в 9 та 11класах.
З метою кращого засвоєння теоретичного матеріалу в програмі вивчення курсу «Органічна хімія», доцільно використовувати розрахункову задачі на виведення молекулярних формул органічних речовин.
Навчитися швидко і правильно розв’язувати задачі на виведення формул речовин можна використовуючи певні алгоритми та основні хімічні і фізичні властивості речовин.
Для формування основних умінь та навичок самостійного і раціонального розв’язування задач на встановлення формул основних класів органічних сполук, пропонується систематизувати їх по вихідним даним і алгоритмам розв’язання.
Пропоную приклади розв’язування задач на виведення формули органічних речовин:
· За належністю до певного класу речовин;
· За густиною та відносною густиною;
· За масовими частками;
· За масами, об’ємами або кількістю речовини продуктів згорання;
· За характерними хімічними властивостями речовин;
· За об’ємними відношеннями газів;
· За законом збереження маси речовини;
· За рівнянням стану ідеальних газів.
МЕТОДИКА РОЗВ’ЯЗУВАННЯ ЗАДАЧ НА ВСТАНОВЛЕННЯ ФОРМУЛ ОРГАНІЧНИХ СПОЛУК
І. Виведення молекулярної форми відомого класу органічних сполук за відносною густиною
Приклад
Відносна густина пари деякого алкану за повітрям дорівнює 3,931. Визначте формулу цього алкану і назвіть його.
 Дано: Розв’язування:
Дано: Розв’язування:
СnH2n+2 M(CnH2n+2)= (14n +2) г/моль
D(CnH2n+2)пов= 3,931 1. Обчислимо молярну масу алкану:
 СnH2n+2 - ? M(CnH2n+2) = D(CnH2n+2)пов
СnH2n+2 - ? M(CnH2n+2) = D(CnH2n+2)пов  Mпов;
Mпов;
Mпов=29г/моль
M(CnH2n+2) = 3,931  29 г/моль = 114 г/моль
29 г/моль = 114 г/моль
2. Обчислимо число атомів Карбону в алкані:
12n + 2 = 114; 14n = 112;  ; С8Н18
; С8Н18
Відповідь: Формула сполуки С8Н18. Це октан.
ІІ. Виведення молекулярної формули за відомими масовими частками елементів
Приклад
Виведіть молекулярну формулу вуглеводню, масова частка Карбону в якому становить 82, 75%, а Гідрогену 17,25%. Відносна густина пари цього вуглеводню за повітрям дорівнює 2.
 Дано: Розв’язування:
Дано: Розв’язування:
ω(С) = 82,75% 1. Обчислюємо молярну масу вуглеводню:
ω(Н) = 17,25% 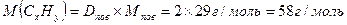
 D(CxHy)пов = 2 2 . Виводимо алгоритм для встановлення кількості атомів Карбону та Гідрогену:
D(CxHy)пов = 2 2 . Виводимо алгоритм для встановлення кількості атомів Карбону та Гідрогену:
CxHy - ? 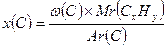
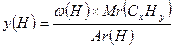
3 . Обчислюємо число атомів Карбону і Гідрогену у вуглеводні (для розрахунків відсотки переводимо в частки):
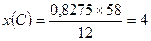
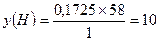
Формула вуглеводню С4Н10
4. Робимо перевірку виведеної формули вуглеводню за молярною масою:
М(С4Н10)=58г/моль
Відповідь: формула вуглеводню С4Н10 (бутан)
ІІІ. Виведення молекулярної формули за відомими масою, об’ємами або кількістю речовини продуктів згорання
Приклад
Внаслідок спалювання вуглеводню масою 1,5 г утворилися оксид карбону (ІV) об’єму 2,24 л (н.у.) та вода масою 2,7 г. Виведіть формулу вуглеводню, якщо відносна густина його за повітрям становить 1,0345.
 Дано: Розв’язування:
Дано: Розв’язування:
m(CxHy)=1,5г 1. Обчислимо молярну масу вуглеводню:
V(C xHy)=2,24 л 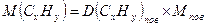
 m(H2O)=2,7г Mпов = 29 г/моль
m(H2O)=2,7г Mпов = 29 г/моль
 D(CxHy)пов=1,0345
D(CxHy)пов=1,0345 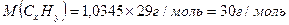
CxHy - ? 2. Обчислимо кількість речовини вуглеводню масою 1,5 г:
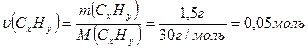
3. Обчислимо кількість речовини оксиду карбону (І V ) об’ємом 2,24 л:
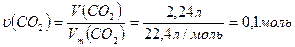
4. Обчислимо кількість речовини води масою 2,7 г:
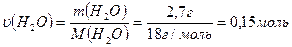
5. Обчислимо співвідношення кількостей речовин вуглеводню, оксиду карбону (І V ) та води:
υ (CxHy) : υ (СО2) : υ (Н2О) = 0,05 : 0,1 : 0,15
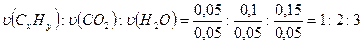
6. Обчислимо число атомів Карбону і Гідрогену у вуглеводні:
СхНу + О2 → 2 СО2 + 3Н2О
х=2; у=6; С2Н6; М(С2Н6) = 30 г/моль
Відповідь: Формула вуглеводню С2Н6 (етан)
Дата добавления: 2022-11-11; просмотров: 28; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
