Примеры реакций электрофильного замещения
Нитрование. Бензол и алкилбензолы реагирует со смесью концентрированной азотной и серной кислот (нитрующей смесью) с образованием ароматических нитросоединений.

Серная кислота выступает в роли катализатора, участвующего в генерировании электрофильной частицы – катиона нитрония  .
.
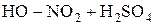 D
D 

Затем катион нитрония вступает в реакцию с ароматическим субстратом по механизму  .
.

Активированные субстраты, например, фенолы, нитруются в более мягких условиях разбавленной азотной кислотой (см. 10.2.4).
Галогенирование . Свободные галогены, например,  и
и  не способны реагировать с ароматическими системами бензола и алкилбензолов. Для проведения галогенирования необходим катализ кислотами Льюиса, такими как
не способны реагировать с ароматическими системами бензола и алкилбензолов. Для проведения галогенирования необходим катализ кислотами Льюиса, такими как  и др. При этом в молекуле галогена поляризуется за счет донорно-акцепторного взаимодействия и у нее появляется так называемый "электрофильный конец".
и др. При этом в молекуле галогена поляризуется за счет донорно-акцепторного взаимодействия и у нее появляется так называемый "электрофильный конец".
 D
D 

Более активные субстраты (фенолы, ариламины) взаимодействуют с молекулярными галогенами без катализатора (см. 10.2.4. и 13.4.3).
Сульфирование . Арены взаимодействуют с концентрированной серной кислотой или олеумом (раствор 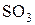 в серной кислоте) с образованием аренсульфокислот:
в серной кислоте) с образованием аренсульфокислот:

Электрофильной частицей в этих реакциях является 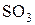 . Атаку ароматического субстрата осуществляет атом серы, поскольку он сильно положительно поляризован, и, следовательно, электронодефицитен:
. Атаку ароматического субстрата осуществляет атом серы, поскольку он сильно положительно поляризован, и, следовательно, электронодефицитен:
|
|
|
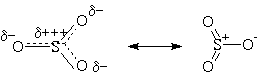
Сульфирование является обратимым процессом. Сульфогруппа в ароматическом ядре может замещаться на водород и гидроксил, что широко используется в органическом синтезе.
Алкилирование по Фриделю-Крафтсу . Подобно галогенам, алкилгалогениды могут быть сильно поляризованы кислотами Льюиса (хлоридами алюминия и цинка, трифторидом бора и др.), и становятся способными к электрофильному замещению в ароматическом ядре. Электрофильными частицами в этих реакциях являются карбокатионы или донорно-акцепторные комплексы галогенпроизводных с кислотами Льюиса.
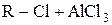 D
D  D R+AlCl4-
D R+AlCl4-

Кроме алкилгалогенидов для алкилирования ароматических соединений могут использоваться алкены или спирты в присутствии кислотного катализатора.


Присутствие катализатора необходимо для генерирования электрофильной частицы – карбокатиона:


Продукты алкилирования вступают в реакции электрофильного ароматического замещения легче, чем исходное соединение (Alk - электронодонорная группа), поэтому далее преимущественно алкилируется продукт и образуются продукты полиалкилирования.
Ацилирование по Фриделю-Крафтсу . Арены взаимодействуют с хлорангидридами и ангидридами карбоновых кислот в присутствии кислот Льюиса с образование кетонов:
|
|
|

X= Cl, OCOR
Хлорангидриды и ангидриды, имеют полярную карбонильную группу. Электрофильная активность этих соединений, однако, невелика, и должна быть повышена действием кислот Льюиса. В результате образуется поляризованный комплекс (а в пределе – ацил-катион), действующий как электрофил:


Полиацилирования не наблюдается, поскольку образующийся кетон значительно менее реакционноспособен, чем исходное соединение. Ароматические соединения с сильно дезактивирующими заместителями, например, нитро- или циано- группами, также не ацилируются по Фриделю-Крафтсу.
Электрофильное замещение в конденсированных ароматических углеводородах. Конденсированные ароматические углеводороды обладают большей реакционной способностью, чем бензол, так как энергия сопряжения, приходящаяся на одно ароматическое кольцо в них меньше, чем в бензоле.
При замещении в нафталине возможно образование двух изомерных продуктов: a- и в b-замещенных нафталинов. Атомы водорода в a-положении обладают более высокой реакционной способностью и, если реакция протекает в условиях кинетического контроля (хлорирование, нитрование), то образуется в основном a-изомер:
|
|
|


Сульфирование нафталина концентрированной серной кислотой при 80оС приводит к a-изомеру, который образуется с большей скоростью(кинетический контроль), а при 160оС – к термодинамически более стабильному b-изомеру (термодинамический контроль).

Дата добавления: 2022-01-22; просмотров: 22; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
