Искусственный интеллект на тропе войны
Докинг — это все же просто вычислительная методика, работающая по явно заданному компьютерному алгоритму. А как насчет более передовых технологий?
Горячей темой в разработке лекарств являются машинное обучение и искусственный интеллект. Несмотря на свою молодость, такие разработки уже достигли неплохих успехов: искусственный интеллект предсказывает пути синтеза неорганических материалов [38], определяет, как «свернется» белок [39], разрабатывает новые ингибиторы DDR-киназ [40]. Это будущее, стремительно входящее в практику фармацевтических компаний. Однако коронавирус ждать не будет — нужно, чтобы будущее наступило экстренно.
Компания InSilico Medicine, которая специализируется на применении искусственного интеллекта в медицине, предложила использовать свои протоколы для разработки новых антикоронавирусных лекарств. В отличие от предыдущих работ, это не перепрофилирование, а «придумывание» новой молекулы. Изюминка в том, что «придумать» (сгенерировать) структуру должен был компьютер [41]. А генерировать предполагалось на основе уже знакомой нам протеазы Mpro.
Так как эта компания начала работу в числе первых, они «не успели» дождаться кристаллографической структуры и использовали модель по гомологии, «вставив» в нее лиганд, содержащийся в шаблоне, и оптимизировав его положение молекулярным моделированием. К этой информации было добавлено почти 6 тыс. известных антипротеазных соединений. Компьютер должен был «придумать» соединения как на основе структуры связывающего кармана, так и на основе известных блокаторов.
|
|
|
В программе для «придумывания» была реализована особая архитектура нейронной сети (имитирующая нейронные сети мозга). Здесь уже нет явного алгоритма — как и живой мозг, программа учится. Компания использовала весь имеющийся у них арсенал методик: сети-автокодировщики, состязательные сети (в таком методе две нейронные сети соревнуются между собой), языковые модели (работающие по принципу предсказания следующего слова в предложении).
«Придуманные» компьютером молекулы далее подвергались фильтрации и отсеву по нескольким критериям: подходящие физико-химические параметры, отсутствие «нехороших» групп, предсказанная активность, качество докинга в модели протеазы, показатели новизны и разнообразия.
Методология довольно впечатляющая и очень напоминает таковую в предыдущем исследовании этой группы по созданию ингибиторов DDR-киназ [40], опубликованном в журнале Nature Biotechnology (что говорит само за себя). Сейчас группа занимается синтезом соединений для дальнейшей экспериментальной проверки, так что — ждем окончательных результатов и надеемся, что они будут хорошими!
|
|
|
Совсем другим путем пошли их конкуренты из компании BenevolentAI [42]. Они сконцентрировали внимание на перепрофилировании. Но на этот раз не использовали скрининг и докинг, а предложили искусственному интеллекту заняться процессом познания. Из научной литературы был извлечен граф знаний. На нем видно, что белок ACE2, с которым связывается коронавирус, участвует в эндоцитозе. Важным регулятором эндоцитоза является AP2-ассоциированная протеинкиназа-1 (AAK1). Соответственно, ее подавление может предотвратить эндоцитоз вируса.
Далее из 300 существующих ингибиторов ААК1 отобрали 40 одобренных для применения в клинической практике. Исключили препараты, обладающие выраженными нежелательными реакциями или требующие высоких дозировок лекарств. Среди шести высокоактивных ингибиторов особенно интересен ингибитор янус-киназ барицитиниб (изначально разработанный для лечения ревматоидного артрита). Он ингибирует не только ААК1, но и циклин-G-ассоциированную киназу (GAK), которая также участвует в эндоцитозе. Авторы полагают, что эта молекула может использоваться для профилактики и лечения коронавирусной инфекции. Идея хорошая, и — в кои-то веки — связана не с протеазой вируса, а с другой мишенью. Но это лишь модельные данные — их еще надо проверить.
|
|
|
По этим работам был написан весьма интересный критический разбор [43]. Обе работы критиковались в основном за очевидность. Так, критики считали, что работа сотрудников BenevolentAI — это скорее продвинутый научный поиск, доступный и человеку. Зачем здесь искусственный интеллект? Его триумфа здесь особо не просматривается. Но, на наш взгляд, сама по себе разработка, где искусственный интеллект собирает граф научных знаний с потенциальным медицинским применением, заслуживает внимания. Хотя бы с технической точки зрения. Такой подход может оказаться полезным в будущем — время покажет. Повторимся, что все данные пока предварительные.
InSilico критикуют за то, что их генератор создает молекулы, собирая «кусочки» известных лекарств. Например, одна из них содержит кусок противогельминтного препарата празиквантела (который в одной из упомянутых выше работ «выиграл» в докинге). Но основная претензия критиков заключается в том, что сотрудники InSilico не использовали перепрофилирование. Критики посчитали, что вряд ли кто-нибудь захочет вложиться в реальную разработку абсолютно новых лекарств. Но, в нашем понимании, это не проблема искусственного интеллекта и научного подхода коллектива InSilico.
|
|
|
Но не бизнесом единым движется область искусственного интеллекта в дизайне лекарств. Исследователи из Университета Мичигана использовали нейронную сеть-автокодировщик для генерации новых молекул, активных против Mpro [44]. Было сгенерировано несколько молекул, которые имеют неплохие физико-химические характеристики, а также доступны для синтеза (синтетическая доступность оценивалась с помощью SAScore [45]). Они сравнили созданные молекулы с рекомендованным на момент исследования сочетанием лопинавира с ритонавиром и нашли, что в целом характеристики биодоступности и синтетической доступности сгенерированных молекул были лучше. Но даже беглый взгляд на эти молекулы позволяет заметить, что тут еще нужно поработать над медико-химической составляющей. Многие структуры содержат очень реакционноспособные фрагменты, и до вируса в таком виде молекулы точно не дойдут. Это исследование еще очень «сырое».
В другой работе [46] той же команды использовались свёрточные нейронные сети. Они работают по принципу нейронных сетей в зрительных центрах коры головного мозга. Сети предсказывали энергии связывания молекул с Мpro-белком коронавируса. Сначала авторы собрали данные по молекулам, активным против SARS, потом «сдокировали» их в расшифрованную протеазу SARS-CoV-2 и на основе этого создали обучающую выборку. Отдельно собрали данные из базы BindingDB уже по отношению к разным белкам. С помощью полученной модели протестировали около 1400 известных лекарств для поиска возможности их перепрофилирования под лечение коронавируса. На их основе нашли группу молекул, которые можно перепрофилировать. По активности в этой группе лидировали: противоопухолевое таргетное средство, ингибитор протеасом бортезомиб, противотревожный и седативный препарат флуразепам и таргетный препарат для лечения лейкемии понатиниб.
Интересны данные исследователей по ингибиторам других протеаз как кандидатам в блокаторы протеазы коронавируса (табл. 1). «Лидером» оказался ингибитор протеазы вируса гепатита С боцепревир — только его авторы отмечали как имеющего высокую предсказанную аффинность к протеазе коронавируса. Его предсказанная аффинность высока: –9,36 ккал/моль. «Аутсайдером» оказался фосфорорганический яд изофлурофат — всего –4,94 ккал/моль, что почти ничто по меркам молекулярного моделирования.
| Таблица 1. Кандидаты в блокаторы протеазы коронавируса (из [46]; с изменениями) | |
| Класс веществ | Препараты |
| Ингибиторы вирусных протеаз | Ампренавир, атазанавир, боцепревир, дарунавир, индинавир, лопинавир, нелфинавир, ритонавир, саквинавир, симепревир, телапревир, типранавир, фосампренавир |
| Ингибиторы факторов свертывания крови (антикоагулянты) | Апиксабан, аргатробан, дабигатрана этексилат, ксимелагатран, ривароксабан |
| Ингибиторы АПФ | Беназеприл, каптоприл, квинаприл, лизиноприл, моэксиприл, периндоприл, рамиприл, спираприл, трандолаприл, фозиноприл, цилазаприл, эналаприл |
| Ингибиторы DPP4 | Алоглиптин, видаглиптин, линаглиптин, саксаглиптин, ситаглиптин |
| Ингибиторы других протеаз человеческого организма | Кандоксатрил, ремикирен, циластатин |
| Другие препараты/вещества | Изофлурофат, экабет |
Несмотря на то, что авторы выделили только боцепревир, ему «наступают на пятки» несколько ингибиторов вирусных протеаз, используемых для лечения вирусного гепатита и ВИЧ-инфекции, а также — немного неожиданно — ингибиторы факторов свертывания крови, которые также являются протеазами. В числе победителей также ингибиторы ангиотензинпревращающего фермента — того самого, к которому прикрепляется коронавирус. Это ведь тоже протеаза. Так что эти результаты также требуют проверки. Возможно, удастся создать препарат с двойным действием.
Исследователи группы Артема Черкасова, работающие в Университете Британской Колумбии (Ванкувер) [47], применили разработанный ими подход «глубокого докинга» [48] для поиска активных молекул с использованием кристаллической структуры Мpro уханьского коронавируса. «Глубокий докинг» представляет собой количественную модель «структура—свойство» на основе глубокого обучения, которая позволяет предсказывать результаты докинга. Методологически это исследование похоже на работу группы из Мичиганского университета.
Такой подход позволяет «просеять» гораздо больше соединений, чем при обычном докинге: ведь машина умеет предугадывать, какая энергия получится при докинге, и отбрасывать неподходящие молекулы. С использованием этого подхода авторы смогли провести виртуальный скрининг более 1,3 млрд (!) молекул из базы данных ZINC. В числе выявленных ими «лидеров» снова (уже в который раз!) оказался препарат для лечения ВИЧ — лопинавир. Также было отмечено «соединение 80» (имени у «новорожденного» вещества пока нет, только номер) — ингибитор протеазы SARS-CoV (из 2002 г.) (рис. 10). Однако 99% отмеченных соединений пока не синтезировано — это еще предстоит сделать.


Рисунок 10. Предсказанное положение одного из веществ (а; пурпурная стержневая модель), найденных группой А. Черкасова, и взаимодействия (б) этого соединения в связывающем участке протеазы SARS-CoV-2 по итогам докинга. Синими пунктирными линиями показаны водородные связи с пептидным остовом, зелеными — с атомами боковой цепи.
Истояник -[47]
Группа корейских ученых [49] обучила нейронную сеть предсказывать константу связывания молекулы с белком и провела поиск активных молекул среди коммерчески доступных. В результатах этого исследования оказались сразу три препарата против ВИЧ — ритонавир, который ранее был рекомендован для терапии коронавирусной инфекции (в сочетании с лопинавиром), а также атазанавир и эфавиренц. Немного разнообразия в эту подборку внесло противовирусное средство ганцикловир (но — от цитомегаловирусной инфекции).
Не протеазой единой...
Читатели могли обратить внимание (и мы сами неоднократно подчеркивали), что в компьютерных скринингах на блокирование Mpro часто «выигрывают» препараты для лечения ВИЧ-инфекции и гепатита C. Причем именно те, которые блокируют протеазы этих вирусов. Такое решение кажется очевидным — ведь протеазы могут быть похожи у разных вирусов. Кажется, что до этого можно догадаться и безо всякого моделирования! И исследователи уже догадались — об этом говорит применение комбинации лопинавира с ритонавиром против коронавирусных инфекций. А если так, то зачем вообще все эти высокопроизводительные вычисления и искусственный интеллект?
Не все так просто. Протеазы могут различаться по структуре и механизму катализа. Например, протеаза ВИЧ — аспартатная, протеаза вируса гепатита C — сериновая [50], а главная протеаза SARS-CoV-2 — цистеиновая [51], то есть они относятся к разным классам и имеют разный механизм действия. При таком разнообразии будет удачей, если ингибитор от одной протеазы подойдет к другой и будет эффективно ее блокировать. И искусственный интеллект здесь может послужить неплохим подспорьем, позволяя прикинуть шансы.
Кроме того, при недостатке экспериментальной информации самый очевидный путь может оказаться неверным. Например, если анти-ВИЧ-препараты эффективны против коронавирусов, связано ли это именно с протеазой?
Рассмотренные исследования давали положительный эффект, потому что в них протеаза была единственной мишенью. Этот момент может быть источником ошибки. А что, если сделать скрининг по всем возможным мишеням в составе коронавируса, которые изображены на рисунке 5? Этот рисунок взят из статьи [17], авторы которой уже провели такую масштабную работу. Построив по гомологии модели всех белков коронавируса, они провели скрининг существующих лекарств и натуральных соединений методом докинга.
По каждой мишени был получен список из 40 «лидеров», что в сумме, пожалуй, ставит рекорд по производительности среди статей, затронутых в обзоре. Весь список приведен в оригинальной статье — здесь же мы коснемся самых интересных находок.
Для ритонавира было найдено две возможные мишени, для лопинавира — даже четыре, но главной протеазы среди них нет! Зато рибавирин — аналог нуклеозида, для которого ожидаемо действие на репликацию и синтез белка, — оказался лидером по связыванию с папаин-подобной протеазой PLpro. Ему на пятки наступает валганцикловир — противогерпетическое средство, и тоже нуклеозидной природы! Правда, результаты скрининга против Mpro немного перекликаются с результатами команды из Университета Мичигана: там все же представлены препараты против ВИЧ — ампренавир и блокатор нейтральной эндопептидазы кандоксатрил. Но уверенность в протеазе как мишени перепрофилирования это исследование все же способно пошатнуть.
А коллектив исследователей из Польши исследовал главные протеазы SARS-CoV и SARS-CoV-2 методом молекулярной динамики и сообщил неприятное известие: оказывается, у этих белков разная форма и объем связывающего «кармашка» (рис. 11). «Карман» очень гибкий и, что самое плохое, подвержен мутациям [51]. Эта работа практически камня на камне не оставляет от представления о консервативности главной протеазы. Оказывается, это не лучшая мишень для драг-дизайна — по крайней мере, компьютерного.

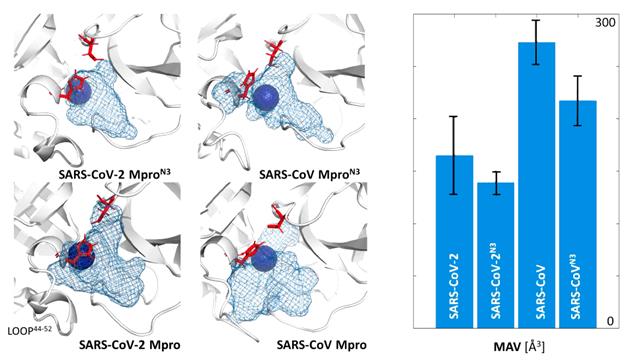
Рисунок 11. Форма сайта связывания главных протеаз вирусов 2002 (SASR-CoV) и 2019 годов (SARS-CoV-2) с ингибитором N3 и без него. На диаграмме справа — доступный объем сайта связывания. Видно, что «карман» протеазы SARS-CoV-2 меньше и имеет другую форму, нежели SARS-CoV.
Источник -[51]
Кроме этого, появились первые данные по клиническим испытаниям комбинации лопинавира с ритонавирсом в сравнении со стандартной терапией (кислород, ИВЛ и пр.) без приема этих лекарств. Результаты разочаровали: снижение смертности (19,2% vs 25,0%) и уменьшение продолжительности болезни (на 1,4 дня) оказались статистически незначимыми. При этом у 19% пациентов возникли побочные эффекты [52]. А ведь именно на эти препараты была большая надежда в плане блокирования Mpro.
Такое обилие плохих новостей несколько охладило интерес к главной протеазе. Скрининги по ней по-прежнему проводят многие исследовательские группы, но это направление стало своеобразным мейнстримом. И исследователи стали искать другие идеи.
Недавно появилось еще два масштабных скрининга против всех возможных мишеней [53], [54], причем один из них — даже с молекулярной динамикой [53]! Кроме этого, уже расшифрована структура белка «шипов» коронавируса и механизм его взаимодействия с АПФ на мембране клетки [55–58]. Этой перспективной мишенью уже воспользовались исследователи из Университета Теннесси — с помощью молекулярной динамики они смоделировали контакт между «шипом» вируса и АПФ и попробовали сделать масштабный докинг в него [59]. Получился довольно большой список «лидеров».
РНК-зависимая РНК-полимераза (RdRp) вируса стала объектом исследования ученых из Исследовательского центра IBM имени Томаса Уотсона и Университета Колумбии [60]. Они исследовали связывание уже упоминавшегося ремдесивира с этой полимеразой методом молекулярной динамики.
Ремдесивир исходно был разработан для лечения лихорадки Эбола, вирус которой также имеет РНК-зависимую РНК-полимеразу. В организме ремдесивир превращается в структурный аналог нуклеотидов, которыми полимераза достраивает цепь РНК (рис. 12). Схватив такую «молекулярную обманку», полимераза блокируется, а цепь РНК обрывается [61].


Рисунок 12. Ремдесивир превращается в нуклеозидтрифосфат, имитирующий «строительные блоки» РНК. Стоит РНК-полимеразе связать такой ложный «кирпичик», как цепь РНК оборвется.
С помощью молекулярной динамики исследователи хотели предсказать, как ремдесивир может связаться с полимеразой нового коронавируса. По их расчетам, его связывание должно быть примерно в 800 раз сильнее, чем связывание АТФ! Впрочем, пока это только модельные данные. Но биологически правдоподобные: RdRp есть у всех РНК-содержащих вирусов, и их структура наиболее консервативна (рис. 13). Их даже используют для установления филогении РНК-содержащих вирусов, подобно тому, как для клеточных организмов используют 16S рибосомную РНК [61]. Так что в этом случае ингибитор от одной полимеразы вполне может подойти к другой, а это внушает надежду.


Рисунок 13. Филогенетическое дерево RdRp РНК-содержащих вирусов (коронавирусы вверху). Возможно, все RdRp — очень дальние родственники друг другу.
Источник -[65]
А пока все искали оружие против вируса, исследователи из компании GERO решили поискать препарат, который сделает хозяина невосприимчивым к вирусу! С помощью собственной нейронной сети они нашли молекулы, вызывающие изменения экспрессии генов, похожие на эффект нокаута гена COBP2. Последний, в свою очередь, отвечает за репликацию вируса SARS. Так они нашли некоторое количество противовирусных препаратов с активностью против SARS и MERS (с эффективной концентрацией на уровне микромоль).
Относительная доступность средств био- и хемоинформатики делает возможным поиск сразу во всех направлениях. Но экспериментов по найденным новым веществам пока очень мало, и поэтому неясно: помогут ли в итоге вычислительные методы и искусственный интеллект в борьбе с вирусом? Это покажет время, однако нынешняя пандемия является в некотором смысле «тренировочной» для био- и хемоинформатиков. Даже если в итоге «компьютерные» находки не потребуются — мы будем иметь бесценный опыт компьютерной «гонки вооружений» с новыми патогенами, который может пригодиться в будущем.
Дата добавления: 2022-01-22; просмотров: 20; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
