Дегидрирование предельных углеводородов.
При пропускании алканов над катализатором при высокой температуре (400—600 °С) происходит отщепление молекулы водорода и образование алкена:

Дегидратация спиртов (отщепление воды).
Воздействие водоотнимающих средств (Н2SO4, Аl2O3) на одноатомные спирты при высокой температуре приводит к отщеплению молекулы воды и образованию двойной связи:
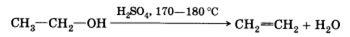
Эту реакцию называют внутримолекулярной дегидратацией (в отличие от межмолекулярной дегидратации, которая приводит к образованию простых эфиров).
Дегидрогалогенирование (отщепление галогеноводорода).
При взаимодействии галогеналкана со щелочью в спиртовом растворе образуется двойная связь в результате отщепления молекулы галогеноводорода.

СН3—СН2—СН—СН3 → СН3—СН2—СН=СН2 + HCl
l
Сl СН3—СН=СН—СН3 +HCl
Обратите внимание, что в результате этой реакции образуется преимущественно бутен-2, а не бутен-1, что соответствует правилу Зайцева:
При отщеплении галогеноводорода от вторичных и третичных галогеналканов атом водорода отщепляется от наименее гидрированного атома углерода.
Дегалогенирование.
При действии цинка на дибромпроизводное алкана происходит отщепление атомов галогенов, находящихся при соседних атомах углерода, и образование двойной связи:

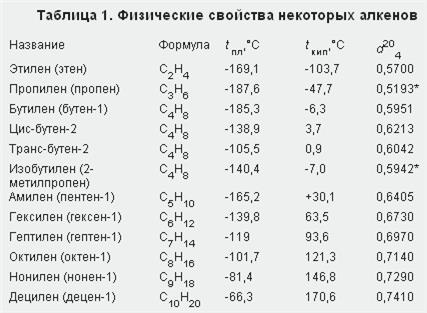
Физические свойства
Первые три представителя гомологического ряда алкенов — газы, вещества состава С5Н10—С16Н32 — жидкости, высшие алкены — твердые вещества.
|
|
|
Температуры кипения и плавления закономерно повышаются при увеличении молекулярной массы соединений.
Химические свойства
Реакции присоединения
Напомним, что отличительной чертой представителей непредельных углеводородов — алкенов является способность вступать в реакции присоединения. Большинство этих реакций протекает по механизму электрофильного присоединения.
Гидрирование алкенов.
Алкены способны присоединять водород в присутствии катализаторов гидрирования — металлов — платины, палладия, никеля:
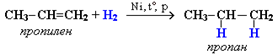
CH3—СН2—СН=СН2 + Н2 → CH3—CH2—СН2—СН3
Эта реакция протекает при атмосферном и при повышенном давлении и не требует высокой температуры, так как является экзотермической. При повышении температуры на тех же катализаторах может пойти обратная реакция — дегидрирование.
2. Галогенирование (присоединение галогенов).
Взаимодействие алкена с бромной водой или раствором брома в органическом растворителе (ССl4) приводит к быстрому обесцвечиванию этих растворов в результате присоединения молекулы галогена к алкену и образования дигалогеналканов.
Опыт
CH2=CH2 + Br2→ СН2Br—СН2Br
этен 1,2 - дибромэтан
|
|
|
Дата добавления: 2021-12-10; просмотров: 56; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
