Все четыре связи N—Н в катионе аммония равноценны.
Материалы урока
Химическая связь
Учение о химической связи составляет основу всей теоретической химии.
Под химической связью понимают такое взаимодействие атомов , которое связывает их в молекулы, ионы, радикалы, кристаллы.
Различают четыре типа химических связей: ионную, ковалентную, металлическую и водородную.
Ионная химическая связь
Ионная химическая связь — это связь, образовавшаяся за счет электростатического притяжения катионов к анионам.
Как вы знаете, наиболее устойчивой является такая электронная конфигурация атомов, при которой на внешнем электронном уровне, подобно атомам благородных газов, будет находиться 8 электронов (или для первого энергетического уровня — 2).
При химических взаимодействиях атомы стремятся приобрести именно такую устойчивую электронную конфигурацию и часто достигают этого или в результате присоединения валентных электронов от других атомов (процесса восстановления), или в результате отдачи своих валентных электронов (процесса окисления).
Атомы, присоединившие «чужие» электроны, превращаются в отрицательные ионы, или анионы .
Атомы, отдавшие свои электроны, превращаются в положительные ионы, или катионы.
Понятно, что между анионами и катионами возникают силы электростатического притяжения, которые и будут удерживать их друг около друга, осуществляя тем самым ионную химическую связь.
|
|
|
Так как катионы образуют в основном атомы металлов, а анионы — атомы неметаллов, логично сделать вывод, что этот тип связи характерен для соединений типичных металлов (элементы главных подгрупп I и II групп, кроме магния и бериллия Ве) с типичными неметаллами (элементы главной подгруппы VII группы).
Классическим примером является образование галогенидов щелочных металлов (фторидов, хлоридов и др.). Например, рассмотрим схему образования ионной связи в хлориде натрия:

Два разноименно заряженных иона, связанные силами притяжения, не теряют способности взаимодействовать с противоположно заряженными ионами, вследствие чего образуются соединения с ионной кристаллической решеткой.
Ионные соединения представляют собой твердые, прочные, тугоплавкие вещества с высокой температурой плавления.
Растворы и расплавы большинства ионных соединений — электролиты.
Такой тип связи характерен для гидроксидов типичных металлов и многих солей кислородсодержащих кислот. Однако при образовании ионной связи не происходит идеального (полного) перехода электронов. Ионная связь является крайним случаем ковалентной полярной связи.
В ионном соединении ионы представлены как бы в виде электрических зарядов со сферической симметрией электрического поля, одинаково убывающего с увеличением расстояния от Центра заряда (иона) в любом направлении. Поэтому взаимодействие ионов не зависит от направления, то есть ионная связь, в отличие от ковалентной, будет ненаправленной.
|
|
|
Ионная связь существует также в солях аммония, где нет атомов металлов (их роль играет катион аммония).
Ковалентная химическая связь
Ковалентная химическая связь — это связь, возникаю щая между атомами за счет образования общих электронных пар.
В основе ее описания также лежит представление о приобретении атомами химических элементов энергетически выгодной и устойчивой электронной конфигурации из восьми электронов (для атома водорода из двух). Такую конфигурацию атомы получают не путем отдачи или присоединения электронов, как в случае ионной связи, а посредством образования общих электронных пар.
Механизм образования такой связи может быть обменный или донорно-акцепторный.
Обменный механизм действует, когда атомы образуют общие электронные пары за счет объединения неспаренных электронов. Например:
1) Н2 — водород:
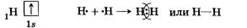
Связь возникает благодаря образованию общей электронной пары s-электронами атомов водорода (перекрыванию s-орбиталей):
|
|
|

Связь возникает за счет образования общей электронной пары из s- и р-электронов (перекрывания s—р-орбиталей):

Донорно-акцепторный механизм образования ковалентной связи рассмотрим на классическом примере образования иона аммония NH4+:

Донор имеет электронную пару, акцептор — свободную орбитальную, которую эта пара может занять.
В ионе аммония все четыре связи с атомами водорода ковалентные: три образовались благодаря созданию общих электронных пар атомом азота и атомами водорода по обменному механизму, одна образовалась по донорно-акцепторному механизму.
Все четыре связи N—Н в катионе аммония равноценны.
Аналогично образуется донорно-акцепторная связь в ионе метиламмония [СН3NH3]+.

Ковалентные связи классифицируют не только по механизму образования общих электронных пар, соединяющих атомы, но и по способу перекрывания электронных орбиталей, по числу общих электронных пар, а также по смещению их к одному из связанных атомов.
Дата добавления: 2021-12-10; просмотров: 45; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
