Роль эхокардиографии в диагностике ХСН
ХРОНИЧЕСКАЯ СЕРДЕЧНАЯ НЕДОСТАТОЧНОСТЬ
С физиологической точки зрения, сердце представляет собой насос, который откачивает кровь из венозного русла и нагнетает ее в артериальное. Производительность этого насоса может меняться от 4–5 л/мин в условиях физического и эмоционального покоя до 25 л/мин при интенсивной физической нагрузке. Неспособность сердца обеспечить системный кровоток, адекватный метаболическим потребностям организма, называется сердечной недостаточностью.
В зависимости от особенностей нарушения системной гемодинамики выделяют систолическую и диастолическую сердечную недостаточность. При систолической сердечной недостаточности уменьшается кровенаполнение артериального русла, что ведет к снижению артериального давления (АД) и недостаточному поступлению крови к органам и тканям. При диастолической сердечной недостаточности уменьшается отток крови из венозного русла, что ведет к повышению венозного давления и выходу жидкой части крови за пределы сосудистого русла, то есть к развитию отеков.
Сердечную недостаточность подразделяют на острую (ОСН) и хроническую (ХСН). ОСН развивается быстро, иногда, мгновенно и сразу приводит к столь выраженным нарушениям гемодинамики, что метаболические потребности организма не удовлетворяются даже в условиях физического покоя. ОСН может стать причиной внезапной смерти, может трансформироваться в ХСН, но может и пройти практически бесследно.
Гемодинамические нарушения при ХСН развиваются постепенно и первоначально могут появляться только при достаточно выраженных физических нагрузках. С течением времени гемодинамические расстройства прогрессируют и доходят до степени, при которой метаболические потребности организма не удовлетворяются уже и в условиях физического покоя. Рано или поздно ХСН приводит к смерти пациента, если, конечно, он не скончается раньше от других причин.
Этиология и патогенез ХСН
К развитию ХСН приводят заболевания, сопровождающиеся
· первичным поражением миокарда, — инфаркт миокарда, миокардиты, кардиомиопатии,
· увеличением постнагрузки (нагрузки давлением) на сердце, — стеноз устья аорты, легочной артерии, митрального и трикуспидального клапанов, артериальная гипертензия, легочная гипертензия,
· возрастанием преднагрузки (нагрузки объемом) на сердце, — дефекты межпредсердной и межжелудочковой перегородки, открытый артериальный проток, недостаточность митрального и аортального клапана.
Повреждение миокарда или увеличение нагрузки на сердце приводит в действие кардиальные и экстракардиальные механизмы компенсации, обеспечивающие адаптацию сердца к новым условиям жизнедеятельности и поддержание адекватного сердечного выброса (рис. 1).
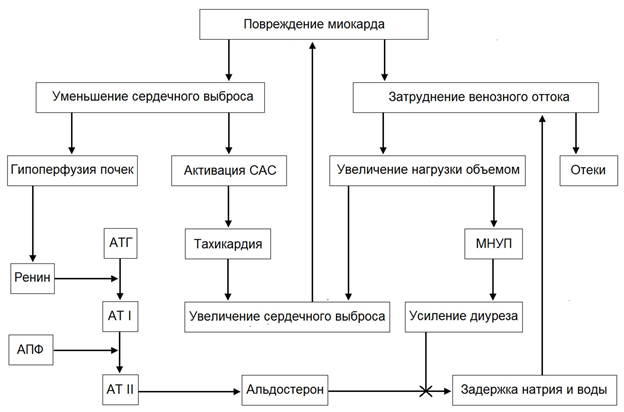
Рис. 1. Патогенез ХСН (объяснение в тексте)
Механизмы компенсации (адаптации) можно разделить на аварийные и долговременные.
Аварийным экстракардиальным механизмом адаптации служит активация симпатико-адреналовой системы, обеспечивающая поддержание сердечного выброса за счет увеличения частоты и силы сердечных сокращений, что сопровождается резким возрастанием потребности миокарда в кислороде.
Аварийным кардиальным механизмом адаптации можно считать дилатацию сердца, приводящую к перерастяжению миокарда в период диастолы и, следовательно, к возрастанию силы его сокращения во время систолы (механизм Франка-Старлинга). Выполняемая сердцем работа и потребность миокарда в кислороде при этом увеличивается.
Долговременным кардиальным механизмом адаптации является гипертрофия миокарда, уменьшающая относительную нагрузку на сердце, то есть нагрузку, приходящуюся на единицу массы сердечной мышцы. Однако гипертрофия миокарда развивается за счет увеличения массы только функционально активной ткани, то есть кардиомиоцитов и не сопровождается ростом обеспечивающих структур, в частности, сосудистой сети. Вследствие этого гипертрофированный миокард оказывается в условиях недостаточного кровоснабжения, что рано или поздно приводит к дистрофии миокардиоцитов, срыву компенсации и развитию ХСН.
Активация ренин-ангиотензин-альдостероновой системы (РААС) играет роль долговременного экстракардиального механизма адаптации при ХСН. Пусковым механизмом активации РААС служит гиперпродукция ренина, обусловленная гипоперфузией почек из-за снижения сердечного выброса. Ренин переводит ангиотензиноген (АТГ) в ангиотензин I (АТ I), который под воздействием ангиотензинпревращающего фермента (АПФ) превращается в ангиотензин II (АТ II). Последний вызывает генерализованный спазм артериол большого круга кровообращения, что ведет к повышению АД
и обеспечивает адекватное кровоснабжение жизненно важных органов, в
частности, почек, но повышает нагрузку на сердце и его потребность в кислороде. Кроме того, АТ II стимулирует выработку альдостерона, что ведет к задержке жидкости в организме и, увеличивая приток крови к сердцу, способствует развитию его дилатации и повышению сердечного выброса по механизму Франка-Старлинга. При этом возрастает выполняемая сердцем работа и его потребность в кислороде.
Таким образом, механизмы адаптации обеспечивают поддержание сердечного выброса, но, стимулируя работу сердца, способствуют его быстрому «изнашиванию» и прогрессированию ХСН. Этим определяется современная стратегия лечения ХСН, призванная уменьшить выраженность экстракардиальных компенсаторных реакций и снизить тем самым нагрузку на сердце.
Клинические проявления ХСН
Клиническая картина ХСН складывается из симптомов, связанных с недостаточным кровоснабжением органов и тканей, и симптомов, обусловленных венозным застоем в малом и/или большом круге кровообращения.
Одышка при доступных ранее физических нагрузках, сердцебиение и быстрая утомляемость отражают неспособность сердца обеспечить адекватное кровоснабжение работающей мускулатуры. При тяжелой ХСН одышка может отмечаться и в покое, поскольку работа дыхательных мышц становится для организма непосильной нагрузкой.
Появление или усиление одышки в горизонтальном положении тела и улучшение самочувствия в положении сидя (ортопноэ) является характерным признаком венозного застоя в малом круге кровообращения. С застоем крови могут быть связаны и влажные, незвучные, мелкопузырчатые хрипы в нижних отделах легких, а также появление небольшого плеврального выпота. Отек слизистой бронхов может привести к появлению свистящего дыхания и сухих
хрипов, что затрудняет дифференциальную диагностику сердечной и
легочной недостаточности. Ранним, но очень неспецифичным признаком венозного застоя в легких служит ночной кашель.
Венозный застой в большом круге кровообращения сопровождается набуханием шейных вен, увеличением и болезненностью печени, появлением гепатоюгулярного рефлюкса, чувством переполнения в животе, развитием периферических отеков, начиная от легкой пастозности лодыжек и заканчивая анасаркой.
Клиническую картину ХСН дополняют симптомы, отражающие изменения со стороны сердца: ритм галопа, смещение верхушечного толчка влево, систолический шум на верхушке.
Следует отметить, что симптомы, из которых складывается клиническая картина ХСН, могут отмечаться и при других заболеваниях. Поэтому диагноз ХСН можно считать обоснованным лишь в том случае, когда у пациента имеются изменения структуры и функции сердца, способные привести к нарушениям системной гемодинамики. Для выявления таких изменений используется эхокардиографическое исследование.
Роль эхокардиографии в диагностике ХСН
Эхокардиографическое исследование (ЭхоКГ) в большинстве случаев позволяет диагностировать заболевание, ставшее причиной развития ХСН, и оценить функциональное состояние желудочков сердца.
Принципиально важным является выявление заболеваний, нарушающих внутрисердечную гемодинамику, то есть пороков сердца и болезней перикарда, своевременное хирургическое лечение которых может предотвратить развитие или прогрессирование ХСН. При отсутствии такой патологии решающее значение в диагностике ХСН приобретает оценка функционального состояния желудочков сердца.
Для оценки систолической функции левого желудочка рассчитывают
фракцию выброса (ФВ), равную отношению ударного объема к конечному диастолическому объему левого желудочка:
 ФВ(%) = 100 КДО – КСО,
ФВ(%) = 100 КДО – КСО,
КДО
Где КДО и КСО — соответственно конечный диастолический и конечный систолический объем левого желудочка.
Существуют два метода определения объема левого желудочка: метод Тейхольца и метод Симпсона. В первом случае объем левого желудочка принимается равным кубу его размера, измеренного в парастернальной позиции по длинной оси:
КДО = КДР3; КСО = КСР3,
где КДР и КСР — соответственно конечный диастолический и конечный систолический размер левого желудочка (рис. 2).
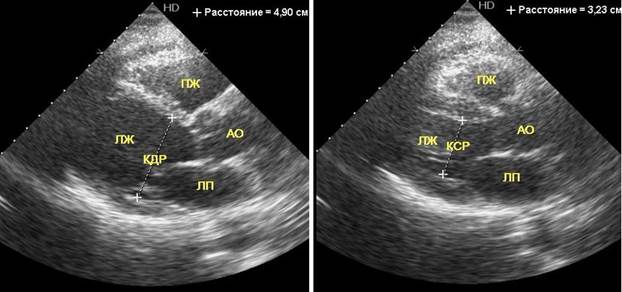 |
Рис. 2. Измерение КДР и КСР левого желудочка
Метод Тейхольца дает весьма приблизительное представление об объеме левого желудочка, что позволяет уверенно говорить о нарушении его систолической функции лишь в том случае, если ФВ, измеренная по этому методу, ниже 45%.
По методу Симпсона полость левого желудочка разбивается на 20 дисков разного диаметра, но одинаковой толщины (рис. 3), а объем полости принимается равным сумме объемов всех этих дисков:
i=20 𝐿
𝑉 = ∑ 𝜋𝑅2
i=1
i 20
где R — радиус диска, i — его порядковый номер, L — длина левого желудочка, V — его объем.
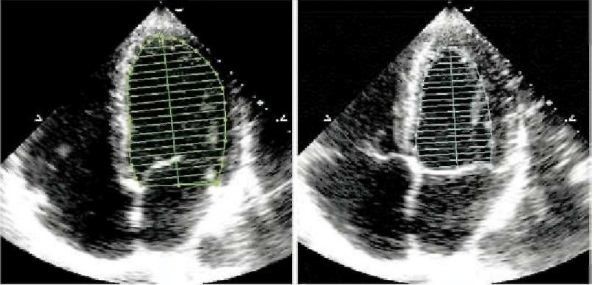 |
Рис. 3. Определение КДО и КСО левого желудочка по методу Симпсона
При использовании метода Симпсона нарушение систолической функции левого желудочка диагностируют, если ФВ ниже 55%.
Оценка диастолической функции левого желудочка представляет собой значительно более сложную задачу, для решения которой необходимо, как минимум, с помощью допплеровского исследования изучить характер трансмитрального кровотока (рис. 2).
Диастолическое наполнение желудочков сердца протекает в две фазы. Сначала кровь поступает из предсердий в желудочки по градиенту давления, возникающему при расслаблении миокарда желудочков. После того, как давление в желудочках и предсердиях выровняется, кровоток через атриовентрикулярные клапаны на короткое время прекращается (диастазис), но затем сокращение предсердий нагнетает в желудочки дополнительную порцию крови.
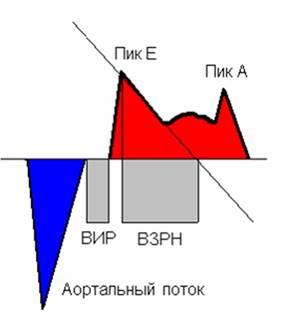 Рис. 4. Схематическое изображение допплеровского спектра трансмитрального кровотока. ВИР — время изоволюмического расслабления, ВЗРН — время замедления раннего наполнения
Рис. 4. Схематическое изображение допплеровского спектра трансмитрального кровотока. ВИР — время изоволюмического расслабления, ВЗРН — время замедления раннего наполнения
В норме максимальная скорость трансмитрального кровотока в раннюю фазу диастолического наполнения левого желудочка (пик Е, от англ. early — ранний) больше, чем в предсердную (пик A, от англ. atrium — предсердие), но отношение Е/А не превышает 2.
При I степени диастолической дисфункции нарушается способность миокарда левого желудочка к расслаблению, вследствие чего скорость трансмитрального кровотока в раннюю фазу диастолического наполнения уменьшается, и пик E снижается. «Недозаполнение» левого желудочка в раннюю фазу трансмитрального кровотока компенсируется усиленной работой левого предсердия, вследствие чего скорость трансмитрального кровотока в предсердную фазу увеличивается, и пик A возрастает. В результате пик A становится выше пика E, а отношение Е/А — меньше 1.
При II степени диастолической дисфункции нарушается способность левого желудочка к наполнению во время систолы предсердий, вследствие чего пик А снижается и отношение Е/А становится нормальным (псевдонормализация кровотока).
При III степени диастолической дисфункции способность левого желудочка к наполнению во время систолы предсердий практически
утрачивается, пик А резко снижается и отношение Е/А становится больше 2 (рестриктивный тип наполнения).
При II и, особенно, при III степени диастолической дисфункции повышается давление в левом предсердии, что ведет к затруднению оттока из легочных вен и развитию венозного застоя в малом круге кровообращения.
Нарушение систолической функции левого желудочка всегда сочетается с диастолической дисфункцией, степень которой можно оценить по характеру трансмитрального кровотока. Отношение Е/А < 1 указывает на I степень диастолической дисфункции (нарушение релаксации), 1 ≤ Е/А < 2 — на II степень (псевдонормальная диастолическая функция), Е/А ≥ 2 — на III степень (табл. 1).
Таблица 1
Критерии диастолической дисфункции
| Систолическая дисфункция | Диастолическая дисфункция | |||
| Нет | 1-я степень | 2-я степень | 3-я степень | |
| Есть | – |
Е/А < 1 |
1 ≤ Е/А < 2 |
Е/А ≥ 2 |
| Нет | е’ ≥ 8 см/с | |||
| Не имеет значения | Е/е’ ≤ 8 | СДЛА ≤ 35 | СДЛА > 35 | Е/е’ ≥ 15 |
У больных с сохраненной систолической функцией левого желудочка оценить состояние его диастолической функции только по характеру трансмитрального кровотока не представляется возможным. В этом случае требуется проведение тканевого допплеровского исследования, позволяющего определить скорость движения миокарда в раннюю диастолу (е’). Если е’ не меньше 8 см/с, то диастолической дисфункции нет, в противном случае ее степень определяется так же, как у больных с нарушением систолической функции.
Существует и другой алгоритм определения степени диастолической дисфункции у больных с сохраненной систолической функцией, согласно которому при отношении Е/е’ не более 8 диастолической дисфункции нет, а
при величине этого отношения 15 и более имеет место диастолическая
дисфункция III степени. При отношении Е/е’ от 9 до 14 имеется диастолическая дисфункция I или II степени, для разграничения которых у больных без легочной патологии можно использовать уровень систолического давления в легочной артерии. Если давление не превышает 35 мм рт. ст., то имеется I степень диастолической дисфункции, в противном случае — II. У больных с патологией легких для разграничения I и II степени диастолической дисфункции можно использовать объем левого предсердия, индексированный по площади поверхности тела. Если величина этого показателя меньше 35 мл/м2, то речь идет о I степени диастолической дисфункции, в противном случае — о II степени.
Стоит обратить внимание, что последний алгоритм может быть использован и у больных с фибрилляцией предсердий, поскольку он не требует определения скорости предсердного наполнения (пик А).
Функциональное состояние правого желудочка оценивают по наличию признаков его перегрузки и состоянию нижней полой вены (НПВ). Признаком перегрузки правого желудочка являет увеличение его диастолического размера в парастернальной позиции более 30 мм или соотношение размеров правого и левого желудочков более 1 (Рис. 5),
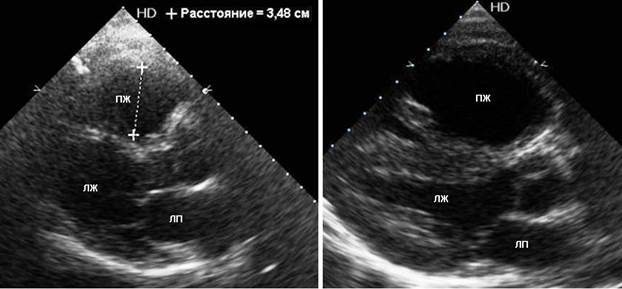
Рис. 5. Признаки перегрузки правого желудочка (ПЖ). ЛЖ — левый желудочек, ЛП — левое предсердие
В норме диаметр НПВ на выдохе не превышает 1,8 см, а на вдохе уменьшается не менее, чем на 50%. Увеличение диаметра НПВ и уменьшение степени ее спадения на вдохе указывают на венозный застой в большом круге кровообращения.
Дата добавления: 2021-12-10; просмотров: 38; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
