Генетические маркёры резистентной депрессии
Нейротрофическая гипотеза депрессии свидетельствует об ассоциации между эффектами нейропластичности и клиническим ответом на терапию антидепрессантами. В новой работе, проведённой Breitfeld J. и коллегами, изучалась индивидуальная вариабильность эффекта антидепрессивной терапии на пролиферацию клеток лимфобластоидной линии у 25 терапевтически-резистентных пациентов в сравнении с 25 пациентами, которые отреагировали на первую линию терапии антидепрессантами, из исследования STAR*D.
Кроме того, была проанализирована изменчивость экспрессии генов, ассоциированных с клеточной пролиферацией, для поиска предварительных генов-кандидатов для прогнозирования ответа на лечения на основе донорских клеток лимфобластоидной линии. Пролиферация клеток определялась с помощью EdU (5-этинил-2′-дезоксиуридин) анализа после 21 дня инкубации клеток лимфобластоидной линии с флуоксетином (0.5 ng μl−1) и циталопрамом (0.3 ng μl−1). Экспрессия генов была исследована с помощью панели генов-кандидатов, полученной от полногеномного поиска ассоциаций эффектов антидепрессантов на пролиферацию клеток лимфобластоидной линии исследования MARS, с помощью ПЦР в реальном времени.
In vitro были получены значительные различия клеточной пролиферации в группах клеток лимфобластоидной линии от пациентов, отреагировавших на первую линию антидепрессантами, и от пациентов с терапевтически-резистентной депрессией. Анализ экспрессии генов с помощью панели генов-кандидатов выявил и подтвердил влияние генов-кандидатов ABCB1, FZD7 и WNT2B на развитие резистентности к антидепрессивной терапии.
|
|
|
Таким образом, потенциал данных генов в качестве предварительных биомаркёров резистентности к антидепрессивной терапии был подтверждён, что свидетельствует о том, что тестирование клеточной пролифераации in vitro может служить в качестве функционального биомаркёра определения нейропластических эффектов антидепрессантов.
Подготовил: Касьянов Е.Д.
Источник: J. Breitfeld, C Scholl, M Steffens, G Laje, and J C Stingl. Gene expression and proliferation biomarkers for antidepressant treatment resistance. Transl Psychiatry. 2017 Mar; 7(3): e1061.
Генные аномалии в патогенезе болезни Паркинсона: предварительные результаты общегеномных исследований (2015-2017 г.)
На основе полногеномного поиска ассоциаций (GWAS) выявлено 24 генные аномалии, влекущих за собой нейродегенеративные заболевания головного мозга, в частности болезнь Паркинсона (БП). Из них 17 аномалий были найдены при содействии Фонда Джей Фокса и 23andMe на основе анализа данных 425 000 пациентов с диагнозом БП.
Болезнь Паркинсона — многофакторное нейродегенеративное заболевание с выраженным генетическим компонентом. В ходе болезни наблюдается уменьшение числа дофаминергических нейронов в базальных ядрах головного мозга, покрышке среднего мозга и в черном веществе. Патогенез болезни пока с точностью не известен, но за последние двадцать лет учёные изменили мнение о роли генов в формировании характерных для заболевания патологий. Следуя примеру диагностики болезни Альцгеймера, опознаваемого по наличию гена аполипропротеина ε4, ведутся исследования по выявлению мутаций генов, связанных с диагнозом БП.
|
|
|
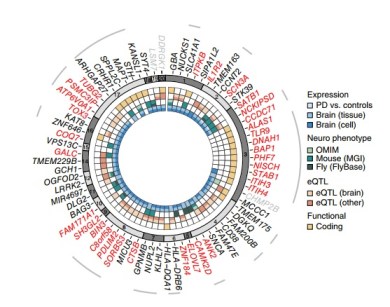
Области мозга с генными аномалиями при болезни Паркинсона.
Благодаря профильному подбору лекарств учёные надеются найти оптимальные медикаментозные методы лечения БП в соответствии с особенностями выявленных дисфункций. Например, при мутации гена LRRK2 (кодирующего белок дардарин), генная активность повышается, в результате чего ускоряются дегенеративные процессы. В этом случае медикаментозное лечение должно быть направлено на подавление этой активности.
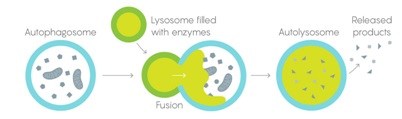
Новейшие исследования посвящены преимущественно внутриклеточным процессам переработки веществ, то есть роли лизосом и аутофагии. Этот процесс и его типология, а также влияние на развитие БП были изучены нобелевским лауреатом 2016 года Ёсинори Осуми.
|
|
|
У пациентов с БП наблюдается накопление альфа-синуклеина, «биомаркера» заболевания. Вместо его нормальной метаболической деградации в клетке патогенная агрегация этого белка влечёт за собой образование т.н. телец Леви в нейронах. Чтобы избежать накопление белка, влекущего за собой формирование патогенных соединений, можно будет задействовать «чистящий» механизм клетки. В перспективе разработки новых стратегий лечения планируется исследовать гены STK39 и ITPKB, поскольку они задействованы в синтезе белков, поддающихся воздействию лекарственных средств (druggable genomes).
Подготовила:Мартемьянова Е.О.
Источники:Diana Chang, Mike A Nalls et al. A meta-analysis of genome-wide association studies identifies 17 new Parkinson’s disease risk loci. Nature Genetics (2017) doi:10.1038/ng.3955
Дата добавления: 2018-02-15; просмотров: 462; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
