Расчётные формулы для расчета количества воздуха, необходимого для горения.
Министерство сельского хозяйства РФ
Федеральное государственное образовательное
учреждение высшего профессионального образования
«Пермская государственная сельскохозяйственная академия
имени академика Д.Н. Прянишникова»
Физико-химические процессы
Горения и взрыва
Практикум
Часть 1
Пермь
ФГОУ ВПО «Пермская ГСХА»
2016
УДК 621.7.148
ББК 79.3
Физико-химические процессы горения и взрыва (ТЕКСТ): практикум сост. Л. В. Куслина, ФГОУ ВПО «Пермская ГСХА», 2010.-72.; 20см.- 50 экз.101с.
Практикум составлен Л. В. Куслиной.
Рецензенты:
Кафедра Безопасности жизнедеятельности Пермского государственного технического университета, заведующий кафедрой доктор технических наук, профессор В.А.Трефилов;
Кафедра физической химии Пермского государственного университета, кандидат химических наук, доцент кафедры физической химии С.П. Шавкунов.
Cборник практических занятий предназначен для студентов очного и заочного обучения инженерного факультета специальности 280101 «Безопасность жизнедеятельности в техносфере». Книга станет хорошим помощником в изучении дисциплины, при проведении практических занятий, подготовке к сдаче экзаменов и зачетов, в написании рефератов по дисциплине «Физико-химические процессы горения и взрыва». Данное учебное пособие соответствует государственному образовательному
Рекомендовано к изданию кафедрой « Безопасность жизнедеятельности» (протокол № от 25.06.2016) и методической комиссией инженерного факультета ( протокол № от 25.06. 2016).
Оглавление
Введение …………………………………………………………………………..4
1.Материальный баланс процесса горения……………………...5
1.1.Практическое занятие №1 по теме: «Расчёт количества воздуха, необходимого для горения веществ»…………………………………….………7
1.2. Практическая работа№2 по теме: «Расчет объема и состава продуктов горения»…………………………………………………………………………..20
2.Тепловой баланс процессов горения ………………………….23
2.1Практическая работа№3 по теме: «Расчет теплоты сгорания веществ»….27
2.2.Практическая работа№4 по теме: «Расчет температуры горения»………32
3.Концентрационные пределы воспламенения………………40
3.1Практическая работа№5 по теме: «Концентрационные пределы воспламенения»………………………………………………………………….43
4Температурные параметры пожарной опасности веществ……………………………………………………………………….55
4.1.Практическая работа№6 по теме: «Расчет температурных пределов воспламенения» …………………………………………………………………61
4.2.Практическая работа№7 по теме: «Расчет температур вспышки
и воспламенения»……………………………………………………………….64
4.3.Практическая работа№8 по теме: «Расчет стандартной температуры самовоспламенения»…………………………………………………………….70
5.Потенциал горючести…………………………………………………77
5.1.Практическая работа№9 по теме: «Потенциал горючести»………………78
Перечень тем и разделов, которые рекомендуются для самостоятельного изучения………………………………………………………………………….83
Контрольные вопросы по курсу« Физико-химические основы горения и взрыва»…………………………………………………………………………...84
Список используемой литературы……………………………………………...88
Приложения……………………………………………………………………...89
Введение
Спецкурс ОПД 05 - «Физико-химические основы горения и взрыва», согласно государственному образовательному стандарту представляет собой совокупность следующих вопросов: физико-химические основы горения; теории горения: тепловая, цепная, диффузионная; виды пламени и скорости его распространения; условия возникновения и развития процессов горения; взрывы: типы взрывов, физические и химические взрывы, классификация взрывов по плотности вещества, по типам химических реакций, энергия и мощность, форма ударной волны, длительность импульса.
Данный практикум предназначен для формирования у студентов практических навыков по спецкурсу «Физико-химические основы горения и взрыва».
В практикуме представлены расчетные работы по следующим темам:
1. Материальный баланс процесса горения;
2. Тепловой баланс процессов горения;
3. Концентрационные пределы воспламенения;
4. Температурные параметры пожарной опасности;
5. Потенциал горючести.
МАТЕРИАЛЬНЫЙ БАЛАНС ПРОЦЕССА ГОРЕНИЯ
Горение - это важнейший из применяемых человеком физико-химических процессов. Роль огня в возникновении и развитии цивилизации необычайно велика. Своеобразное отражение этого факта – миф о Прометее или гениальные догадки философов древности о том, что "огонь" является одним из немногих основных "элементов природы", в настоящее время можно сказать состояний вещества. До сих пор, несмотря на интенсивное развитие атомной, гидро-, гелио- и геотермальной энергетики, за счёт сжигания топлива производится основная доля энергии, обеспечивающей потребности человеческого общества. Все остальные источники, включая продукты питания, дают человечеству менее десяти процентов необходимой ему энергии.
Что же такое горение, роль которого в жизни человеческого общества так велика?
Горение –это режим протекания экзотермических химических реакций, характеризующийся значительной скоростью химического превращения, излучением тепла и света и способностью реакции к прохождению в самоподдерживающемся или самораспространяющемся режиме.
Материальный баланс процесса горения — соотношение (равенство) между количеством веществ, которые вступают в реакцию горения, и количеством веществ (продуктов горения), которые получаются вследствие этой реакции.
Расход воздуха на горение
При горении происходит взаимодействие между молекулами горючего вещества и окислителя, при этом получаются продукты сгорания.
Горючее вещество + Окислитель = Продукты сгорания
Как правило, окислителем при горении выступает кислород воздуха. Схематично химическую реакцию сгорания одного моля вещества в воздухе можно представить уравнением:
ГВ + β(О2 + 3,76 N2) = ∑ ni·ПГi + β·3,76N2,
в котором символами ГВ, О2, N2, ПГi обозначены молекулы, соответственно горючего вещества, кислорода, азота и i-го продукта горения; ni — количество молекул i–го продукта горения, приходящееся на одну молекулу горючего; β — стехиометрический коэффициент реакции горения.
Это лишь суммарная реакция, но она достаточна для проведения практических расчетов и является обобщенной записью материального баланса реакции горения.
Минимальный объем воздуха, который необходим для полного сгорания единицы количества горючего вещества, называется удельным теоретическим объемом воздуха и обозначается V0в.В зависимости от единиц измерения количества горючего вещества (1 моль, 1 м³, 1 кг) удельный объем измеряется в м³/моль, м³/м³, м³/кг.
Действительное количество воздуха, который поступает в зону горения, отличается от теоретического. Соответствующий объем называется удельным действительным объемом воздуха и обозначается vв. Разность между количеством воздуха, который идет на горение и теоретически необходимым, называется избытком воздуха. Для характеристики процесса горения используют понятие коэффициент избытка воздуха - αв., который показывает, во сколько раз количество воздуха, который действительно поступает в зону горения, отличается от теоретически необходимого количества для полного сгорания единицы количества горючего вещества.
Таким образом, действительный удельный объем воздуха равняется:
Vв = v0в · αв.
Часть воздуха, неизрасходованная на горение, переходит в продукты горения.
В случае кинетического горения, при αв = 1, смесь горючего с воздухом является стехиометрической. Величина тепловыделения на единицу продуктов сгорания при этом максимальна, вследствие чего температура в зоне горения также максимальна.
При αв< 1 в смеси недостаток окислителя и излишек горючего вещества. Такая смесь называется богатой. Характерной особенностью процесса горения в этом случае является образование продуктов неполного сгорания.
При αв > 1 смесь называется бедной. В ней недостаток горючего вещества и излишек окислителя. При этом продукты горения включают в себя избыток воздуха.
Продукты горения - это газообразные, твердые и жидкие вещества, образующиеся в процессе горения.
Состав продуктов горения зависит от состава горючего вещества и условий протекания реакции горения. Продукты горения образуют дым.
Дым - дисперсная система, состоящая из твердых и жидких частиц (дисперсной фазы), находящихся в газовой дисперсионной среде.
Свойства дыма характеризуются следующими параметрами:
- Концентрация дыма - это масса продуктов горения, находящихся в единице объема. В зоне задымления концентрация продуктов горения находится в интервале от 1·10–4 до 5·10–3 кг/м³.
- Наличие конденсированной фазы обуславливает непрозрачность дыма. Степень снижения прозрачности зависит от концентрации, размера и природы частиц дисперсной фазы. Параметром, характеризующим оптические свойства дыма, является плотность задымления.
- Плотность задымления — отношение интенсивности света Iп, прошедшего через слой дыма, к интенсивности падающего света Ij.
- Dд = Iп/Iо
-Содержание кислорода. В обычных условиях содержание кислорода в воздухе составляет 21% (объемный). Снижение концентрации кислорода в воздухе приводит к кислородному голоданию людей. Так, при снижении концентрации ниже 16%, работа без индивидуальных средств защиты органов дыхания невозможна.
-Токсичность продуктов горения - способность продуктов горения вызвать отравления людей, находящихся без индивидуальных средств защиты органов дыхания.
-Температура дыма. Температура продуктов горения непосредственно возле зоны горения может достигать 1000°С, но в помещениях температура дыма обычно существенно ниже. Основным фактором, влияющим на температуру дыма, являются условия газообмена. При увеличении коэффициента избытка воздуха температура продуктов горения снижается. Опасной для людей, считается температура выше 70°С. Продолжительное пребывание людей при такой температуре, связано с риском для жизни из-за перегрева организма.
Стойкость дыма определяют такие параметры дымовых частиц, как:
- маленькая масса;
- высокая удельная поверхность;
- броуновское движение, в котором они находятся;
- наличие на их поверхности электрического заряда.
Продукты неполного сгорания, образующиеся при горении веществ и материалов в закрытых помещениях, при поступлении свежего воздуха могут образовывать горючую смесь. Горение при этом происходит в кинетическом режиме (взрыв).
Практическая работа №1
Тема: «Расчёт количества воздуха, необходимого для горения веществ»
Цель работы: Ознакомиться с классификацией процессов горения, сформировать представления про основные параметры, характеризующие пожарную опасность веществ в разных агрегатных состояниях, освоить способы определения этих параметров. Освоить расчеты необходимого количества воздуха для горения.
Расчётные формулы для расчета количества воздуха, необходимого для горения.
Для практических расчётов принимают, что воздух состоит из 21% кислорода и 79% азота. Таким образом, объёмное соотношение азота и кислорода в воздухе составит:
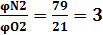 (1.1)
(1.1)
где 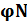 2,
2, 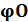 2- это объёмное (% об.) содержание азота и кислорода в окислительной среде.
2- это объёмное (% об.) содержание азота и кислорода в окислительной среде.
Следовательно, на 1м3 (кмоль) кислорода в воздухе приходится 3,76м3(кмоль) азота.
Весовое соотношение азота и кислорода в воздухе можно определить, исходя из соотношения:
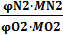 =
= 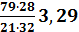
где МN2, 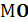 2-молекулярные массы соответственно кислорода и азота.
2-молекулярные массы соответственно кислорода и азота.
Для удобства расчётов горючие вещества разделяют на три типа (таб.1.1).Индивидуальные химические соединения ( метан, уксусная кислота и т.п., вещества сложного состава ( древесина, торф, сланцы, нефть и т. п.),смесь газов (генераторный газ и т.д.)
Таблица 1.1
| ТИП ГОРЮЧИХ ВЕВЕЩЕСТВ | РАСЧЕТНЫЕ ФОРМУЛЫ | № ФОРМУЛЫ | РАЗМЕРНОСТЬ |
| Индивидуальное Вещество | V0B = 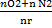
| (1.3а) | М3; 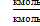
|
V0B = 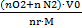
| (1.3б) | 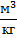
| |
| Вещества сложного состава | V0B =0,269∙( 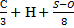 ) )
| (1.4) | 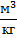
|
| Смесь газов | V0B = 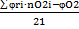
| (1.5) | 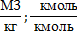
|
Здесь: V0B-теоретическое количество воздуха;
nr, 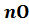 2
2 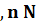 2 количество горючего, кислорода. и азота получаемые из уравнения химической реакции горения кмоль;
2 количество горючего, кислорода. и азота получаемые из уравнения химической реакции горения кмоль;
М- молекулярная масса горючего;
V0- объем 1 моля газа при нормальных условиях (22,4 м3)
C, H, S, O-весовое содержание соответствующих элементов в составе горючего, % ;
 ri-коцентрация i-того горючего компонента, %;
ri-коцентрация i-того горючего компонента, %;
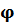 О 2 концентрация кислорода в составе горючего газа, %об.;
О 2 концентрация кислорода в составе горючего газа, %об.;
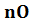 2 i-количество кислорода необходимое для окисления одного i-того кмоля горючего компонента, ккмоль.
2 i-количество кислорода необходимое для окисления одного i-того кмоля горючего компонента, ккмоль.
Для определенного объема воздуха при горении в условиях, отличных от нормальных, пользуются следствием из уравнения состояния идеальных газов:
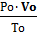 =
= 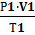 (1.6)
(1.6)
где, 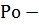 нормальное давление, Па.
нормальное давление, Па.
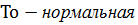 температура, К.
температура, К.
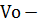 объем воздуха при нормальных условиях;
объем воздуха при нормальных условиях;
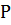 1
1 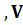 1
1  Т1
Т1 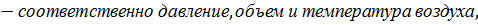
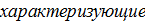 заданные условия горения.
заданные условия горения.
Практическое количество воздуха V0 –объем воздуха, фактически поступивший в зону горения.
Отношение практического объема воздуха к теоретическому называется коэффициентом избытка воздуха 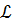 :
:
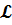 =
= 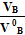 (1.7)
(1.7)
Разность между практическим и теоретическим объемами воздуха называется избытком воздуха ∆ 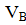 :
:
∆ 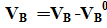 (1.8)
(1.8)
Из (1.7)и (1.8) следует, что
∆ 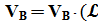 -1) (1.9)
-1) (1.9)
Если известно содержание кислорода в продуктах горения, то коэффициент избытка воздуха определяется по формуле:
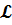 =1+
=1+ 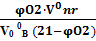 (1.10) где
(1.10) где 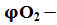 концентрация кислорода в составе горючего газа, % об.;
концентрация кислорода в составе горючего газа, % об.;
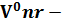 теоретический объем продуктов горения.
теоретический объем продуктов горения.
Для вещества , у которых объем продуктов горения равен объему израсходованного воздуха( например, горение серы и углерода),формула (1.10) упрощается:
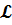 =
= 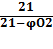 (1.11)
(1.11)
Если содержание кислорода в окислительной среде отличается от содержания его в воздухе, то формулу(1.10) можно записать в виде:
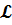 =1+
=1+ 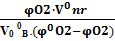 (1.12)
(1.12)
и соответственно формулу (1.11)
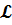 =
= 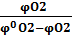 (1.13) ,
(1.13) ,
где 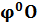 2-содержание кислорода в окислительной среде, % об.
2-содержание кислорода в окислительной среде, % об.
Примеры решения задач.
Пример №1.
Определить теоретическое количество воздуха, необходимого для горения 1м3 метана при нормальных условиях.
Решение: Горючее вещество является индивидуальным химическим соединением, поэтому для расчета его объема надо пользоваться формулой (1.3.а). Запишем уравнение химической реакции горения СН4 в воздухе:
СН4+ 2О2+2∙3,76N2=CО2+2Н2О+2∙3,76N2
Из уравнения находим: no2=2; nN2=2∙3,76=7,52; nCH2=1;тогда
V0B= 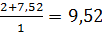 м3/ м3 или кмоль/кмоль
м3/ м3 или кмоль/кмоль
Пример №2
Определить объем теоретического количества воздуха, необходимого для горения 1кг бензола.
Решение: горючее – индивидуальное химическое соединение, поэтому для расчета по формуле (1.3.б) запишем уравнение химической реакции горения:
С2Н2+7,75O2+7,75∙3,76N2=6CO2+3H2O+7,75∙3,75N2 и найдем:
nО2=7,75; nN2=7,5∙3,76=28,2; nr=1,
Молекулярная масса бензола М=6∙12+6∙1=78 объем 1 кмоля газа при нормальных условиях составляет 22.4м3:
V0B=y m:val="p"/></m:rPr><w:rPr><w:rFonts w:ascii="Cambria Math" w:h-ansi="Times New Roman"/><wx:font wx:val="Cambria Math"/><w:color w:val="000000"/><w:sz w:val="28"/><w:sz-cs w:val="28"/></w:rPr><m:t>=10,3</m:t></m:r></m:oMath></m:oMathPara></w:p><w:sectPr wsp:rsidR="00000000"><w:pgSz w:w="12240" w:h="15840"/><w:pgMar w:top="1134" w:right="850" w:bottom="1134" w:left="1701" w:header="720" w:footer="720" w:gutter="0"/><w:cols w:space="720"/></w:sectPr></w:body></w:wordDocument>"> 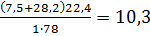 м3/кг
м3/кг
Пример №3
Определить объем воздуха, необходимого для горения 1кг органической массы состава: С-60%, О-25%, N-5%, W-%(влажность), если коэффициент избытка воздуха 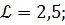 а температура воздуха 305К, давление 995ГПа.
а температура воздуха 305К, давление 995ГПа.
Решение: Так как горючее вещество сложного состава, то теоретическое количество воздуха при нормальных условиях определим по формуле (1.4):
V0B=0,269( 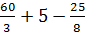 )=5,9 м3/кг
)=5,9 м3/кг
Из формулы (1.7) рассчитаем практическое количество воздуха при нормальных условиях:
V0B= 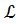 V0B=2,5∙5,9=14,75 м3/кг
V0B=2,5∙5,9=14,75 м3/кг
Находим количество воздуха, пошедшего на горение вещества при заданных условиях горения; используя формулу (1.6), получим:
VB(р,т)=  =16,8 м3/кг
=16,8 м3/кг
Пример №4.
Определить объем воздуха, необходимого для горения 5м3смеси газов, состоящих из 20% СН4, 10% СО, 5%N, 35%О2, если коэффициент избытка воздуха равен 1,8.
Решение:Горючее-смесь газов. Поэтому для расчета объема воздуха, пошедшего на сгорание, воспользуемся формулой (1.5). Для определения стехиометрических коэффициентов при кислороде nо2 запишем уравнение реакции горения горючих компонентов в кислороде:
СН4+2О2=СО2+2Н2О;
С 2Н2+2,5О2=2СО2+Н2О; СО+0,5О2=СО2 тогда
V0B= 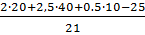 =5,7 м3/кг
=5,7 м3/кг
Для горения 5м3 газовой смеси необходимый теоретический объем воздуха составит: V0B=5∙5,7 =32,5 м3 Практическое количество воздуха : V0B=1,8∙32,5=58,5 м3.
Пример №5
Определите коэффициент избытка воздуха при горении уксусной кислоты, если на горение 1кг поступило 3 м3 воздуха.
Решение: Для определения коэффициента избытка воздуха по формуле (1.7) необходимо рассчитать его теоретическое количество. Молекулярная масса уксусной кислоты-60.
СН3СООН+2О2+2∙3,76N2=2СО2+2∙3,76 N2;
V0B= 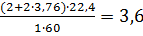 м3/кг
м3/кг
тогда коэффициент избытка воздуха равен:
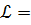
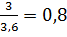
Горение протекало при недостатке воздуха.
Пример №6
Определить объем воздуха, пошедшего на окисление 1м3 аммиака:
NН3+0,75О2 +0,75 3,76 N2=1,5Н2О+0,5N2+0,75∙3,76N2,
тогда
V0B= 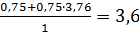 м3/кг
м3/кг
Для определения коэффициента избытка воздуха по формуле (1.10) необходимо рассчитать теоретическое количество продуктов горения 1м3аммиака (см. след параграф 1.2 формула (1.14)):
V0пр= 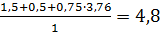 м3/кг
м3/кг
Пример №7
Определить объем окислительной среды, состоящей из 60%О2 и 40%N2,необходимый для горения 1 кг изопропилового спирта, если ее температура равна 295К, давление 620гПа.
Решение: так как окислительная среда отличается по составу от воздуха, определим по формуле (1.1) объемное соотношение кислорода и азота: 40:60+0,67
Уравнение реакции горения изопропилового спирта:
С3Н7ОН+4,5О2+4,5 0,67N2=3СО2+4Н2О+4,5⋅0,67 N2
Теоретический объем окислительной среды при нормальных условиях рассчитаем по формуле (1.3). Молекулярная масса горючего-60.
V0ос= 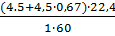 =2,8 м3/кг
=2,8 м3/кг
Объем окислительной среды при заданных условиях горения определим из формулы (1.6):
V0ос(рr)= 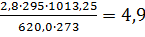 м3/кг
м3/кг
Пример № 8
Определить сколько кг динитротолуола сгорело в герметичном объеме 100м3, если содержание кислорода в продуктах сгорания составило 12%.
Решение: Так как в продуктах горения содержится кислород, то горение протекало в избытке воздуха, коэффициент избытка которого определим по формуле (1.10). Для этого запишем уравнение горения:
С7Н6(NO2)2+6,5O2+6,5∙3,76N2=7CO2+3H2O+N2+6,5∙3,76N2
Молекулярная масса горючего-182.Теоретический объем воздуха равен:
V0B= 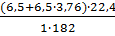 =3,8 м3/кг
=3,8 м3/кг
Теоретический объем продуктов горения (формула1.14):
V0пr= 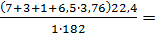 4,4 м3/кг
4,4 м3/кг
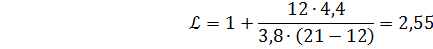
Практический объем воздуха, пошедший на горение:
VB= 2,55 ∙3.8=9,7 м3/кг
Тогда массу сгоревшего динитротолуола Р определим из соотношения:
Рr = 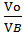 , Рr =
, Рr = 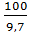 =10,3 кг
=10,3 кг
Контрольные задачи
1. Определить количество (теоретическое) воздуха, необходимое для горения 1кг: метилового, этилового, пропилового и амилового спиртов. Построить график зависимости объема воздуха от молекулярной массы спирта.
2. Определить теоретический объем воздуха, необходимого для горения 1м3: метана, этана, пропана, бутана и пентана. Построить график зависимости объема воздуха от положения вещества в гомологическом ряду (содержания углерода в молекуле вещества).
3. Определить теоретический объем воздуха, пошедший на горение 1кг: метана, метилового спирта. Объяснить причину влияния состава вещества на объем воздуха, требуемый для их горения.
4. Определить объем воздуха, пошедший на горение 1 кг древесины состава: С-47%, Н-8%, О-40%, W-5% если коэффициент избытка воздуха равен 2,8; давление 900ГПа, температура 285К.
5. Сколько воздуха поступило на горение 1кг углерода, если в продуктах горения содержание кислорода составило 17%?
6. Сколько воздуха требуется подать на сжигание 200м3 генераторного газа состава: СО-29%, Н2-14% , СН4-3%, СО2-6,5%, N2-45%, O2-2,5% если коэффициент избытка воздуха равен 2,5?
7. Определить количество сгоревшего толуола, кг. в помещении объемом 400 м3,если после пожаре при отсутствии газообмене установлено, что содержание кислорода снизилось до 17%.
8. Сколько м3хлора поступило на горение 300м3 водорода, если в продуктах горения избыток окислителя составил 80м3?
9. Определить избыток воздуха в продуктах горения газовой смеси состава: СО-15%, С4Н10-45%,О2-30%,N2-10% если коэффициент избытка равен 1,2 ;температура 265К; давление 850ГПа
10. Сколько м3 окислительной среды, состоящей из 50% кислорода, 50% азота, необходимо для горения 8кг этилацетата, если коэффициент избытка равен 1,2; температура 265К; давление 850 ГПа.
11. Определить коэффициент избытка окислительной среды, состоящей из 70% кислорода и 30% азота, если при горении серы содержание кислорода снизилось до 55%. Определить количество сгоревшей серы, кг , если объем помещения равен 180 м3.
12. Сколько антрацита (принять, что содержание углерода равно 100%) сгорело в помещении объемом 150м3, если прекращение горения наступило при снижении кислорода до 13%, газообмен не учитывать
Дата добавления: 2018-02-15; просмотров: 8663; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
