Растворимость белков, свойства растворов белков.
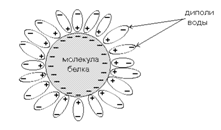
Растворимость белков в воде зависит от всех перечисленных выше свойств белков: формы, молекулярной массы, величины заряда, соотношения полярных и неполярных функциональных групп на поверхности белка. Кроме этого, растворимость белка определяется составом растворителя, т.е. наличием в растворе других растворённых веществ. Например, некоторые белки легче растворяются в слабом солевом растворе, чем в дистиллированной воде. С другой стороны, увеличение концентрации нейтральных солей может способствовать вьшадению определённых белков в осадок. Денатурирующие агенты, присутствующие в растворе, также снижают растворимость белков.
Физико-химические свойства белков
Физико-химические свойства белков определяются их аминокислотным составом и пространственной структурой (организацией). Белки обладают следующими основными свойствами:
– кислотно-основными;
– буферными;
– осмотическими;
– оптическими;
– растворимостью;
– осаждаемостью;
– денатурацией.
Кислотно-основные свойства белков (электрические)
Белки являются амфотерными полиэлектролитами. Амфотерность белкам придают кислотные и основные группы боковых радикалов аминокислот и концевые аминогруппа (NH3+) и карбоксильная группа (COO–) полипептидного остова, поскольку другие α-амино- и α-карбоксильные группы участвуют в образовании пептидных связей.
Коллоидные и осмотические свойства белков
Водные растворы белков являются устойчивыми и равновесными, они со временем не коагулируют и не требуют присутствия стабилизаторов. Поскольку белковые растворы гомогенны, то напоминают истинные растворы, однако высокая молекулярная масса белков придает их растворам свойства коллоидных систем:
1. Оптические свойства белков
Растворы белков способны рассеивать лучи видимого света (эффект дифракции или явление Тиндаля). Луч света, проходя через раствор белка, преломляется и свет рассеивается. На данном физико-химическом свойстве белков основан метод количественного определения белка рефрактометрически (в чистых белковых растворах, например, в сыворотке крови).
2. Малая скорость диффузии – способствует равномерному распределению белков внутри клетки, между клеткой и кровью, а также препятствует скоплению белка в местах его биосинтеза.
3. Осмотические свойства белков
Белки в клетке, межклеточной жидкости, в крови повышают осмотическое давление и вызывают явление осмоса, т.е. перемещение ионов Nа+ и воды через мембраны в раствор белка.
Неспособность белков проникать через полупроницаемые мембраны вследствие высокой молекулярной массы используется в практике для очистки белков от низкомолекулярных примесей (солей, биогенных аминов, мочевины и др.) – процесс диализа.
4. Высокая вязкость белковых растворов
С увеличением концентрации белка вязкость раствора повышается, поскольку повышаются силы сцепления между поверхностями белковых молекул.
При повышении температуры вязкость белковых растворов понижается. Добавление некоторых солей кальция приводит к повышению вязкости, поскольку ионы Са2+ способствуют сцеплению молекул с помощью кальциевых мостиков. Иногда вязкость белкового раствора в присутствии Са2+ настолько увеличивается, что он теряет текучесть и превращается в гель.
5. Способность белков к образованию гелей
Денатурация белков, типы денатурации.
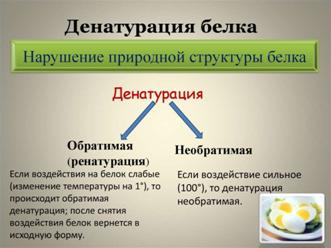
ДЕНАТУРАЦИЯ - это лишение белка его природных, нативных свойств, сопровождающееся разрушением четвертичной (если она была), третичной, а иногда и вторичной структуры белковой молекулы, которое возникает при разрушении дисульфидных и слабых типов связей, участвующих в образовании этих структур. Первичная структура при этом сохраняется, потому что она сформирована прочными ковалентными связями. Разрушение первичной структуры может произойти только в результате гидролиза белковой молекулы длительным кипячением в растворе кислоты или щелочи.
Факторы, вызывающие денатурацию белков
Факторы, которые вызывают денатурацию белков, можно разделить на физические и химические.
Физические факторы
1. Высокие температуры. Для разных белков характерна различная чувствительность к тепловому воздействию. Часть белков подвергается денатурации уже при 40-500С. Такие белки называют термолабильными. Другие белки денатурируют при гораздо более высоких температурах, они являются термостабильными.
2. Ультрафиолетовое облучение
3. Рентгеновское и радиоактивное облучение
4. Ультразвук
5. Механическое воздействие (например, вибрация).
Химические факторы
1. Концентрированные кислоты и щелочи. Например, трихлоруксусная кислота (органическая), азотная кислота (неорганическая).
2. Соли тяжелых металлов (например, CuSO4).
3. Органические растворители (этиловый спирт, ацетон)
4. Растительные алкалоиды.
5. Мочевина в высоких концентрациях
5. Другие вещества, способные нарушать слабые типы связей в молекулах белков.
Воздействие факторами денатурации применяют для стерилизации оборудования и инструментов, а также как антисептики.
Дата добавления: 2018-02-15; просмотров: 1706; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
