Й способ – через степень гидролиза.
По определению: b = c Г / c 0 = [ OH ]/ c 0 Þ [ OH ] = b × c 0
рН = 14 – рОН = 14 + lg [ OH ] = 14 + lg b × c 0
а) b - по строгой формуле;
б) b - по приближенной формуле (если КГ < 10-4):
b ≈ 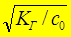 =
= 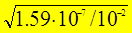 = 4 × 10 - 3 << 1 Þ
= 4 × 10 - 3 << 1 Þ
Расчет по приближенной формуле правомерен.
[ OH ] = b × c 0 = 4 × 10 - 3 × 10 - 2 = 4 × 10 - 5
рН = 14 + lg [ OH ] =14 - 4,4 = 9,6
Задача 6
Определить сР MgF 2 , в растворе, в котором g ( Mg 2+ ) = 0,7; g ( F - ) = 0,96
Решение:
MgF 2 (тв) Û Mg 2+ (нас.р-р) + 2 F - (нас.р-р)
Ср 2 Ср
ПР( MgF 2 ) = 4 × 10-9 = 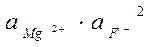
а Mg2+ = g ( Mg2+ ) ∙ Ср
а F ¯ = g ( F¯ ) ∙ 2 Ср
сР = 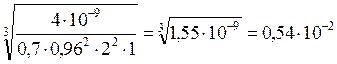 моль/л
моль/л
Растворимость зависит от
1) ионной силы раствора – введение растворимого электролита, не имеющего общих ионов
ПР = gMg2+ ×сMg2+ ×gF-2×сF-2
С ↑ I ионной силы раствора Þ g i ↓ Þ сР ↑
Введения одноименного иона
MgF 2 (тв) Û Mg 2+ (нас.р-р) + 2 F - (нас.р-р)
NaF (р-р) → Na + (р-р) + F - (р-р)
с F - ↑ Þ равновесие смещается влево Þ с Р ↓
Дата добавления: 2021-05-18; просмотров: 42; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
