Изомерия — это явление существования разных веществ — изомеров с одинаковым качественным и количественным составом, т. е. одинаковой молекулярной формулой.
Предмет органической химии. Органические вещества
Органической химией изначально называлась химия веществ, полученных из организмов растений и животных. С такими веществами человечество знакомо с глубокой древности. Люди умели получать уксус из прокисшего вина, а эфирные масла из растений, выделять сахар из сахарного тростника, извлекать природные красители из организмов растений и животных.
Химики разделяли все вещества в зависимости от источника их получения на минеральные (неорганические), животные и растительные (органические).
Долгое время считалось, что для получения органических веществ нужна особая «жизненная сила» — vis Vitalis, которая действует только в живых организмах, а химики способны всего лишь выделять органические вещества из продуктов.

Шведский химик Й. Я. Берцелиус, президент Королевской шведской Академии наук. Научные исследования охватывают все главные проблемы общей химии первой половины XIX в. Экспериментально проверил и доказал достоверность законов постоянства состава и кратных отношений применительно к неорганическим оксидам и органическим соединениям. Определил атомную массу 45 химического элемента. Ввел современные обозначения химических элементов и первые формулы химических соединений.
Берцелиус определил органическую химию как химию растительных или животных веществ, образующихся под влиянием «жизненной силы». Именно Берцелиус ввел понятия органические вещества и органическая химия .
|
|
|
Развитие химии привело к накоплению большого количества фактов и к краху учения о «жизненной силе» — витализма.
Немецкий ученый Ф. Вёлер в 1824 г. осуществил первый синтез органических веществ — получил щавелевую кислоту путем взаимодействия двух неорганических веществ — дициана и воды:
N≡C—С≡N + 4Н2О → СООН + 2NН3
|
СООН
дициан щавелевая кислота
А в 1828 г. Вёлер, нагревая водный раствор неорганического вещества цианата аммония, получил мочевину — продукт жизнедеятельности животных организмов:

Изумленный таким результатом, Вёлер написал Берцелиусу: «Должен сказать Вам, что я умею приготовить мочевину, не нуждаясь ни в почке, ни в животном организме вообще...»
Вёлер Фридрих (1800-—1882)

Немецкий химик. Иностранный член Петербургской Академии наук (с 1853 г.). Его исследования посвящены как неорганической, так и органической химии. Открыл циановую кислоту (1822), получил алюминий (1827), бериллий и иттрий (1828).
В последующие годы блестяшие синтезы анилина Г. Кольбе и Э. Франклендом (1842), жира М. Бертло (1854), сахаристых веществ А. Бутлеровым (1861) и др. окончательно похоронили миф о «жизненной силе».
|
|
|
Появилось классическое определение К. Шорлеммера, не потерявшее своего значения и более 120 лет спустя:
«Органическая химия есть химия углеводородов и их производных, т. е. продуктов, образующихся при замене водорода другими атомами или группами атомов».
Сейчас органическую химию чаще всего называют химией соединений углерода. Почему же из более чем ста элементов Периодической системы Д. И. Менделеева природа именно углерод положила в основу всего живого? Ответ на этот вопрос неоднозначен. Многое вам станет понятно, когда вы рассмотрите строение атома углерода и поймете слова Д. И. Менделеева, сказанные им в «Основах химии» об этом замечательном элементе: «Углерод встречается в природе как в свободном, так и в соединительном состоянии, в весьма различных формах и видах... Способность атомов углерода соединяться между собой и давать сложные частицы проявляется во всех углеродистых соединениях... Ни в одном из элементов... способности к усложнению не развито в такой степени, как в углероде... Ни одна пара элементов не дает столь много соединений, как углерод с водородом».
Строение атома углерода
В настоящее время органическую химию рассматривают как химию соединений углерода, но, отдавая дань уважения истории, по-прежнему продолжают называть ее органической химией. Поэтому так важно более подробно рассмотреть строение атома этого элемента, характер и пространственное направление образуемых им химических связей.
|
|
|
Атом углерода состоит из ядра, имеющего положительный заряд +6 (так как содержит шесть протонов), и электронной оболочки, на которой находятся шесть электронов, расположенных на двух энергетических уровнях (слоях):

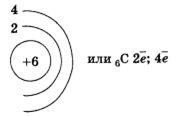
Реальное строение атома углерода гораздо сложнее, чем представлено на приведенной схеме.
Дело в том, что «живущий» в пространстве вокруг ядра электрон обладает одновременно свойствами и частицы (имеет массу 1/1840 от массы протона или нейтрона), и волны (способен к огибанию препятствий — дифракции, характеризуется определенной амплитудой, длиной волны, частотой колебаний и т. д.). Нельзя точно определить положение электрона в пространстве вокруг ядра. Поэтому говорят о большей или меньшей вероятности пребывания электрона в данной области пространства. Если бы мы могли сфотографировать атом и на снимке положение электрона отражалось бы в виде точки, то при наложении огромного числа таких снимков мы получили бы картину электронного облака. Чем больше плотность этого облака, тем с большей вероятностью электрон находится в этой области.
|
|
|
Пространство вокруг ядра, в котором заключено 90% электронного облака, называется орбиталью. Это означает, что 90% времени электрон находится в этом ограниченном пространстве. В дальнейшем мы будем понимать термины «орбиталь» и «облако» как равноценные.
Атом углерода имеет два вида орбиталей: s-орбитали сферической формы и р-орбитали в форме гантели или объемной восьмерки (рис. 2).
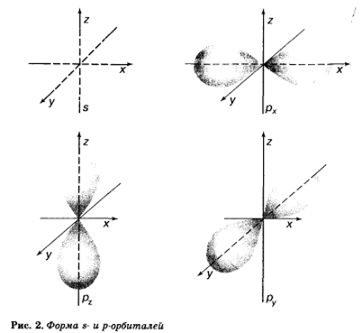

Эти орбитали отличаются друг от друга не только формой, но и удаленностью от ядра атома. Чем более удалена от ядра орбиталь, тем большую энергию имеет электрон на этой орбитали. Энергия электрона — важнейшая характеристика его состояния. Причем, и это очень важно, энергия электрона в атоме может принимать только определенные значения, а сам электрон может занимать орбиталь на определенном расстоянии от ядра. Эти орбитали отличаются запасом (уровнем) энергии.
Чтобы различать энергетические уровни, их нумеруют в порядке удаления от ядра. Ближайший к ядру — первый (1), затем второй (2) и т. д.
В атоме углерода первый уровень составляет одна s-орби-таль, на которой находятся два электрона. Второй энергетический уровень атома углерода также содержит s-орбиталь, но большего размера, так как запас энергии электронов на ней выше, чем у электронов первого уровня, а также три р-орбитали. Это гантелеобразные орбитали одного размера, которые взаимно перпендикулярны, подобно осям координат х, у и 2 (см. рис. 2). Каждую орбиталь могут занимать два электрона, но с противоположными значениями спинов.
Спин (от англ. to spin — вращаться) — это собственный магнитный момент электрона (при введении понятия «спин» в 1925 г. предполагали, что магнитные свойства электрона как заряженной частицы вызваны его вращением вокруг собственной оси). Спин электрона появляется лишь при взаимодействии его с другими электронами и с внешним магнитным полем. Спин может иметь только два значения — положительное и отрицательное.
Чтобы представить расположение электронов в атоме, надо помнить, что каждый электрон занимает энергетически наиболее выгодное положение, при котором запас его энергии будет наименьшим. Он всегда стремится занять наиболее близкое к ядру положение и попасть на орбиталь более простой формы (например, сначала на s-, а уж потом на р-орбиталь). А если в пределах одного уровня имеется несколько одинаковых орбиталей, электроны размещаются вначале каждый на отдельной орбитали с одинаковыми спинами, а уж затем попарно, но с противоположными спинами.
Соответственно электронная формула атома углерода будет иметь вид 1s22s22p2.
Очень часто строение электронных оболочек атомов отображают с помощью электронно-графических формул. В них каждая орбиталь обозначается одной клеткой; каждый электрон — стрелкой; направление стрелки соответствует направлению спина.
Изобразим электронно-графические формулы атомов углерода
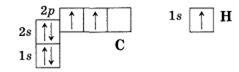
Валентность химического элемента чаще всего определяется числом неспаренных электронов. Атом углерода, как видно из электронно-графической формулы, имеет два неспаренных электрона, поэтому с их участием могут образоваться две электронные пары, осуществляющие две ковалентные связи.
Однако в органических соединениях углерод не двух-, а всегда четырехвалентен. Это можно объяснить тем, что в возбужденном (получившем дополнительную энергию) атоме происходит распаривание 2«-электронов и переход одного из них на 2р-орбиталь:
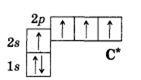

Такой атом имеет четыре неспаренных электрона и может принимать участие в создании четырех ковалентных связей.
Для образования ковалентной связи необходимо, чтобы орбиталь одного атома перекрывалась с орбиталью другого. При этом чем больше перекрывание, тем прочнее связь.
Химические связи, образующиеся в результате перекрывания электронных орбиталей вдоль линии связи, называются σ-связями (сигма-связями).
Линия связи — прямая, соединяющая ядра атомов. Для s-орбиталей возможен лишь единственный способ перекрывания — с образованием σ-связей.
р-орбитали могут перекрываться с образованием σ-связей, а также могут перекрываться в двух областях, образуя ковалентную связь другого вида — за счет «бокового» перекрывания:


Химические связи, образующиеся в результате «бокового» перекрывания электронных орбиталей вне линии связи, т. е. в двух областях, называются п-связями (пи-связями).
Рассмотренный вид связи характерен для молекул этилена С2Н4, ацетилена С2Н2 (двойные и тройные связи). Но об этом более подробно мы узнаем чуть позже
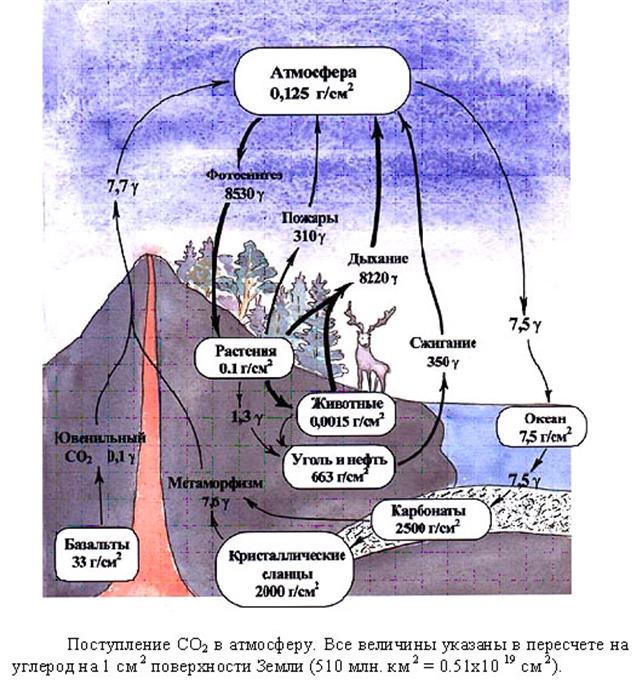
Многочисленные связи атомов углерода между собой и с атомами других элементов (водорода, кислорода, азота, серы, фосфора), входящих в состав органических веществ, могут разрушаться под влиянием природных факторов. Поэтому углерод совершает непрерывный круговорот в природе: из атмосферы (углекислый газ) — в растения (фотосинтез), из растений — в животные организмы, из живого — в мертвое, из мертвого — в живое...
Органические вещества имеют ряд особенностей, которые отличают их от неорганических веществ:
1. Неорганических веществ насчитывается немногим более 100 тыс., тогда как органических — почти 18 млн
2. В состав всех органических веществ входят углерод и водород, поэтому большинство из них горючи и при горении обязательно образуют углекислый газ и воду.
3. Органические вещества построены более сложно, чем неорганические, и многие из них имеют огромную молекулярную массу, например те, благодаря которым происходят жизненные процессы: белки, жиры, углеводы, нуклеиновые кислоты и т. д.
4. Органические вещества можно расположить в ряды сходных по составу, строению и свойствам — гомологов.
Гомологическим рядом называется ряд веществ, расположенных в порядке возрастания их относительных молекулярных масс, сходных по строению и химическим свойствам, где каждый член отличается от предыдущего на гомологическую разность СН2.
Таблица 1. Рост числа известных органических соединений
| Год | Число известных органических соединений |
| 1880 | 12 000 |
| 1910 | 150 000 |
| 1940 | 500 000 |
| 1960 | 1 000 000 |
| 1970 | 2 000 000 |
| 1980 | 5 500 000 |
| 2000 | 18 000 000 |
5. Для органических веществ характерной является изомерия, очень редко встречающаяся среди неорганических веществ.
Изомерия — это явление существования разных веществ — изомеров с одинаковым качественным и количественным составом, т. е. одинаковой молекулярной формулой.
Величайшим обобщением знаний о неорганических веществах является Периодический закон и Периодическая система элементов Д. И. Менделеева. Для органических веществ аналогом такого обобщения служит теория строения органических соединений А. М. Бутлерова.
Для количественной характеристики способности атомов одного химического элемента соединяться с определенным числом атомов другого химического элемента в неорганической химии, где большинство веществ имеет немолекулярное строение, применяют понятие "степень окисления". В органической химии, где большинство соединений имеет молекулярное строение, используют понятие «валентность».
Дата добавления: 2021-05-18; просмотров: 175; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
