Составьте молекулярное уравнение реакции между гидроксидом алюминия и соляной кислотой (HCl).
Ответ:____________________________________________________________
2) Укажите, какие свойства (оснόвные или кислотные) проявляет гидроксид алюминия в данной реакции. Ответ:___________________________________________________________________
 |
Дана схема превращений: Zn → ZnSO4 → ZnCl2 → Zn(OH)2
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Ответ:
1)________________________________________________________________________________
2)________________________________________________________________________________
3)________________________________________________________________________________
 Установите соответствие между формулой органического вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Установите соответствие между формулой органического вещества и классом/группой, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | КЛАСС/ГРУППА |
| А) CH4 Б) C6H5OH В) HCHO | 1) спирты 2) альдегиды 3) фенолы 4) углеводороды |
Запишите в таблицу выбранные цифры под соответствующими буквами.
Ответ:
| А | Б | В |
 |
В автомобильных свинцово-кислотных аккумуляторах в качестве электролита применяется 35%-ный раствор серной кислоты в дистиллированной воде. Рассчитайте массы безводной серной кислоты и дистиллированной воды, которые необходимы для приготовления 600 г такого раствора. Запишите подробное решение задачи.
| Дано: | Решение: |
Перевод баллов в оценку:
19-20 - "5"
|
|
|
16-18 - "4"
11-15 - "3"
10 - "2"
Вариант
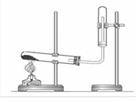
 Из курса химии Вам известно, что при получении газообразных веществ в лаборатории собирать получаемый газ можно двумя способами: вытеснением воды и вытеснением воздуха. На рис. 1–3 изображены приборы для получения и собирания различных газов.
Из курса химии Вам известно, что при получении газообразных веществ в лаборатории собирать получаемый газ можно двумя способами: вытеснением воды и вытеснением воздуха. На рис. 1–3 изображены приборы для получения и собирания различных газов.

| 
| 
|
| Рис. 1 | Рис. 2 | Рис. 3 |
Определите, какие из указанных приборов можно использовать для получения и собирания в лаборатории:
а) аммиака;
б) хлороводорода.
Запишите в таблицу номер рисунка и название соответствующего способа собирания газа.
 |
Ответ:
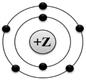
 На рисунке изображена модель электронного строения атома некоторого химического элемента.
На рисунке изображена модель электронного строения атома некоторого химического элемента.
На основании предложенной модели выполните следующие задания:
1) запишите порядковый номер химического элемента, которому соответствует данная модель атома;
2) запишите номер периода и номер группы в Периодической системе химических элементов Д.И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот элемент.
Ответы запишите в таблицу:
| Порядковый номер химического элемента | № периода | № группы | Металл/ неметалл |
|
|
|
 Периодическая система химических элементов Д.И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента радиусы атомов в периодах уменьшаются, а в группах увеличиваются.
Периодическая система химических элементов Д.И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента радиусы атомов в периодах уменьшаются, а в группах увеличиваются.
Учитывая эти закономерности, расположите в порядке уменьшения радиуса атомов следующие элементы: Si , O , N , P . Запишите символы элементов в нужной последовательности.
Ответ:
 В приведённой ниже таблице перечислены характерные свойства веществ с молекулярной и атомной кристаллической решёткой.
В приведённой ниже таблице перечислены характерные свойства веществ с молекулярной и атомной кристаллической решёткой.
| Характерные свойства веществ | |
| С молекулярной кристаллической решёткой | С атомной кристаллической решёткой |
| · При обычных условиях могут находиться в одном из трёх агрегатных состояний; · имеют низкие значения температур кипения и плавления; · имеют низкую теплопроводность; · летучие | · Твёрдые; · прочные; · тугоплавкие; · нелетучие |
Используя данную информацию, определите, какую кристаллическую решётку имеют вещества. Ответ:
|
|
|
1) Углекислый газ (СО2) имеет
2) Алмаз (С) имеет

В пищевой промышленности используется добавка Е338, которая представляет собой ортофосфорную кислоту (H3PO4). Применяется она в основном как консервант, фиксатор цвета продуктов, регулятор кислотности.
Получение ортофосфорной кислоты можно проводить различными способами, один из которых заключается во взаимодействии оксида фосфора(V) P2O5 с водой.
При взаимодействии ортофосфорной кислоты с основаниями образуются её соли – ортофосфаты. Они также широко применяются в промышленности. Так, например, ортофосфат натрия (Na3PO4). используется в составе чистящих и моющих средств, стиральных порошков и отбеливателей. Это соединение часто используют для «смягчения» (устранения жёсткости) воды. Жёсткость воды обусловлена присутствием в ней растворимых солей кальция и магния (хлоридов, гидрокарбонатов и др.). Смягчение воды необходимо, поскольку использование жёсткой воды в промышленности вызывает появление осадка (накипи) на стенах котлов, в трубах, а также существенно увеличивает расход моющих средств.
|
|
|
 Сложные неорганические вещества условно можно распределять, то есть классифицировать, по четырём классам, как показано на схеме. В эту схему впишите недостающие название класса и три формулы веществ (из текста), являющихся представителями соответствующих классов.
Сложные неорганические вещества условно можно распределять, то есть классифицировать, по четырём классам, как показано на схеме. В эту схему впишите недостающие название класса и три формулы веществ (из текста), являющихся представителями соответствующих классов.
Ответ:
| Сложные вещества |

| Оксиды | Кислоты
| Соли | |||
| КОН |
| ||||
 1) Составьте молекулярное уравнение реакции получения ортофосфорной кислоты.
1) Составьте молекулярное уравнение реакции получения ортофосфорной кислоты.
Ответ:
2) Укажите, к какому типу (соединения, разложения, замещения, обмена) относится эта реакция. Ответ:
 1) Составьте молекулярное уравнение реакции между ортофосфорной кислотой (H 3PO 4 ) и основанием – гидроксидом натрия ( NaOH ). Ответ:
1) Составьте молекулярное уравнение реакции между ортофосфорной кислотой (H 3PO 4 ) и основанием – гидроксидом натрия ( NaOH ). Ответ:
2) Укажите, к какому типу (соединения, разложения, замещения, обмена) относится эта реакция. Ответ:
 Дана схема превращений:
Дана схема превращений:
SO 2 → SO 3 → K 2 SO 4 → KOH
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Ответ:
1)
2)
3)
 Установите соответствие между формулой органического вещества и его названием: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Установите соответствие между формулой органического вещества и его названием: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | НАЗВАНИЕ |
| А) С6Н5ОН | 1) ацетилен |
| Б) С2Н2 | 2) глюкоза |
| В) С6Н12О6 | 3) этанол |
| 4) фенол |
Запишите в таблицу выбранные цифры под соответствующими буквами
Ответ:
| А | Б | В |
 В медицине в качестве гипертонического раствора используют 20%-ный раствор глюкозы в воде. Рассчитайте массу глюкозы и воды, которые необходимы для приготовления 500 г такого раствора. Запишите подробное решение задачи.
В медицине в качестве гипертонического раствора используют 20%-ный раствор глюкозы в воде. Рассчитайте массу глюкозы и воды, которые необходимы для приготовления 500 г такого раствора. Запишите подробное решение задачи.
| Дано: | Решение: |
Перевод баллов в оценку:
19-20 - "5"
16-18 - "4"
11-15 - "3"
10 - "2"
Вариант
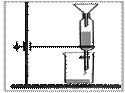
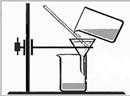
 Из курса химии Вам известны следующие способы разделения смесей: отстаивание, фильтрование, дистилляция (перегонка), действие магнитом, выпаривание, кристаллизация.
Из курса химии Вам известны следующие способы разделения смесей: отстаивание, фильтрование, дистилляция (перегонка), действие магнитом, выпаривание, кристаллизация.
На рис. 1 и 2 изображены два из названных способов.
| 
|
| Рис. 1 | Рис. 2 |
Из числа перечисленных ниже смесей выберите те, которые можно разделить с помощью способов, изображённых на рисунках.
а) речной песок и древесные опилки
б) вода и оливковое масло
в) сахарный песок и крахмал
г) мел и вода
Запишите в соответствующие графы таблицы названия выбранных смесей, номер соответствующего рисунка и название способа разделения смеси.
 |
Ответ:
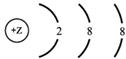
 На рисунке изображена схема распределения электронов по энергетическим уровням в атоме некоторого химического элемента.
На рисунке изображена схема распределения электронов по энергетическим уровням в атоме некоторого химического элемента.
На основании предложенной схемы выполните следующие задания:
1) запишите символ химического элемента, которому соответствует данная схема строения атома;
2) запишите номер периода и номер группы в Периодической системе химических элементов Д.И. Менделеева, в которых расположен этот элемент;
3) определите, к металлам или неметаллам относится простое вещество, которое образует этот элемент.
 |
Ответы запишите в таблицу:
 Периодическая система химических элементов Д.И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента радиусы атомов в периодах уменьшаются, а в группах увеличиваются.
Периодическая система химических элементов Д.И. Менделеева – богатое хранилище информации о химических элементах, их свойствах и свойствах их соединений. Так, например, известно, что с увеличением порядкового номера химического элемента радиусы атомов в периодах уменьшаются, а в группах увеличиваются.
Учитывая эти закономерности, расположите в порядке уменьшения радиуса атомов следующие элементы: B , Al , C , N . Запишите символы элементов в нужной последовательности.
Ответ:
 В приведённой ниже таблице представлены некоторые характеристики ковалентной и ионной видов химической связи.
В приведённой ниже таблице представлены некоторые характеристики ковалентной и ионной видов химической связи.
| Химическая связь | |
| Ковалентная | Ионная |
| Образована атомами одного и того же элемента-неметалла или атомами различных неметаллов | Образована атомами металла и неметалла |
Используя данную информацию, определите вид химической связи в молекулах.
Ответ:
1) В молекуле оксида углерода (IV) (СО2) _______________________________________________
2) В молекуле хлороводорода (HCl) _____________________________________________________
Сульфат меди(II) (CuSO4) – важнейшая из солей меди. Кристаллогидрат сульфата меди(II) называют медным купоросом. В сельском хозяйстве медный купорос применяется как антисептик, фунгицид и медно-серное удобрение.
В промышленности эту соль применяют в производстве ацетатного волокна, а также используют в качестве фиксатора окраски и консерванта.
Сульфат меди(II) в промышленности получают различными способами, например растворением оксида меди(II) (CuO) в серной кислоте (H2SO4).
Эта соль часто служит исходным сырьём для получения других соединений, например гидроксида меди(II) (Cu(OH)2). Для водного раствора сульфата меди(II) возможна реакция с металлами активнее меди, например с цинком.
Сульфат меди(II) является соединением с умеренной токсичностью. Однако работать с порошком или пудрой сульфата меди(II) следует осторожно, не допуская их пыления.
 |
Сложные неорганические вещества условно можно распределять, то есть классифицировать, по четырём классам, как показано на схеме. В эту схему впишите недостающие название класса и три формулы веществ (из текста), являющихся представителями соответствующих классов.
Ответ:
| Сложные вещества |

| Оксиды | Основания | Соли | |
| H2SO4 |
1)  Составьте молекулярное уравнение реакции цинка с раствором сульфата меди(II).
Составьте молекулярное уравнение реакции цинка с раствором сульфата меди(II).
Ответ:
Дата добавления: 2021-04-15; просмотров: 268; Мы поможем в написании вашей работы! |

Мы поможем в написании ваших работ!
